Benzene: formula. Benzene: struttura elettronica, proprietà
Gli idrocarburi aromatici sono una parte importante della serie ciclica composti organici. Il rappresentante più semplice di tali idrocarburi è il benzene. La formula di questa sostanza non solo la distingueva da un certo numero di altri idrocarburi, ma dava anche impulso allo sviluppo di una nuova direzione nella chimica organica.
Scoperta di idrocarburi aromatici
Gli idrocarburi aromatici furono scoperti all'inizio del XIX secolo. A quei tempi, il combustibile più comune per l'illuminazione stradale era l'illuminazione del gas. Dal suo condensato, il grande fisico inglese Michael Faraday individuò tre grammi di sostanza oleosa nel 1825, descrisse dettagliatamente le sue proprietà e lo chiamò: idrogeno cementato. Nel 1834, uno scienziato tedesco, il chimico Mitscherlich, riscaldando l'acido benzoico con la calce, ottenne il benzene. La formula con cui è stata condotta questa reazione è la seguente:
Ad
C6 H5 COOH + CaO fusion C6 H6 + CaCO3.
A quel tempo, acido benzoico raro è stato ottenuto dalla resina benzoica, che può essere rilasciata da alcune piante tropicali. Nel 1845, un nuovo composto fu trovato nel catrame di carbone, che era una materia prima abbastanza economica per ottenere una nuova sostanza su scala industriale. Un'altra fonte di benzene è l'olio prodotto in alcuni campi. Per soddisfare le esigenze industriali del benzene, è anche prodotto dall'aromatizzazione di alcuni gruppi di idrocarburi di petrolio aciclici.
La versione moderna del nome suggerita dallo scienziato tedesco Liebig. La radice della parola "benzene" dovrebbe essere cercata nelle lingue arabe - lì è tradotto come "incenso".
Proprietà fisiche del benzene
Il benzene è un liquido incolore con un odore specifico. Questa sostanza bolle ad una temperatura di 80,1 ° C, indurisce a 5,5 ° C e si trasforma in una polvere cristallina bianca. Il benzene praticamente non conduce calore ed elettricità, è scarsamente solubile in acqua e bene - in vari oli. Le proprietà aromatiche del benzene riflettono l'essenza della struttura della sua struttura interna: un nucleo benzenico relativamente stabile e una composizione indefinita.
Ad
Classificazione chimica del benzene

Il benzene e i suoi omologhi - toluene ed etilbenzene - sono una serie aromatica di idrocarburi ciclici. La struttura di ciascuna di queste sostanze contiene una struttura comune chiamata anello benzenico. La struttura di ciascuna delle sostanze di cui sopra contiene uno speciale raggruppamento ciclico creato da sei atomi di carbonio. Si chiama anello benzenico aromatico.
Storia della scoperta
L'istituzione della struttura interna del benzene si è estesa per diversi decenni. I principi di base della struttura (modello ad anello) furono proposti nel 1865 dal chimico A. Kekule. Come dice la leggenda, lo scienziato tedesco ha visto la formula di questo elemento in un sogno. Successivamente è stato proposto di semplificare la scrittura della struttura di una sostanza, il cosiddetto: benzene. La formula per questa sostanza è un esagono. I simboli del carbonio e dell'idrogeno, che dovrebbero essere localizzati agli angoli dell'esagono, sono omessi. Quindi, risulta semplice esagono regolare con alternanza di linee singole e doppie sui lati. La formula generale del benzene è mostrata nella figura sottostante. 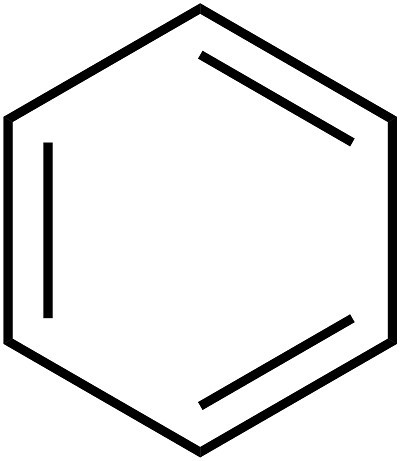
Idrocarburi aromatici e benzene
La formula chimica di questo elemento suggerisce che le reazioni di addizione non sono caratteristiche del benzene. Per questo, così come per altri elementi della serie aromatica, sono tipiche le reazioni di sostituzione degli atomi di idrogeno nell'anello benzenico.
Ad
Reazione di solfonazione
Garantendo che l'interazione sia concentrata acido solforico e benzene, aumentando la temperatura di reazione, si possono ottenere acido benzosolfonico e acqua. La formula strutturale del benzene in questa reazione è la seguente: 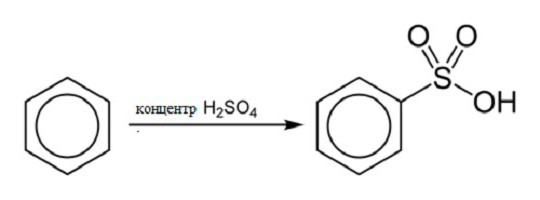
Reazione di alogenazione
Il bromo o il cromo in presenza di un catalizzatore reagisce con il benzene. Questo produce derivati alogeni. Ma la reazione di nitrazione avviene utilizzando concentrati acido nitrico. Il risultato finale della reazione è il composto di azoto:
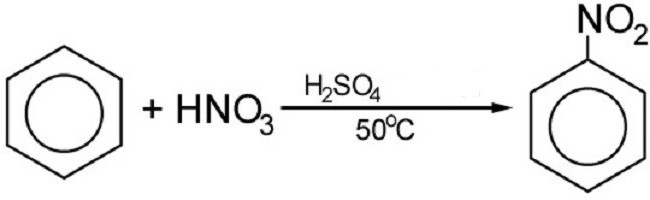
Usando nitrurazione, si ottiene un esplosivo noto a tutti: trotile o trinitotoluene. Pochi sanno che il benzene è la base di Tola. Molti altri composti nitro basati sull'anello benzenico possono anche essere usati come esplosivi.
Formula elettronica del benzene
La formula standard dell'anello benzenico non riflette accuratamente la struttura interna del benzene. Secondo questo, il benzene deve avere tre legami p localizzati, ognuno dei quali deve interagire con due atomi di carbonio. Ma, come dimostra l'esperienza, il benzene non ha i soliti doppi legami. La formula molecolare del benzene consente di vedere che tutti i legami nell'anello benzenico sono equivalenti. Ciascuno di essi ha una lunghezza di circa 0,140 nm, che è un valore intermedio tra la lunghezza di un legame semplice standard (0,154 nm) e un doppio legame etilenico (0,134 nm). La formula strutturale del benzene, raffigurata con legami alternati, è imperfetta. Un modello tridimensionale più credibile di benzene, che appare come mostrato nella foto qui sotto. 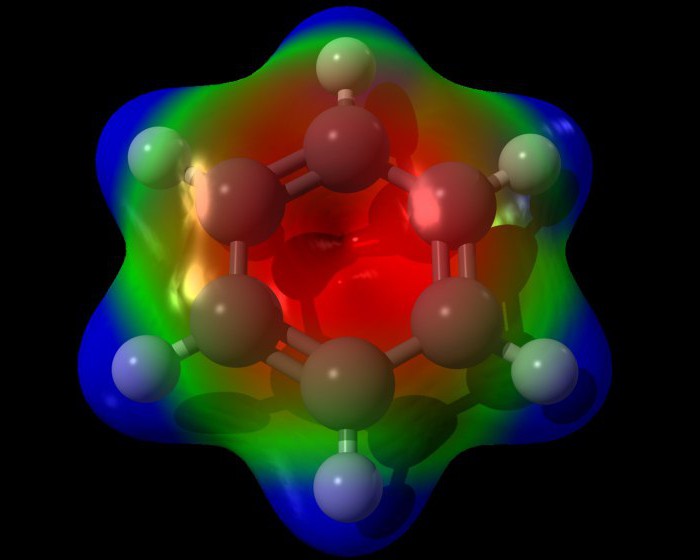 Ciascuno degli atomi dell'anello benzenico è nello stato di ibridizzazione sp 2 . Spende la formazione di sigma bond su tre elettroni di valenza. Questi elettroni comprendono due atomi di carboidrati adiacenti e un atomo di idrogeno. In questo caso, sia gli elettroni che i legami C - C, H - H si trovano sullo stesso piano.
Ciascuno degli atomi dell'anello benzenico è nello stato di ibridizzazione sp 2 . Spende la formazione di sigma bond su tre elettroni di valenza. Questi elettroni comprendono due atomi di carboidrati adiacenti e un atomo di idrogeno. In questo caso, sia gli elettroni che i legami C - C, H - H si trovano sullo stesso piano.
Il quarto elettrone di valenza forma una nuvola nella forma di una figura volumetrica otto, situata perpendicolare al piano dell'anello benzenico. Ciascuna simile nuvola di elettroni si sovrappone al di sopra del piano dell'anello di benzene e direttamente sotto di essa con le nubi di due atomi di carbonio adiacenti.
Ad
La densità delle nubi di p-elettroni di questa sostanza è uniformemente distribuita tra tutti i legami di carbonio. In questo modo si forma una singola nuvola di elettroni anulari. In chimica generale, questa struttura è chiamata sestetto elettronico aromatico.
Valore uguale dei legami interni del benzene
È proprio l'equivalenza di tutte le facce dell'esagono che spiega l'uniformità dei legami aromatici, che provocano le caratteristiche chimiche e fisiche tipiche del benzene. Di seguito viene mostrata la formula per la distribuzione uniforme della nuvola di p-elettroni e l'equivalenza di tutte le sue connessioni interne.
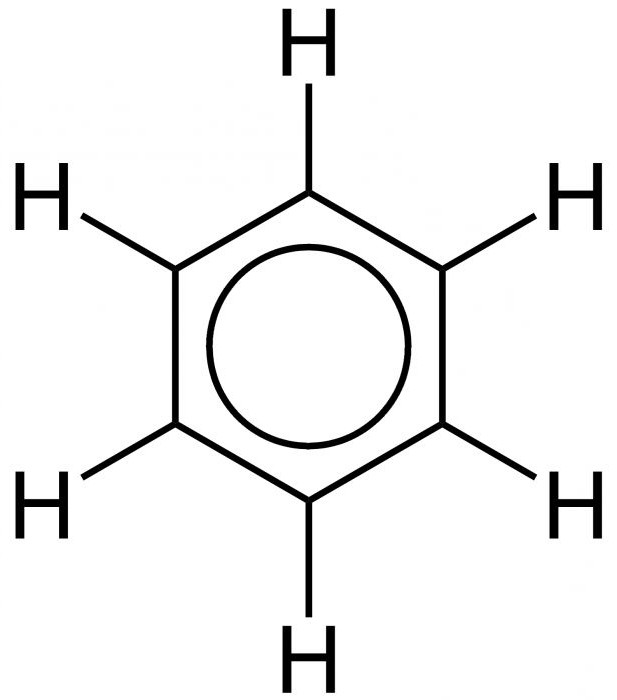
Come si può vedere, invece di alternare funzioni singole e doppie, la struttura interna è rappresentata come un cerchio.
L'essenza della struttura interna del benzene fornisce la chiave per comprendere la struttura interna degli idrocarburi ciclici e amplia le possibilità di applicazione pratica di queste sostanze.