Anidride carbonica: formula, proprietà e applicazioni
Anidride carbonica (anidride carbonica) - un composto che si verifica frequentemente. È formato dall'ossidazione di vari materia organica. I processi più comuni di formazione di questo composto sono il decadimento di resti di animali e piante, la combustione di vari tipi di combustibile, la respirazione di animali e piante. Ad esempio, una persona rilascia circa un chilogrammo di biossido di carbonio al giorno nell'atmosfera. Ossido e anidride carbonica possono anche essere formati in natura inanimata. L'anidride carbonica viene emessa durante l'attività vulcanica e può anche essere estratta da fonti di acqua minerale. L'anidride carbonica si trova in piccole quantità nell'atmosfera della terra. 
Le caratteristiche della struttura chimica di questo composto gli consentono di partecipare a una varietà di reazioni chimiche, la cui base è l'anidride carbonica.
formula
Nel composto di questa sostanza, l'atomo di carbonio tetravalente forma un legame lineare con due molecole di ossigeno. L'aspetto di una tale molecola può essere rappresentato come segue: 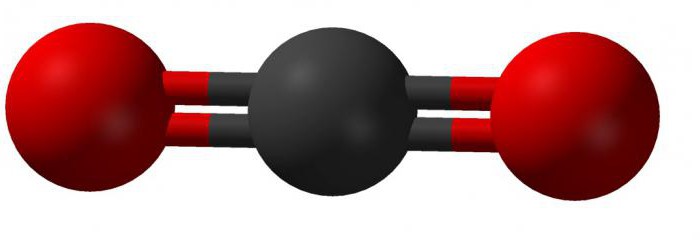
La teoria dell'ibridazione spiega la struttura della molecola di anidride carbonica nel modo seguente: due legami sigma esistenti sono formati tra orbitali di atomi di carbonio e due orbitali di ossigeno 2p; Gli orbitali di carbonio che non partecipano all'ibridazione sono accoppiati con analoghi orbitali di ossigeno. Nelle reazioni chimiche, il biossido di carbonio è scritto nella forma: CO 2.
Ad
Proprietà fisiche
In condizioni normali, il biossido di carbonio è un gas incolore e inodore. È più pesante dell'aria, quindi anidride carbonica e può comportarsi come un liquido. Ad esempio, può essere versato da un contenitore all'altro. Questa sostanza è leggermente solubile in acqua - circa 0,88 l di CO 2 si scioglie in un litro di acqua a 20 ° C. Una leggera diminuzione della temperatura modifica drasticamente la situazione: 1,7 litri di CO2 possono dissolversi nello stesso litro d'acqua a 17 ° C. Con forte raffreddamento, questa sostanza precipita sotto forma di fiocchi di neve - si forma il cosiddetto "ghiaccio secco". Questo nome deriva dal fatto che sotto pressione normale la sostanza, bypassando la fase liquida, si trasforma immediatamente in un gas. L'anidride carbonica liquida si forma ad una pressione leggermente superiore a 0,6 MPa ea temperatura ambiente. 
Proprietà chimiche
Quando interagisce con forti agenti ossidanti, il diossido di carbonio 4 mostra proprietà ossidanti. La reazione tipica di questa interazione è:
C + CO 2 = 2CO.
Quindi, con l'aiuto del carbone, il biossido di carbonio viene ridotto alla sua modificazione bivalente - monossido di carbonio.
In condizioni normali, il biossido di carbonio è inerte. Ma alcuni metalli attivi possono bruciarvi, rimuovendo l'ossigeno dal composto e rilasciando gas di carbonio. Reazione tipica: magnesio bruciante:
Ad
2Mg + CO 2 = 2MgO + C.
Nel corso della reazione si formano ossido di magnesio e carbonio libero. 
Nei composti chimici, la CO 2 presenta spesso le proprietà di un tipico ossido di acido. Ad esempio, reagisce con basi e ossidi di base. Il risultato della reazione sono sali dell'acido carbonico.
Ad esempio, la reazione del composto di ossido di sodio con anidride carbonica può essere rappresentata come segue:
Na 2 O + CO 2 = Na 2 CO 3 ;
2NaOH + CO 2 = Na 2 CO 3 + H 2 O;
NaOH + CO 2 = NaHCO 3 .
Acido carbonico e soluzione di CO 2
Il biossido di carbonio nell'acqua forma una soluzione con un piccolo grado di dissociazione. Questa soluzione di anidride carbonica è chiamata acido carbonico. È incolore, delicato e ha un sapore aspro.
Registrare la reazione chimica:
CO 2 + H 2 O ↔ H 2 CO 3.
L'equilibrio è praticamente spostato a sinistra - solo circa l'1% del biossido di carbonio iniziale si trasforma in acido carbonico. Maggiore è la temperatura, minore è la soluzione delle molecole di acido carbonico. Quando il composto bolle, scompare completamente e la soluzione si disintegra in anidride carbonica e acqua. La formula strutturale dell'acido carbonico è presentata di seguito. 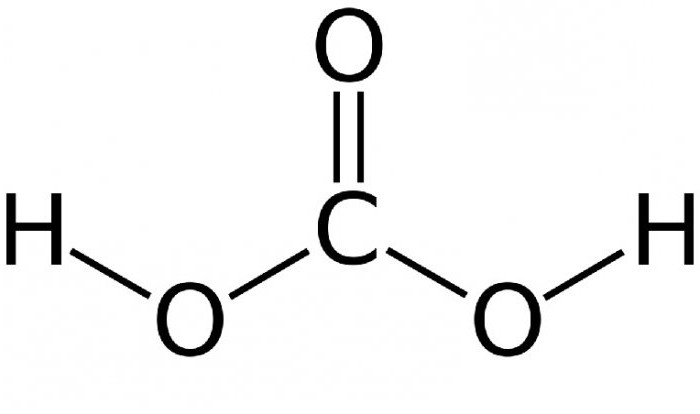
Proprietà dell'acido carbonico
L'acido carbonico è molto debole. Nelle soluzioni, si decompone in ioni idrogeno H + e composti HCO 3 - . In quantità molto piccole formano CO 3 - ioni.
L'acido carbonico è dibasico, quindi i sali formati da esso possono essere medi ed acidi. I sali intermedi della tradizione chimica russa sono chiamati carbonati e i sali forti sono chiamati idrocarbonati.
Ad
Reazione qualitativa
Uno dei possibili modi per rilevare il biossido di carbonio è cambiare la trasparenza della soluzione calcarea.
Ca (OH) 2 + CO 2 = CaCO 3 ↓ + H 2 O.
Questa esperienza è conosciuta dal corso di chimica scolastica. All'inizio della reazione si forma una piccola quantità di precipitato bianco, che successivamente scompare quando l'anidride carbonica viene fatta passare attraverso l'acqua. Il cambiamento di trasparenza si verifica perché nel processo di interazione del composto insolubile - il carbonato di calcio viene convertito in una sostanza solubile - bicarbonato di calcio. La reazione procede lungo il seguente percorso:
CaCO 3 + H 2 O + CO 2 = Ca (HCO 3 ) 2 .
Produzione di anidride carbonica
Se vuoi ottenere una piccola quantità di CO2, puoi iniziare la reazione acido cloridrico con carbonato di calcio (Marmo). Il record chimico di questa interazione è simile a questo:
Ad
CaCO 3 + HCl = CaCl 2 + H 2 O + CO 2 .
Anche con questo scopo usa la reazione di combustione di sostanze contenenti il carbone, come acetilene:
CH 4 + 2 O 2 → 2 H 2 O + CO 2 .
Per la raccolta e la conservazione della sostanza gassosa risultante utilizzando l'apparato Kipp.
Per le esigenze dell'industria e dell'agricoltura, la scala della produzione di biossido di carbonio deve essere ampia. Un metodo popolare di questa reazione su larga scala è la combustione del calcare, che provoca la produzione di anidride carbonica. La formula di reazione è mostrata di seguito:
CaCO 3 = CaO + CO 2 ↑.
Applicazione di anidride carbonica
L'industria alimentare dopo una produzione su larga scala di "ghiaccio secco" è passata a un metodo fondamentalmente nuovo di stoccaggio dei prodotti. È indispensabile nella produzione di bevande gassate e acqua minerale. Il contenuto di CO 2 nelle bevande dà loro freschezza e aumenta significativamente la durata di conservazione. Una carbidazione di acqua minerale consente di evitare la stoltezza e il sapore sgradevole. 
In cucina si usa spesso l'aceto dell'acido citrico. L'anidride carbonica rilasciata allo stesso tempo conferisce sfarzo e leggerezza alla pasticceria.
Questo composto è spesso usato come additivo alimentare che aumenta la durata di conservazione dei prodotti alimentari. Secondo gli standard internazionali per la classificazione del contenuto di additivi chimici nei prodotti, passa sotto il codice E 290,
Ad
L'anidride carbonica in polvere è una delle sostanze più popolari che costituiscono miscele antincendio. Questa sostanza si trova negli estintori a schiuma.
È meglio trasportare e conservare l'anidride carbonica nei cilindri metallici. A temperature superiori a 31 ° C, la pressione nel cilindro può raggiungere uno stato critico e la CO 2 liquida entrerà in uno stato supercritico con un brusco aumento della pressione di lavoro a 7,35 MPa. Un contenitore metallico può sopportare una pressione interna fino a 22 MPa, quindi il campo di pressione a temperature superiori ai trenta gradi è considerato sicuro.