La reazione di Lebedev: formula, meccanismo di reazione. Produzione di butadiene
La reazione di Sergey Vasilyevich Lebedev divenne il punto di partenza nella ricerca di metodi per la produzione di idrocarburi insaturi diene, che sono ancora ben utilizzati nella creazione di gomme sintetiche. Questa scoperta ha permesso di utilizzare un metodo relativamente economico ed economico per la sintesi di gomma artificiale per scopi militari e tecnici, che ha garantito il rilascio di una sostituzione di gomme naturali di alta qualità e duratura in epoca sovietica.

Principio di reazione
Secondo il principio del flusso, questa sintesi è attribuita alla pirolisi catalitica (decomposizione termica), che avviene in presenza di catalizzatori di allumina-ossido di zinco ad una temperatura di circa 450 ° C.
In chimica, la reazione di Lebedev è notevole in quanto avviene in una fase, ma al suo interno ci sono tre cambiamenti contemporaneamente:
- l'acqua si divide;
- l'idrogeno si interrompe;
- l'unione avviene tra i residui alchilici.
La sintesi è stata ripetutamente migliorata, nuovi catalizzatori di alluminio sono stati utilizzati con l'aggiunta di sali di manganese e altri metalli e le condizioni sono state variate, che ha permesso di ridurre il consumo di energia mantenendo la temperatura (360-370 ° C) e aumentando il grado di conversione alcolica durante la reazione (fino al 50%, resa butadiene - 1,3 è 42%).

Reagenti e prodotti
Nei primi studi, S. V. Lebedev ricorse alla creazione di butadiene da frazioni di petrolio. Tuttavia, ha successivamente iniziato ad ottenere questo diene da alcool etilico ottenuto dalla fermentazione di patate. Per ottenere un solo pneumatico, era necessario trattare fino a 500 kg di patate, il che, naturalmente, era economicamente non redditizio.
Più tardi, nel periodo 1926-928, S.V. Lebedev, insieme al suo team di studenti e ascoltatori liberi, ha migliorato il metodo per ottenere il butadiene dall'alcol etilico. L'output del diene al momento della dimostrazione è stato del 22%. Grazie agli sforzi, gli scienziati hanno vinto un concorso organizzato da I.V. Stalin tra gli ex paesi dell'Unione Sovietica, sulle proposte di metodi per la produzione di gomma sintetica.
Ad
Quindi, ora nella versione finale della sintesi, il butadiene - 1,3 CH 2 = CH - CH = CH 2 , l'acqua H 2 O e l'idrogeno libero H 2 si ottengono nei prodotti principali. Inoltre, possono formarsi alcuni composti aromatici, etilene, propilene, butileni, alcoli superiori e acetaldeide, ma le formule di queste sostanze non sono specificate nell'equazione di base della reazione di Lebedev. Poiché questo diene è una sostanza gassosa, insolubile in acqua, è separato da tutti gli altri idrocarburi per condensazione, adsorbimento con alcol, lavaggio con H 2 O o rettificazione.
Meccanismo di reazione
Nella sintesi durante la scissione (decomposizione) di 2 molecole di alcol etilico, grazie ai catalizzatori disidratante-disidratanti, 2 molecole d'acqua e 1 molecola di gas idrogeno vengono staccate da esse. Secondo il meccanismo della reazione di Lebedev, i residui di alchile si uniscono tra loro formando due doppi legami coniugati insaturi nelle posizioni 1,3 (esempio 1).
Ad
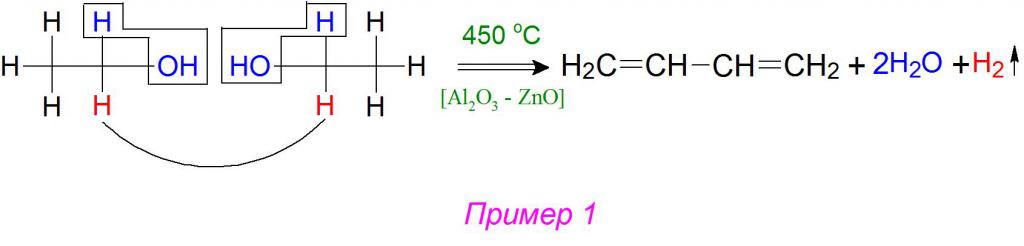
Utilizzare nell'industria
Dopo una vittoria trionfante in una competizione internazionale, lo scienziato ha avuto l'opportunità di realizzare la produzione di gomma sintetica su scala industriale. Poiché la ricezione del butadiene dalla reazione di Lebedev era riconosciuta come molto preziosa, fu finanziata e nel 1930 fu costruito a Leningrado l'impianto sperimentale Liter B, che fino al 1990 occupava il primo posto al mondo nella produzione di gomma artificiale. Sulla base di questa impresa, è stato successivamente istituito l'istituto di ricerca scientifica di gomma sintetica, che continua a studiare composti polimerici.

Ulteriori studi
Le scoperte di S. V. Lebedev servirono come l'inizio dello studio delle proprietà degli idrocarburi dienici, grazie ai quali fu scoperta la cosiddetta "sintesi di diene". Ci sono tre versioni in cui ha studiato la reazione di dimerizzazione di dieni nel corso del suo lavoro scientifico. Il primo assume che come risultato della sintesi, lo scienziato abbia ottenuto il dimero ciclopentadiene. La seconda versione parla della dimerizzazione dell'isoprene per dare il dipentene. E il terzo descrive la preparazione del vinilcicloesene da due molecole di butadiene - 1.3. In ogni caso, questa sintesi ha costituito la base per ulteriori studi sulle proprietà dei dieni coniugati, che sono stati sviluppati da Otto Diels e Kurt Adler, che nel 1950 hanno ricevuto il Premio Nobel.
Sintesi diene
La reazione di Diels-Adler ci ha permesso di ottenere composti ciclici con meccanismi abbastanza semplici, senza ricorrere a complesse reazioni multistadio. L'essenza della reazione è l'interazione di un diene e dienofilo coniugato, che può essere rappresentato da alcheni e alchini con sostituenti elettroacceptor, nonché composti contenenti doppi legami con un eteroatomo, ad esempio -C = O, -C = N, ecc. Come risultato, si forma un idrocarburo ciclico, pertanto, questa reazione è anche chiamata "cicloaddizione".
Ad
La sintesi di diels-adler può avvenire in presenza di acidi di Lewis, che accelerano significativamente il decorso della reazione e più spesso contribuiscono a una buona resa del prodotto principale, oltre a influenzare la formazione di enantiomeri e isomerismo cis / trans.
Un esempio di tale reazione senza catalizzatore è l'aggiunta di butadiene - 1,3 a para-benzochinone in benzene ad una temperatura di 35 ° C, in conseguenza del quale la resa del prodotto raggiunge il 100%. La sintesi procede con il trasferimento di protoni di idrogeno tra gli atomi di carbonio per formare un secondo ciclo e creare un composto forte. Alla fine della reazione, si forma un derivato 1,4-naftochinone, che può reagire ulteriormente con butadiene - 1,3 a 100 ° С con la formazione di un ciclo sul lato opposto. L'antrachinone può essere ottenuto dal prodotto finale di reazione per deidrogenazione, i cui derivati sono usati come coloranti, ad esempio alizarina.
Ad
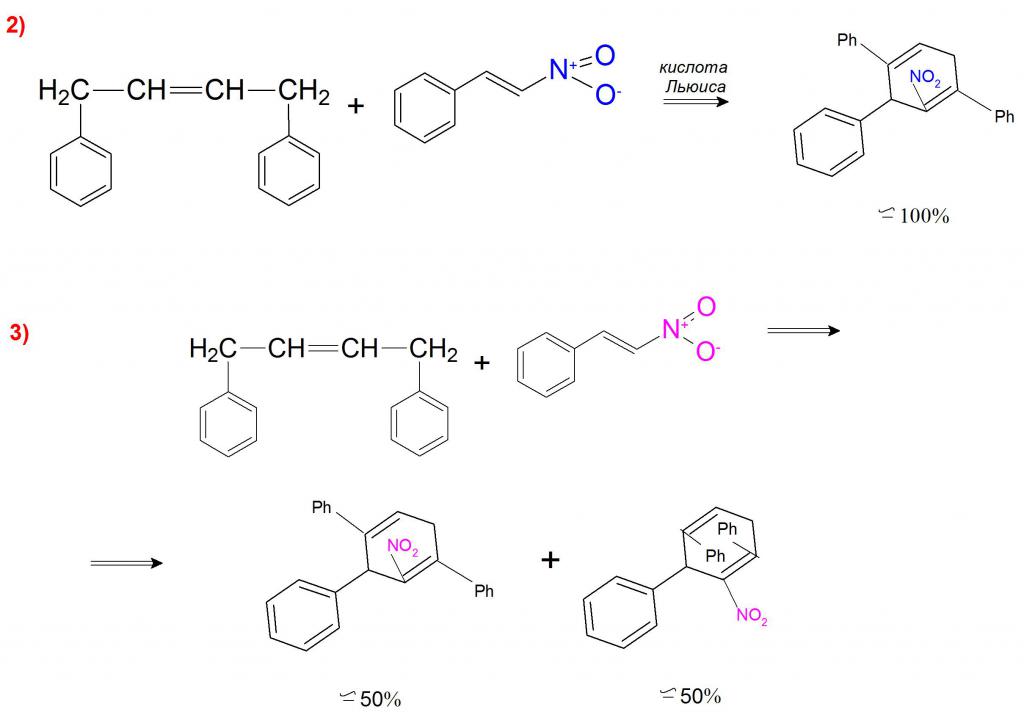
Un esempio di sintesi catalitica può essere la reazione dell'1,4-difenilbutadiene con β-nitrostirene, dove in presenza di un acido di Lewis si forma solo l'addotto endo-nitro (esempio 2). Senza la partecipazione del catalizzatore, questa reazione avviene con la formazione di composti endo nitro e prodotti endo-difenile in un rapporto 1: 1 (Esempio 3).
Tali reazioni confermano l'opportunità dell'uso di sostanze cataliticamente attive nella sintesi di diene, poiché accelerano significativamente il processo e influenzano in modo significativo le regio- (orto-, para- e meta-posizioni) e la stereoselettività (posizioni ottiche e endo- / eso-di-sostituenti).