Principio di Pauli in fisica e chimica: caratteristiche dell'applicazione
La storia della fisica atomica ha molti alti e bassi. Ma grazie al progresso tecnico, qualsiasi ipotesi sorto nelle menti dei teorici potrebbe essere testata in laboratorio. Poiché molti aspetti del comportamento delle particelle elementari non sono ancora suscettibili alle leggi della logica, gli scienziati-scopritori del micromondo hanno accettato di accettarli "così come sono", senza spiegare le ragioni. Il principio di Pauli si riferisce ai risultati di quegli esperimenti che non hanno ancora trovato la loro unica spiegazione.
Contraddizioni nella teoria atomica
Uno dei malintesi più comuni nella fisica atomica era il modello atomico planetario proposto dallo scienziato inglese. Ernest Rutherford. Alla fine, si è rivelato non del tutto affidabile, ma ha permesso di trarre tante giuste conclusioni che i suoi benefici erano indiscutibili. 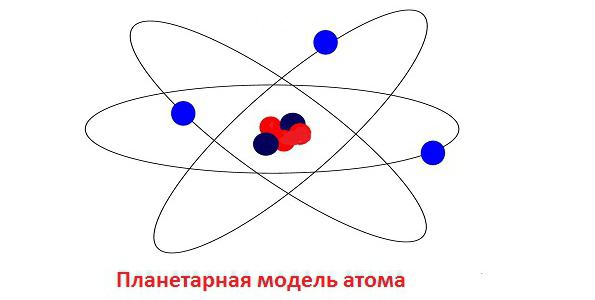 Una delle principali contraddizioni dell'atomo di Rutherford era l'abilità degli elettroni nelle radiazioni. Come risultato della perdita di energia, qualsiasi elettrone alla fine ha dovuto interrompere il suo movimento e cadere nel nucleo. Ma ogni atomo (eccetto uno radioattivo) è intrinsecamente stabile, può esistere per un tempo arbitrariamente lungo e non mostra alcun segno di autodistruzione. Per risolvere questo problema, ci è voluto il talento del geniale fisico danese Niels Bohr.
Una delle principali contraddizioni dell'atomo di Rutherford era l'abilità degli elettroni nelle radiazioni. Come risultato della perdita di energia, qualsiasi elettrone alla fine ha dovuto interrompere il suo movimento e cadere nel nucleo. Ma ogni atomo (eccetto uno radioattivo) è intrinsecamente stabile, può esistere per un tempo arbitrariamente lungo e non mostra alcun segno di autodistruzione. Per risolvere questo problema, ci è voluto il talento del geniale fisico danese Niels Bohr.
Teoria di Bohr
Nel 1913, un giovane fisico sconosciuto dalla Danimarca propose di includere due cambiamenti nella fisica classica, con i quali era possibile spiegare i fatti delle osservazioni e fare molte utili scoperte. Bohr non ha potuto spiegare la causa del comportamento degli elettroni in orbita, quindi il principio di "come è" è stato posto alla base delle sue regole. Queste regole servirono in seguito a un buon servizio e aprirono la strada a nuove scoperte.
Ad
Regole di Bohr

La prima regola era quella modello planetario dell'atomo, proposto da Rutherford è ancora vero. Ma gli elettroni in esso si muovono nelle loro orbite senza radiazioni. La seconda regola di Bohr afferma che il movimento degli elettroni è possibile solo lungo determinate orbite "permesse". Per un elettrone che fa il suo movimento lungo un'orbita permessa, il prodotto dell'impulso e del raggio di questa orbita è sempre un multiplo della costante di Planck. Pertanto, le orbite degli elettroni possono essere localizzate solo su quelle livelli di energia per il quale vale la seguente regola:
(momento elastico * circonferenza dell'orbita) = n * h,
dove h è una tavola costante, e n è un numero naturale. Quindi, con la più piccola orbita consentita, n = 1. La terza regola dice che gli elettroni degli atomi possono essere mossi (ad esempio, bombardandoli con particelle pesanti) in un'orbita esterna libera. Dopo questo, l'elettrone è in grado di tornare a un'orbita interna libera. In questo caso, l'atomo emette un eccesso di energia sotto forma di un quanto di luce.
Ad
Limiti quantici
La regola quantistica di Bohr presuppone che gli elettroni più vicini al nucleo abbiano la più piccola orbita consentita. A questo livello, l'elettrone ha un'energia minima. Ci si aspetterebbe che tutti gli elettroni di un atomo debbano occupare questa orbita e rimanere a questo livello. Tuttavia, questo non succede. Il principio di Pauli ha aiutato a spiegare questa contraddizione.
Wolfgang Pauli
Questo famoso fisico austriaco nacque a Vienna nel 1869. All'università di Monaco, ha ricevuto un'eccellente istruzione completa, ma ha dedicato tutti i suoi lavori scientifici alla fisica quantistica. All'età di vent'anni, Pauli scrisse un articolo di revisione per l'Enciclopedia fisica, molte pagine di cui sono ancora rilevanti oggi. I suoi lavori scientifici furono pubblicati raramente, i suoi pensieri più importanti e le sue ipotesi furono espresse in corrispondenza con i suoi colleghi scientifici. La corrispondenza più vivace fu condotta con N. Bohr e V. Heisenberg. È stato il lavoro congiunto di questi tre scienziati che ha posto le basi per i fondamenti della moderna fisica quantistica. Basandosi sui dati sperimentali di questi tre eminenti scienziati, Pauli ha formato il suo principio. Per lui nel 1945, lo scienziato austriaco ha ricevuto il premio Nobel.
Ad
Movimento di elettroni
Indagando il moto di un elettrone, V. Pauli ha incontrato molti strani momenti nel comportamento di questa particella elementare. Ad esempio, gli elettroni, quando si muovono, si comportano come se ruotassero attorno al loro asse. Il giusto momento di rotazione di un elettrone è chiamato spin. In un punto in orbita si possono inserire due elettroni e i loro spin dovrebbero essere opposti. a vicenda come afferma il principio di Pauli. La fisica di questa restrizione è valida non solo per gli elettroni, ma anche per altre particelle con un valore di spin semi-intero.
Sistema periodico e principio di Pauli
La chimica ha usato il principio di incertezza per spiegare la struttura interna delle sostanze. Ora diventa abbastanza comprensibile perché ci sono solo due elementi nella prima riga della tavola periodica. Sia l'idrogeno che l'elio hanno a loro disposizione una singola orbita inferiore, in cui vi è un solo doppio punto per gli elettroni con spin opposti. L'orbita successiva contiene otto di questi posti. Pertanto, la seconda fila del sistema periodico è stata in grado di prendere otto elementi. Questo modello si estende a tutte le serie del sistema periodico. 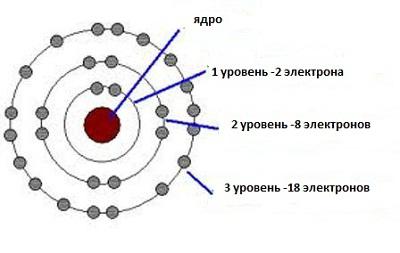
Fisica delle stelle
Stranamente, le leggi del comportamento delle particelle elementari si estendono ben oltre il micromondo. Ad esempio, la fisica stellare si occupa del mondo interiore delle stelle che invecchiano. Il principio di Pauli funziona qui, solo che è compreso in modo un po 'diverso. Ora questa regola dice che in un certo volume spaziale c'è l'opportunità di sistemare solo due particelle elementari con spin opposti. Soprattutto chiaramente questa legge è valida quando si osservano le stelle che invecchiano. Come sai, dopo l'esplosione, la stella della supernova collassa rapidamente, ma non tutte le stelle si trasformano in buchi neri. Con un aumento della soglia di densità limite (e per una stella che invecchia, questo valore è dell'ordine di 10 7 kg / m 3 ), la pressione interna del corpo cosmico aumenta rapidamente. Questo processo ha un termine scientifico speciale: la pressione di un gas degenerato di elettroni. Così, la stella smette di perdere il suo volume e si trasforma in un piccolo corpo celeste delle dimensioni della nostra Terra. Tali stelle in astrofisica sono chiamate nane bianche.
Ad
risultati
Il principio di incertezza è una delle prime leggi del nuovo tipo, che differisce da tutte le idee sul mondo intorno a cui conosciamo. Le nuove leggi sono fondamentalmente diverse dalle regole della fisica classica a noi note fin dall'infanzia. Se le vecchie regole parlano di cosa può accadere quando vengono intraprese determinate azioni, allora le leggi di un nuovo tipo indicano che qualcosa non dovrebbe accadere.

Gli algoritmi per risolvere molti problemi dovrebbero essere basati sul principio di Pauli leggermente modificato. Togliendo all'inizio soluzioni impossibili ai problemi, c'è la possibilità di trovare l'unica risposta corretta. L'uso pratico del principio di incertezza riduce significativamente il tempo richiesto per l'elaborazione informatica delle informazioni. Precedentemente noto solo nella cerchia dei fisici teorici, il principio di Pauli è andato oltre i limiti della fisica quantistica, denotando così nuovi metodi per studiare le leggi della natura.