Modello planetario dell'atomo: l'esperienza di Rutherford
Il modello planetario dell'atomo fu proposto da E. Rutherford nel 1910. I primi studi sulla struttura dell'atomo furono fatti con l'aiuto di particelle alfa. Sulla base dei risultati ottenuti negli esperimenti sulla loro dispersione, Rutherford suggerì che l'intera carica positiva di un atomo fosse concentrata in un piccolo nucleo nel suo centro. D'altra parte, gli elettroni caricati negativamente sono distribuiti all'interno del resto del suo volume.
Un po 'di background
La prima brillante congettura sull'esistenza degli atomi è stata fatta dall'antico scienziato greco Democrito. Da allora, l'idea dell'esistenza degli atomi, le cui combinazioni danno tutte le sostanze intorno a noi, non ha lasciato l'immaginazione della gente della scienza. Di tanto in tanto veniva indirizzato dai suoi vari rappresentanti, ma fino all'inizio del XIX secolo, le loro costruzioni erano solo ipotesi non supportate da dati sperimentali.
Ad
Infine, nel 1804, più di cento anni prima che il modello planetario dell'atomo apparisse, lo scienziato inglese John Dalton presentò prove della sua esistenza e introdusse il concetto di peso atomico, che fu la sua prima caratteristica quantitativa. Come i suoi predecessori, rappresentava gli atomi nelle parti più piccole della materia, come palle solide che non potevano essere divise in particelle ancora più piccole.
Scoperta di elettroni e il primo modello dell'atomo
Passò quasi un secolo quando, finalmente, alla fine del XIX secolo, l'inglese JJ Thomson scoprì anche la prima particella subatomica, un elettrone caricato negativamente. Poiché gli atomi sono elettricamente neutri, Thomson pensò che dovevano consistere in un nucleo con carica positiva con elettroni sparsi per tutto il suo volume. Sulla base di vari risultati ottenuti sperimentalmente, nel 1898 propose il proprio modello dell'atomo, a volte chiamato "prugne nel budino", perché l'atomo in esso era rappresentato come una sfera piena di un liquido caricato positivamente in cui gli elettroni erano incorporati come "prugne" nel budino. " Il raggio di un tale modello sferico era di circa 10 -8 cm. La carica positiva totale del liquido è simmetricamente e uniformemente bilanciata da negativo cariche di elettroni, come mostrato nella foto qui sotto. 
Questo modello ha spiegato in modo soddisfacente il fatto che quando una sostanza viene riscaldata, inizia a emettere luce. Sebbene questo fosse il primo tentativo di capire che cosa sia un atomo, non poteva soddisfare i risultati di esperimenti eseguiti successivamente da Rutherford e altri. Thomson nel 1911 fu d'accordo sul fatto che il suo modello semplicemente non poteva rispondere come e perché la dispersione di raggi α osservata negli esperimenti avvenisse. Pertanto, fu abbandonato e sostituito da un modello planetario più perfetto dell'atomo.
Ad
Come è l'atomo lo stesso?
Ernest Rutherford spiegò il fenomeno della radioattività, che gli portò il premio Nobel, ma il suo contributo più significativo alla scienza fu fatto più tardi quando scoprì che un atomo è costituito da un nucleo denso circondato da orbite di elettroni, proprio come il Sole è circondato da orbite di pianeti. 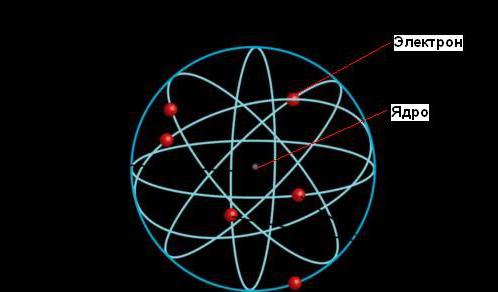
Secondo il modello planetario dell'atomo, la maggior parte della sua massa è concentrata in un nucleo minuscolo (rispetto alle dimensioni dell'intero atomo). Gli elettroni si muovono attorno al nucleo, viaggiando ad una velocità incredibile, ma la maggior parte del volume di atomi è uno spazio vuoto.
La dimensione del nucleo è così piccola che il suo diametro è 100.000 volte più piccolo di quello di un atomo. Rutherford stimava il diametro del nucleo di 10 -13 cm, a differenza delle dimensioni di un atomo - 10-8 cm. Al di fuori del nucleo, gli elettroni ruotano attorno ad esso ad alte velocità, determinando forze centrifughe che bilanciano le forze elettrostatiche di attrazione tra protoni ed elettroni.
Ad
Rutherford's Experiences
Il modello planetario dell'atomo nacque nel 1911, dopo il famoso esperimento con lamina d'oro, che ci permise di ottenere alcune informazioni fondamentali sulla sua struttura. Il percorso di Rutherford alla scoperta del nucleo atomico è un buon esempio del ruolo della creatività nella scienza. La sua ricerca iniziò nel 1899, quando scoprì che alcuni elementi emettono particelle caricate positivamente che possono penetrare qualsiasi cosa. Ha chiamato queste particelle alfa (α) particelle (ora sappiamo che erano nuclei di elio). Come tutti i bravi scienziati, Rutherford era curioso. Si chiese se le particelle alfa potessero essere usate per scoprire la struttura di un atomo. Rutherford decise di puntare il fascio di particelle alfa su un foglio di lamina d'oro molto sottile. Ha scelto l'oro perché può essere usato per produrre fogli di soli 0,00004 cm. Per un foglio di lamina d'oro, ha messo uno schermo che brillava quando le particelle alfa lo colpivano. È stato usato per rilevare le particelle alfa dopo aver attraversato il foglio. Una piccola fessura sullo schermo ha permesso al raggio della particella alfa di raggiungere la lamina dopo l'uscita dalla sorgente. Alcuni di loro dovrebbero passare attraverso il foglio e continuare a muoversi nella stessa direzione, l'altra parte dovrebbe rimbalzare sul foglio e essere riflessa ad angoli acuti. Puoi vedere il diagramma dell'esperimento nella figura sottostante. 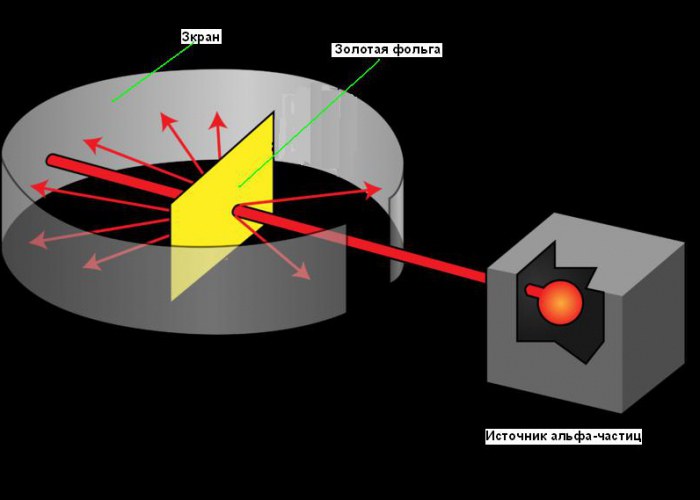
Cosa è successo nell'esperienza di Rutherford?
Basato sul modello dell'atomo JJ Thomson, Rutherford suggerì che le regioni di carica positiva solida che riempivano l'intero volume di atomi d'oro avrebbero deviato o piegato le traiettorie di tutte le particelle alfa mentre passavano attraverso il foglio.
Ad
Tuttavia, la stragrande maggioranza delle particelle alfa passava attraverso la lamina d'oro, come se non esistesse. Sembravano passare attraverso lo spazio vuoto. Solo alcuni di loro deviano dalla retta via, come si supponeva all'inizio. Di seguito è riportato un grafico del numero di particelle sparse nella direzione corrispondente sull'angolo di dispersione. 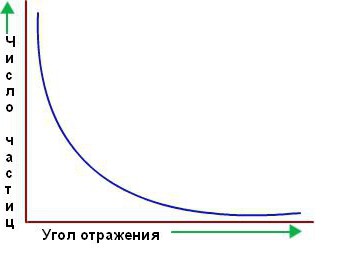
Sorprendentemente, una piccola percentuale di particelle è tornata dalla pellicola mentre il pallone rimbalzava contro lo scudo. Rutherford si rese conto che queste deviazioni erano il risultato di una collisione diretta tra particelle alfa e componenti caricate positivamente di un atomo.
Il nucleo è centrale
Basandosi su una percentuale insignificante di particelle alfa riflesse dalla lamina, si può concludere che l'intera carica positiva e quasi l'intera massa dell'atomo sono concentrate in una piccola area, e il resto dell'atomo è per lo più spazio vuoto. Rutherford ha definito l'area di carica positiva concentrata il nucleo. Ha previsto e presto scoperto che contiene particelle caricate positivamente, che ha chiamato protoni. Rutherford predisse l'esistenza di particelle atomiche neutre chiamate neutroni, ma non riuscì a rilevarle. Tuttavia, il suo studente James Chadwick li scoprì pochi anni dopo. La figura seguente mostra la struttura del nucleo dell'atomo di uranio. 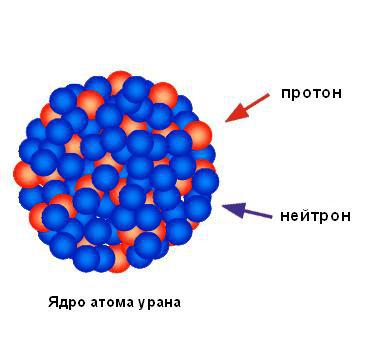
Gli atomi sono costituiti da nuclei pesanti carichi positivamente, circondati da particelle di elettroni estremamente leggere caricate negativamente attorno a loro, e a tali velocità che le forze centrifughe meccaniche semplicemente bilanciano la loro attrazione elettrostatica al nucleo, e in questo contesto è assicurata la stabilità dell'atomo.
Ad
Svantaggi di questo modello
L'idea principale di Rutherford apparteneva all'idea di un nucleo atomico di piccole dimensioni. L'ipotesi delle orbite degli elettroni era pura ipotesi. Non sapeva esattamente dove e come gli elettroni ruotano attorno al nucleo. Pertanto, il modello planetario di Rutherford non spiega la distribuzione di elettroni nelle orbite.
L'idea principale di Rutherford apparteneva all'idea di un nucleo atomico di piccole dimensioni. L'ipotesi delle orbite degli elettroni era pura ipotesi. Non sapeva esattamente dove e come gli elettroni ruotano attorno al nucleo. Pertanto, il modello planetario di Rutherford non spiega la distribuzione di elettroni nelle orbite.
Inoltre, la stabilità dell'atomo di Rutherford era possibile solo con il moto continuo degli elettroni nelle orbite senza perdita di energia cinetica. Ma i calcoli elettrodinamici hanno mostrato che il moto degli elettroni lungo qualsiasi traiettoria curvilinea, accompagnato da un cambiamento nella direzione del vettore di velocità e dall'aspetto di una corrispondente accelerazione, è inevitabilmente accompagnato dall'emissione di energia elettromagnetica. Allo stesso tempo, secondo la legge di conservazione energia, energia cinetica L'elettrone deve essere speso molto rapidamente sulle radiazioni e deve cadere sul nucleo, come mostrato schematicamente nella figura sottostante. 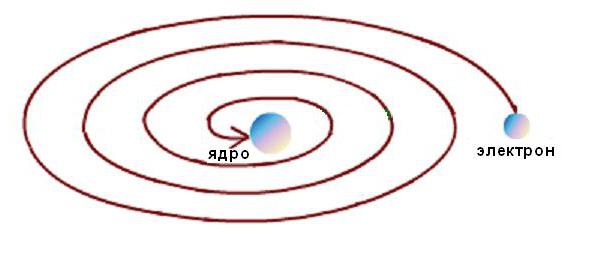 Ma questo non accade, poiché gli atomi sono formazioni stabili. Una tipica contraddizione scientifica sorse tra il modello del fenomeno e i dati sperimentali.
Ma questo non accade, poiché gli atomi sono formazioni stabili. Una tipica contraddizione scientifica sorse tra il modello del fenomeno e i dati sperimentali.
Da Rutherford a Niels Bohr
Il successivo importante passo avanti nella storia atomica avvenne nel 1913, quando lo scienziato danese Niels Bohr pubblicò una descrizione di un modello più dettagliato dell'atomo. Ha definito più chiaramente i luoghi in cui gli elettroni possono essere localizzati. Sebbene in seguito gli scienziati svilupperanno strutture atomiche più raffinate, il modello planetario dell'atomo di Bohr era sostanzialmente corretto, e gran parte di esso è ancora accettato. Aveva molte applicazioni utili, per esempio, con il suo aiuto, spiegavano le proprietà di vari elementi chimici, la natura del loro spettro di radiazioni e la struttura dell'atomo. Il modello planetario e il modello di Bohr furono le pietre miliari più importanti, segnando l'emergere di una nuova direzione in fisica: la fisica del micromondo. Bohr ha ricevuto il premio Nobel per la fisica nel 1922 per il suo contributo alla nostra comprensione della struttura dell'atomo.
Cosa ha portato il nuovo Bohr al modello atomico?
Mentre era ancora un giovane, Bohr lavorava al laboratorio di Rutherford in Inghilterra. Poiché il concetto di elettroni era poco sviluppato nel modello di Rutherford, Bohr si concentrò su di essi. Di conseguenza, il modello planetario dell'atomo fu sostanzialmente raffinato. Bohr postula, che ha formulato nel suo articolo "Sulla struttura degli atomi e delle molecole", pubblicato nel 1913, afferma:
1. Gli elettroni possono muoversi attorno al nucleo solo a distanze fisse da esso, determinati dalla quantità di energia che hanno. Chiamò questi livelli fissi livelli di energia o gusci di elettroni. Bohr li rappresentava sotto forma di sfere concentriche, con un nucleo al centro di ciascuna di esse. In questo caso, gli elettroni con energia inferiore saranno trovati a livelli più bassi, più vicini al nucleo. Coloro che hanno più energia saranno trovati a livelli più alti, più lontano dal nucleo.
2. Se un elettrone assorbe una quantità (piuttosto specifica per un dato livello) di energia, allora salterà al livello di energia successivo più alto. Al contrario, se perde la stessa quantità di energia, ritornerà al livello originale. Tuttavia, un elettrone non può esistere a due livelli di energia.
Questa idea è illustrata con un'immagine. 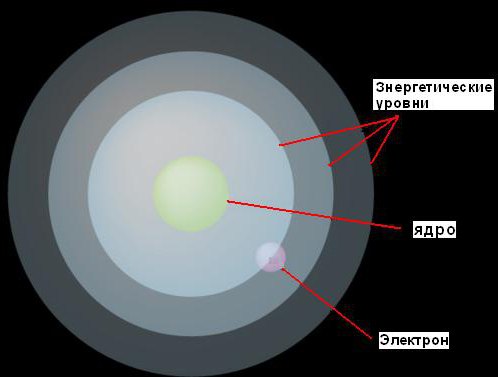
Porzioni di energia per elettroni
Il modello atomico di Bohr è in realtà una combinazione di due idee diverse: il modello atomico di Rutherford con gli elettroni che ruotano attorno al nucleo (in realtà, è il modello planetario dell'atomo di Bohr - Rutherford), e l'idea dello scienziato tedesco Max Planck sulla quantizzazione dell'energia della materia, pubblicata nel 1901. Un quanto (al plurale, quanti) è la quantità minima di energia che può essere assorbita o irradiata da una sostanza. È una sorta di passaggio per il campionamento della quantità di energia.
Se si confronta l'energia con l'acqua e si desidera aggiungerla alla materia sotto forma di un bicchiere, non si può semplicemente versare l'acqua in un flusso continuo. Invece, è possibile aggiungerlo in piccole quantità, ad esempio un cucchiaino. Bohr credeva che se gli elettroni possono assorbire o perdere solo quantità fisse di energia, allora dovrebbero variare la loro energia solo con queste quantità fisse. Quindi, possono solo occupare fisso livelli di energia attorno al nucleo, che corrispondono agli incrementi quantizzati della loro energia.
Pertanto, l'approccio quantistico alla spiegazione di ciò che costituisce una struttura atomica emerge dal modello di Bohr. Il modello planetario e il modello di Bohr erano passaggi peculiari dalla fisica classica alla fisica quantistica, che è lo strumento principale nella fisica del micromondo, inclusa la fisica atomica.