La funzione e la struttura della proteina
Le proteine sono composti organici altamente molecolari. Queste sostanze sono anche chiamate proteine, polipeptidi. Successivamente, considera la struttura e la funzione delle proteine.
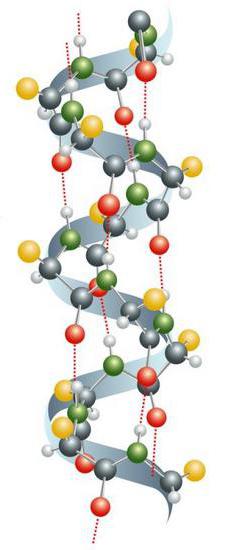
Informazioni generali
La struttura chimica delle proteine è rappresentata da alfa-amminoacidi legati in una catena attraverso un legame peptidico. Negli organismi viventi, la composizione determina il codice genetico. Nel processo di sintesi, nella maggior parte dei casi, vengono utilizzati 20 amminoacidi di tipo standard. Molte delle loro combinazioni formano molecole proteiche con un'ampia varietà di proprietà. I residui di amminoacidi sono spesso soggetti a modifiche post-traduzionali. Possono verificarsi prima che la proteina inizi a svolgere le sue funzioni e nel processo della sua attività nella cellula. Negli organismi viventi, spesso diverse molecole formano complessi complessi. Un esempio di questo è l'associazione fotosintetica.
Ad
Assegnazione di connessione
Le proteine sono considerate un componente importante della nutrizione di esseri umani e animali, poiché nel loro organismo non è possibile sintetizzare tutti gli aminoacidi necessari. Alcuni di loro dovrebbero venire con cibo proteico. Le principali fonti di composti sono carne, noci, latte, pesce, cereali. In misura minore, le proteine sono presenti in verdure, funghi e frutti di bosco. Durante la digestione da parte degli enzimi, le proteine consumate vengono distrutte in aminoacidi. Sono già utilizzati nella biosintesi delle proprie proteine nel corpo o subiscono un ulteriore decadimento - per l'energia.
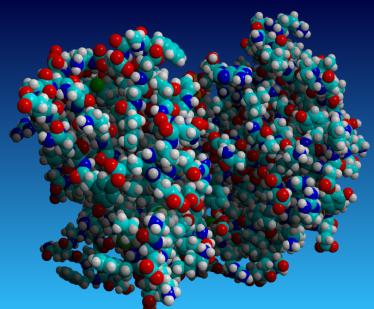
Sfondo storico
La sequenza della struttura della proteina di insulina è stata determinata per la prima volta da Frederius Senger. Per il suo lavoro ha ricevuto il premio Nobel nel 1958. Sanger ha usato il metodo di sequenziamento. Usando la diffrazione radiazione a raggi x successivamente, sono state ottenute strutture tridimensionali di mioglobina ed emoglobina (alla fine degli anni '50). Il lavoro è stato eseguito da John Kendrew e Max Perutz.
Ad
Struttura della molecola proteica
Include polimeri lineari. Essi, a loro volta, sono composti da residui di alfa-amminoacidi, che sono monomeri. Inoltre, la struttura proteica può includere componenti aventi natura non amminoacidica e residui amminoacidici di un tipo modificato. Nella designazione dei componenti utilizzati abbreviazioni a 1 o 3 lettere. Un composto che contiene da due a diverse dozzine di residui viene spesso definito "polipeptide". Come risultato dell'interazione del gruppo alfa-carbossilico di un amminoacido con il gruppo alfa-amminico dell'altro, appaiono i legami (durante la formazione della struttura proteica). Nel composto, le estremità C e N- sono isolate, a seconda del gruppo di residui di amminoacidi liberi: -COOH o -NH 2 . In corso sintesi proteica sul ribosoma come primo terminale, di regola, agisce un residuo di metionina; l'accessione del successivo viene effettuata al C-end dei precedenti.
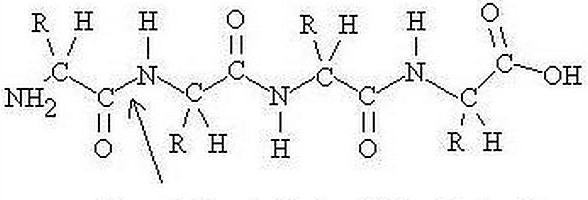
Livelli di organizzazione
Sono stati offerti da Lindrem-Lang. Sebbene questa divisione sia considerata in qualche modo obsoleta, è ancora utilizzata. È stato proposto di distinguere quattro livelli di organizzazione della connessione. La struttura primaria della molecola proteica è determinata dal codice genetico e dalle caratteristiche del gene. Per livelli più alti, la formazione durante il ripiegamento delle proteine è caratteristica. La struttura spaziale della proteina è determinata nell'intera catena di amminoacidi. Tuttavia, è abbastanza labili. Può essere influenzato da fattori esterni. A questo proposito, è più corretto parlare della conformazione del composto, l'energia più benefica e preferibile.
Ad
Livello 1
È rappresentato da una sequenza di residui amminoacidici della catena polipeptidica. Di norma, viene descritto utilizzando le designazioni a una o tre lettere. La struttura primaria delle proteine è caratterizzata da combinazioni stabili di residui di aminoacidi. Eseguono determinati compiti. Tali "motivi conservatori" rimangono preservati nel corso dell'evoluzione delle specie. Secondo loro, molto spesso è possibile prevedere il problema di una proteina sconosciuta. Valutando il grado di somiglianza (omologia) nelle catene di amminoacidi di vari organismi, è possibile determinare la distanza evolutiva formata tra i taxa che compongono questi organismi. La struttura primaria delle proteine è determinata dal sequenziamento o dal complesso iniziale del suo mRNA usando la tabella del codice genetico.
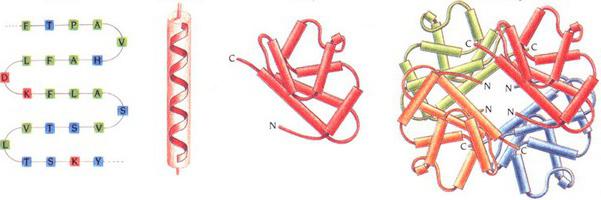
Ordinamento locale della sezione di catena
Questo è il livello successivo di organizzazione: la struttura secondaria delle proteine. Ci sono diversi tipi di esso. L'ordinamento locale di un sito di catena di un polipeptide è stabilizzato da legami a idrogeno. I tipi più popolari sono:
- Alfa elica Sono presentati sotto forma di bobine dense attorno al lungo asse molecolare. Un giro è composto da 3,6 residui di amminoacidi. Il passo dell'elica è 0,54 nm. Questa struttura proteica secondaria è stabilizzata dalle interazioni dei gruppi di peptidi H e O, che sono 4 unità l'una dietro l'altra. L'alfa elica può essere mancina o destrorsa. Tuttavia, quest'ultimo è più spesso rilevato in composti proteici. Interazioni elettrostatiche di arginina, lisina, acido glutammico. Nelle immediate vicinanze, residui di leucina, treonina, serina e asparagina possono causare interferenze steriche con la formazione. La violazione dell'alfa-elica (la sua curva) è causata da parti della prolina.
- Liste beta. Sono presentati sotto forma di diverse catene di polipeptidi a zig-zag. In essi, i legami idrogeno si formano tra amminoacidi, relativamente remoti nella struttura primaria, o diverse catene proteiche. Le connessioni sono generalmente orientate N-estremità nella direzione opposta (orientamento anti-parallelo). Quando si formano liste beta, la piccola dimensione dei gruppi laterali di aminoacidi è importante.
- Frammenti non ordinati.
- 310- e π - elica e altro.

Struttura spaziale
La struttura terziaria delle proteine include elementi del livello precedente. Sono stabilizzati da diversi tipi di interazioni. I legami idrofobici sono della massima importanza. In stabilizzazione sono coinvolti:
- Interazioni covalenti.
- Legami ionici che si formano tra gruppi di aminoacidi laterali che hanno cariche opposte.
- Interazioni di idrogeno.
- Legami idrofobici. Nel processo di interazione con gli elementi H 2 O circostanti, la piegatura della proteina avviene in modo tale che i gruppi di amminoacidi non polari laterali sono isolati dalla soluzione acquosa. I gruppi idrofili (polari) appaiono sulla superficie della molecola.
La struttura terziaria delle proteine è determinata da metodi di risonanza magnetica (nucleare), alcuni tipi di microscopia e altri metodi.
Principio di posa
Gli studi hanno dimostrato che tra 2 e 3 livelli è conveniente allocarne un altro. Si chiama "architettura", "motivo di stile". È determinato dalla posizione relativa dei componenti della struttura secondaria (filamenti beta e alfa eliche) entro i confini del globulo compatto, il dominio delle proteine. Può esistere indipendentemente o essere incluso nella composizione di una proteina più grande insieme ad altre simili. È stabilito che i motivi di stile sono piuttosto conservatori. Si trovano in proteine che non hanno legami né evolutivi né funzionali. La definizione di architettura è alla base della classificazione razionale (fisica).
Ad
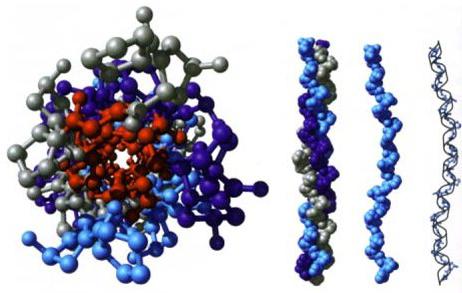
Organizzazione di dominio
Con la disposizione reciproca di diverse catene di polipeptidi all'interno di un singolo complesso proteico, si forma una struttura proteica quaternaria. Gli elementi inclusi nella sua composizione sono formati separatamente sui ribosomi. Solo alla fine della sintesi comincia a formarsi questa struttura proteica. Può contenere sia catene polipeptidiche distinte che identiche. La struttura quaternaria delle proteine è stabilizzata a causa delle stesse interazioni del livello precedente. Alcuni complessi possono includere diverse dozzine di proteine.
Struttura delle proteine: obiettivi difensivi
I polipeptidi del citoscheletro, che agiscono in qualche modo come un'armatura, danno forma a molti organi e partecipano al suo cambiamento. Le proteine strutturali forniscono protezione per il corpo. Ad esempio, questa proteina è il collagene. Costituisce la base della sostanza intercellulare dei tessuti connettivi. La cheratina ha anche una funzione protettiva. Forma la base di corna, piume, capelli e altri derivati dell'epidermide. Quando la proteina lega le tossine in molti casi, si verifica la disintossicazione di quest'ultimo. Questo è il compito della difesa chimica del corpo. Un ruolo particolarmente importante nel processo di neutralizzazione delle tossine nel corpo umano è svolto dagli enzimi epatici. Sono in grado di dividere i veleni o tradurli in forma solubile. Ciò contribuisce a un trasporto più veloce dal corpo. Le proteine presenti nel sangue e altri fluidi biologici forniscono protezione immunitaria, causando una reazione sia ad un attacco di agenti patogeni che a danno. Le immunoglobuline (anticorpi e componenti del sistema del complemento) sono in grado di neutralizzare batteri, proteine estranee e virus.
Ad
Meccanismo di regolazione
Le molecole proteiche che non agiscono come fonte di energia o come materiale da costruzione controllano molti processi intracellulari. Quindi, a causa loro, viene eseguita la regolazione della traduzione, trascrizione, affettamento, attività di altri polipeptidi. Il meccanismo di regolazione si basa sull'attività enzimatica o si manifesta a causa del legame specifico con altre molecole. Ad esempio, fattori di trascrizione, polipeptidi attivatori e proteine repressive sono in grado di controllare l'intensità della trascrizione genica. Allo stesso tempo, interagiscono con sequenze regolatorie di geni. Il ruolo più importante nel controllo del decorso dei processi intracellulari è assegnato alle proteine fosfatasi e alle protein chinasi. Questi enzimi innescano o inibiscono l'attività di altre proteine attraverso l'aggiunta o la scissione di gruppi fosfato da loro.
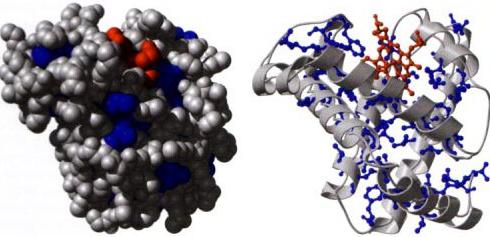
Compito di segnalazione
Spesso è combinato con una funzione normativa. Ciò è dovuto al fatto che molti polipeptidi intracellulari, oltre che extracellulari, possono trasmettere segnali. Fattori di crescita, citochine, ormoni e altri composti hanno questa capacità. Gli steroidi sono trasportati dal sangue. L'interazione ormonale con il recettore agisce come un segnale, a causa del quale viene attivata la risposta della cellula. Gli steroidi controllano il contenuto di composti nel sangue e nelle cellule, nella riproduzione, nella crescita e in altri processi. Un esempio è l'insulina. Regola il livello di glucosio. L'interazione delle cellule viene effettuata mediante la segnalazione di composti proteici trasmessi attraverso la sostanza intercellulare.
Trasporto di elementi
Le proteine solubili coinvolte nel movimento di piccole molecole hanno un'alta affinità per il substrato presente in concentrazioni elevate. Hanno anche la possibilità di rilasciarlo facilmente in aree con il suo basso contenuto. Un esempio è l'emoglobina proteica di trasporto. Sposta l'ossigeno dai polmoni verso altri tessuti e da loro - i trasferimenti anidride carbonica. Alcune proteine di membrana sono anche coinvolte nel trasporto di piccole molecole attraverso le pareti cellulari, cambiandole. Lo strato lipidico citoplasmatico è resistente all'acqua. Ciò impedisce la diffusione di molecole cariche o polari. Le connessioni di trasporto a membrana possono essere suddivise in vettori e canali.
Connessioni ridondanti
Queste proteine formano le cosiddette riserve. Si accumulano, ad esempio, nei semi delle piante, uova animali. Tali proteine fungono da fonte di riserva di materia ed energia. Alcuni composti sono usati dal corpo come un serbatoio di amminoacidi. Essi, a loro volta, sono precursori di sostanze attive coinvolte nella regolazione del metabolismo.
Recettori cellulari
Tali proteine possono essere localizzate direttamente nel citoplasma o incorporate nel muro. Una parte della connessione riceve un segnale. Di norma, di solito è una sostanza chimica e, in alcuni casi, un'azione meccanica (stretching, ad esempio), luce e altri stimoli. Nel processo di esposizione di un segnale a un frammento specifico di una molecola - un recettore polipeptidico - iniziano i suoi cambiamenti conformazionali. Provocano un cambiamento nella conformazione del resto, che trasferisce lo stimolo agli altri componenti della cellula. L'invio di un segnale può essere fatto in diversi modi. Alcuni recettori sono in grado di catalizzare una reazione chimica, mentre i secondi agiscono come canali ionici che si chiudono o si aprono sotto l'influenza di uno stimolo. Alcuni composti legano in modo specifico le molecole di mediazione all'interno della cellula.
Polipeptidi motori
Esiste un'intera classe di proteine che forniscono il movimento del corpo. Le proteine motorie sono coinvolte nella contrazione muscolare, nel movimento cellulare, nell'attività di flagelli e ciglia. A causa di ciò, viene eseguito anche il trasporto direzionale e attivo. Le chinesine e le dineine trasferiscono molecole lungo i microtubuli usando l'ATP come fonte di energia di idrolisi. Quest'ultimo sposta organoidi e altri elementi verso il centrosoma dai siti di cellule periferiche. Le kinesine si stanno muovendo nella direzione opposta. Dyneiny, inoltre, è responsabile per l'attività di flagelli e cilia.