La reazione di Wagner: meccanismo, ruolo nella chimica organica, applicazione
Nonostante il suo nome, la prima reazione di Wagner con alcheni fu effettuata da Markovnikov nel 1878. Ha ottenuto l'alcool, cicloesandolo-1,2, dal cicloesene, agendo su di esso con permanganato di potassio in una soluzione acquosa a 0 ° C. Successivamente, un altro scienziato russo, Wagner, ha sviluppato e studiato questo metodo per ottenere alcoli diidrici. La data della scoperta della reazione è considerata del 1888, quando fu pubblicata la sua monografia "Verso la reazione dell'ossidazione dei composti del carbonio insaturo". Va detto che Wagner ha condotto esperimenti non solo in acque neutre, ma anche in mezzi acidi e alcalini.
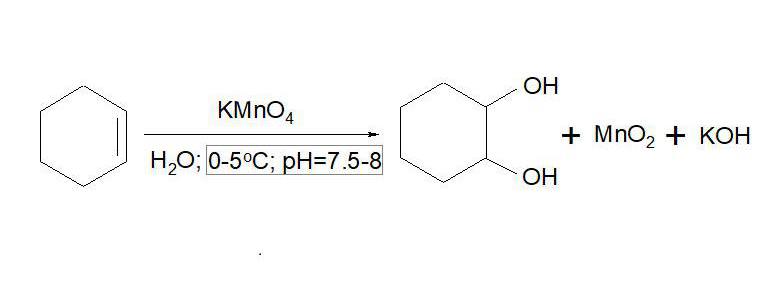
meccanismo
L'essenza della reazione sta nella syn-hydroxylation (aggiunta simultanea di due gruppi idrossile) del doppio legame alchenico. Il reagente è permanganato di potassio è un forte agente ossidante, quindi, per evitare un'ulteriore conversione di un gruppo idrossile in un gruppo carbossilico, è necessario osservare rigorosamente l'acidità: il valore ottimale del parametro pH è 8, cioè, il mezzo deve avere una reazione alcalina debole.
La reazione di Wagner passa attraverso lo stadio di formazione dell'estere ciclico di manganese, che viene quindi immediatamente idrolizzato al diolo diidrico. Il composto intermedio è dovuto al fatto che i gruppi ossidrilici si trovano nella posizione vicinale - a diversi atomi di carbonio. Il composto intermedio stesso, l'intermedio, non è mai stato isolato, ma la sua presenza è confermata dalla ricerca: quando si usa il permanganato con uno ione ossigeno marcato 18O come reagente, si forma un diolo in uscita, nei gruppi ossidrile di cui sono rilevati i 18O desiderati. Di conseguenza, gli atomi di ossigeno passano all'alchene non dall'acqua, dal solvente, ma dal permanganato, l'agente ossidante.
Ad
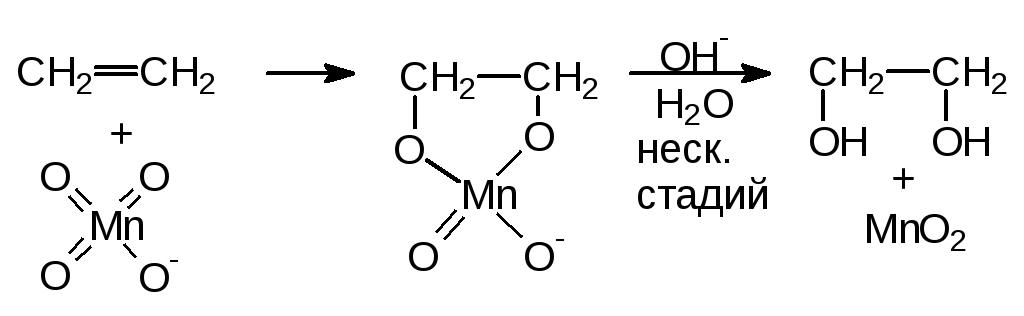
Se l'isomero trans dell'alchene viene introdotto nella reazione di Wagner, i gruppi ossidrile diventano cis-position all'uscita e, nel caso dell'isomero cis dell'alchene, si forma un diolo con gruppi funzionali nella posizione trans. Queste relazioni stereochimiche sono state derivate empiricamente e funzionano anche per le reazioni di aggiunta di altri reagenti su un legame multiplo.
valore
La reazione di ossidazione di Wagner è qualitativa a legame multiplo insieme alla grave ossidazione di idrocarburi insaturi e bromurazione. Durante la reazione, la soluzione di lampone del permanganato di potassio si scolorisce e si forma un precipitato bruno insolubile - ossido di manganese (IV). I prodotti di reazione, alcoli diidrici, sono anche chiamati glicoli. La minore importanza pratica sono i glicoli inferiori basati su etilene, propilene e butilene, nonché composti ad alta molecolare-polimeri basati su di essi, ad esempio, polietilene ossido.
Ad

applicazione
La reazione di Wagner, nonostante i suoi limiti, è ancora ampiamente utilizzata nella sintesi organica. Ciò è dovuto al fatto che la reazione alternativa di syn-hydroxylation degli alcheni viene utilizzata nel processo di ossido di osmio (VIII), che è un reagente tossico, difficile da raggiungere e costoso. Successivamente, è stato proposto un terzo metodo di syn-hydroxylation di un doppio legame - un processo a tre stadi utilizzando iodio e acetato d'argento - ma la reazione di Wagner è il metodo più antico e ancora più noto di ossidazione a doppio legame lieve.