Come si presenta la formula degli amminoacidi?
La formula generale degli amminoacidi conferma la presenza nella molecola di carbonio, idrogeno, ossigeno, nonché il contenuto di due gruppi funzionali: gruppi carbossilici e amminici. Sono loro che spiegano il carattere più ameno di questi composti, la dualità della loro struttura.
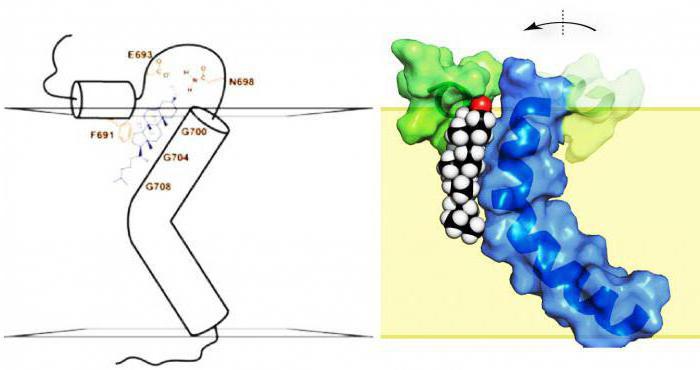
Importanza di composti
Tutti i processi associati all'attività vitale degli organismi si verificano a livello molecolare. Ecco perché è così importante avere una comprensione completa delle funzionalità di tutti materia organica le loro proprietà fisiche e chimiche.
Considera alcuni amminoacidi le cui formule e nomi sono familiari anche agli scolari moderni.
Per diversi decenni, c'è stato un rapido sviluppo della biochimica. Grazie a metodi di ricerca innovativi, è stato possibile spiegare le complesse trasformazioni associate alla sintesi di molecole proteiche. Le informazioni ottenute in laboratori scientifici specializzati sono utilizzate nell'industria farmaceutica medica.
Ad

Caratteristiche biochimiche
Questa scienza sta studiando la composizione chimica degli organismi viventi, la loro struttura, le loro trasformazioni. È grazie alla biochimica che è stata derivata la formula generale di amminoacidi, carboidrati e grassi. Nata nel IX secolo, solo oggi la biochimica è diventata un alleato nel trattamento di malattie ereditarie complesse.
Proprietà e struttura degli amminoacidi
Qualsiasi formula di amminoacidi è un derivato di ammoniaca e acido carbossilico. Attualmente, ci sono circa trecento rappresentanti di questa classe, trovati nella fauna selvatica. Qualsiasi formula di amminoacidi, indipendentemente dalle caratteristiche della catena di carbonio, è costituita da due gruppi funzionali. Ognuno di loro lascia il segno sulle proprietà chimiche generali di questi composti. La formula generale degli aminoacidi è NH2-CH (R) -COOH
Ad
Il radicale, che fa parte della molecola, è un derivato dell'idrocarburo limitante.
Ci sono aminoacidi sostituibili ed essenziali, le loro formule sono considerate nel corso della chimica organica.
Venti membri di questa classe fanno parte delle molecole proteiche, sono considerati la loro componente strutturale essenziale.
Tra quei composti che i diplomati dovrebbero sapere sono: alanina, prolina, leucina, glicina, glutammina, valina, acido aspartico.
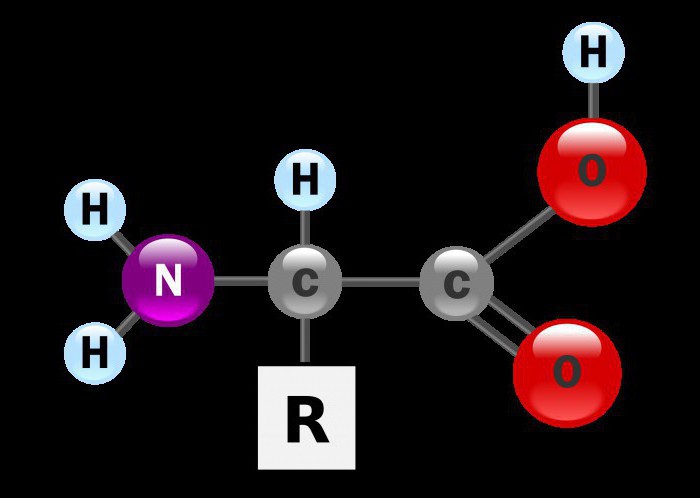
Classificazione Amino
A seconda del tipo di formula amminoacidica, potrebbero esserci alcune differenze nel nome. Nel nostro tempo, composti isolati con radicali non polari. Tra questi, selezionare alanina, prolina, valina, isoleucina, triptofano, fenilalanina. Inoltre, ci sono aminoacidi che hanno radicali polari non caricati: serina, cisteina, glutammina, asparagina.
I composti standard sono componenti integrali delle catene proteiche polipeptidiche, che agiscono come isomeri L-spaziali. Quasi tutti contengono un atomo di carbonio asimmetrico nella struttura, il che spiega la rotazione spaziale libera degli amminoacidi.
Questi composti sono inclusi in cellule microbiche, che si trovano nella composizione di antibiotici.
Il processo di mutua trasformazione degli stereoisomeri è chiamato racemizzazione. Oltre ai rappresentanti standard di questa classe, anche gli aminoacidi non standard sono inclusi nelle molecole proteiche.
A seconda della particolarità della molecola proteica, solo alcuni aminoacidi partecipano alla sua formazione. Ad esempio, l'idrossiprolina è presente nella composizione di collagene.
Tutti gli amminoacidi sono elettroliti deboli, pertanto, in soluzione acquosa subiscono solo una parziale dissociazione. La capacità dei composti di essere sotto forma di ioni polari viene utilizzata quando si analizzano oggetti biologici al fine di identificare la composizione di amminoacidi. Metodi come l'elettroforesi, la cromatografia a scambio ionico sono adatti a questo.
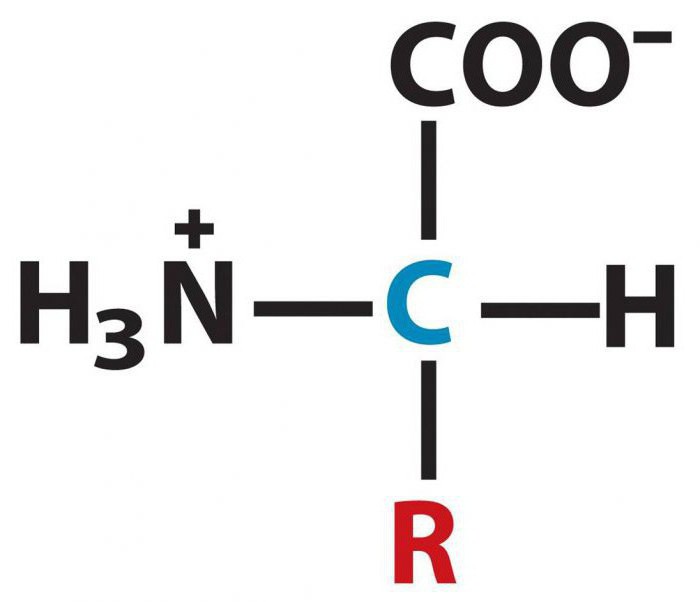
È la sequenza di amminoacidi che determina le caratteristiche della struttura primaria delle molecole proteiche. Tra le principali aree di applicazione di questa classe di sostanze organiche si può notare l'uso nella sintesi organica, l'industria farmaceutica. Gli aminoacidi sono anche usati come mangimi per i bovini.