Cos'è un isomero geometrico?
Gli isomeri geometrici sono isomerismo cis-trans o isomerismo EZ. Le loro azioni sono basate sulla rotazione limitata di legami di carbonio doppio o singolo in composti ciclici.In una connessione ciclica, la rotazione tra il legame singolo di carbonio è limitata e due diversi gruppi sono collegati a ciascun isomero di carbonio in un modo simile. Tali isomeri geometrici spesso differiscono nelle loro proprietà fisiche. Ciò è dovuto alla forma degli isomeri e al momento di dipolo totale. Se i due atomi con la priorità più alta rimangono sullo stesso lato dell'isomero, vengono indicati come Z, e se si trovano nella parte opposta, E.
Breve storia dell'Isomerismo
Il concetto di isomerismo costituzionale è un significativo passo avanti nella storia della chimica moderna, e in particolare nello sviluppo della chimica organica. Alla fine del 1700, diverse sostanze pure erano state isolate studiando la chimica "animale" e "vegetale". Molti furono ricevuti da Karl Wilhelm Scheele (1742-1786). A causa della grande varietà di composti organici, ogni nuova sostanza rappresentava una diversa composizione elementare, che corrispondeva ad un'osservazione generalizzata della chimica "minerale". Il numero di composti organici isolati aumentò nei primi anni del 1800, attraverso l'identificazione di varie sostanze.
Ad
Nel suo libro di storia di chimica Thomas Thomson scrisse nel 1830 che:
Berzelius applicò la teoria dell'atomo anche al regno vegetale, dopo aver analizzato diversi acidi vegetali e mostrando la sua costituzione atomica, ma qui sorge una difficoltà che non possiamo superare nello stato attuale della nostra conoscenza. Ci sono due acidi che consistono esattamente degli stessi atomi. Ora, come dovremmo tenere conto di questa sorprendente differenza nelle proprietà? Indubbiamente, in vari modi in cui gli atomi si trovano in ciascuno di essi.
Thomson ha quindi utilizzato vari schemi di simboli atomici utilizzati in quel momento per spiegare perché due acidi con la stessa composizione elementare, correlata agli isomeri geometrici, hanno proprietà fisiche e chimiche diverse.
Ad
Fino all'inizio del XIX secolo, si riteneva che queste sostanze chimiche presenti negli organismi viventi avessero una forza vitale speciale associata agli esseri viventi e che fossero necessarie nei sistemi viventi per la riproduzione. Nel 1828, Wohler sintetizzò un campione di urea, (NH2) 2CO (anche CH4N2O), che era indistinguibile dall'urea isolata dall'urina biologica.
Ha preparato questa sostanza "animale" da un materiale di partenza inorganico (mineralogico) di ammonio cianato, (NH4) NCO (anche CH4N2O), che è il risultato della combinazione di cloruro di ammonio e argento cianato. Quindi, la barriera tra isomerismo "vivente" e "inanimato" è crollata.
Designazione di isomeri
Nell'isomero cis, due di questi gruppi rimangono sullo stesso lato del doppio legame, mentre nell'isomero trans rimangono nella direzione opposta. Ad esempio, il 2-butene ha due isomeri cis e trans.
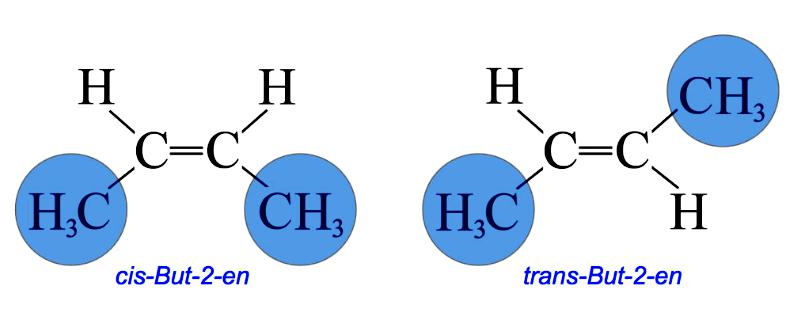
Nell'isomero cis, due gruppi metilici e due gruppi idrogeno rimangono nello stesso lato del doppio legame, mentre nell'isomero trans rimangono nella direzione opposta.
Quando uno o più gruppi collegati a un doppio legame non sono gli stessi, gli isomeri sono chiamati E o Z. Per notificare questo tipo, l'utente dovrà specificare le formule di idrocarburi con isomeri geometrici e determinare l'atomo con la priorità più alta (numero atomico più alto) collegato a ciascun doppio legame C. Se i due atomi con la priorità più alta rimangono sullo stesso lato dell'isomero, che è designato come Z, e, se sono nel lato opposto, sono designati come E.
Ad

Ad esempio, 1 - bromo - 1 - fluoropropano ha due isomeri. In Z-1 - bromo - 1 - fluoropropano, si può vedere che il bromo ha una priorità più alta o un numero atomico più alto (35) rispetto al fluoro (9), che sono collegati a C-1. Il carbonio ha un numero atomico più alto (6) rispetto all'idrogeno (1), che è collegato al C-2 di questo composto. Poiché gli atomi di carbonio con la massima priorità (dal gruppo -CH3) e il bromo attaccato a questi due atomi di carbonio sono sullo stesso lato, questo composto è definito come Z. D'altro canto, in E-1 - bromo - 1 - fluoropropano con il più alto la priorità C e il bromo sono nella direzione opposta, quindi è chiamato E-isomero.
Doppio legame carbonio-carbonio
Gli isomeri sono due molecole che hanno la stessa composizione atomica, ma non sono identiche. Gli atomi di due isomeri possono essere collegati in un ordine diverso (isomerismo strutturale), oppure possono essere collegati allo stesso modo, ma hanno un orientamento diverso: stereoisomerismo spaziale.
Ad
L'isomero strutturale e geometrico in casi particolari, lo stereoisomero, deve soddisfare due requisiti:
- C'è una rotazione limitata nella molecola.
- Entrambi gli atomi coinvolti in un legame restrittivo hanno per loro due gruppi funzionali diversi.
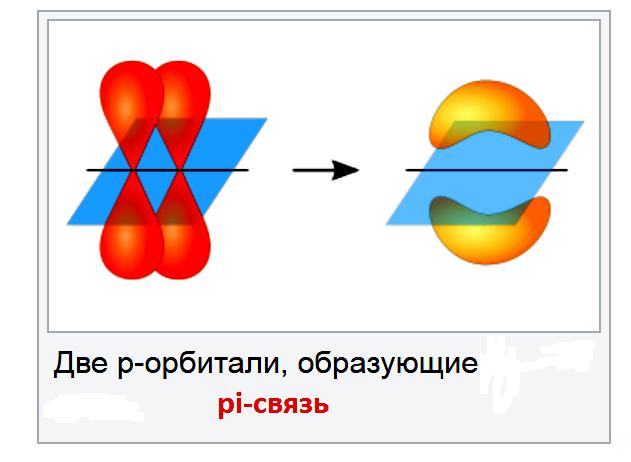
Un esempio comune di rotazione limitata è un doppio legame carbonio-carbonio. Queste connessioni includono la connessione pi, nella maggior parte delle condizioni non è proficuo interromperle.
Gli isomeri geometrici hanno una struttura che influenza le proprietà fisiche di un composto.
Sistema Cis / Trans
Denominare Cis / Trans è il sistema di connessione più facile da usare. Innanzitutto, viene identificata la catena di carbonio più lunga nella molecola e quindi vengono identificati i gruppi funzionali di interesse. Nell'isomero cis, i due gruppi in questione sono sullo stesso lato del doppio legame (cis significa "dallo stesso lato" in latino). Nell'isomero trans, i due gruppi presi in considerazione si trovano su lati opposti del doppio legame (trans significa attraverso la lingua latina). Ad esempio, due diversi isomeri geometrici di butene-2.
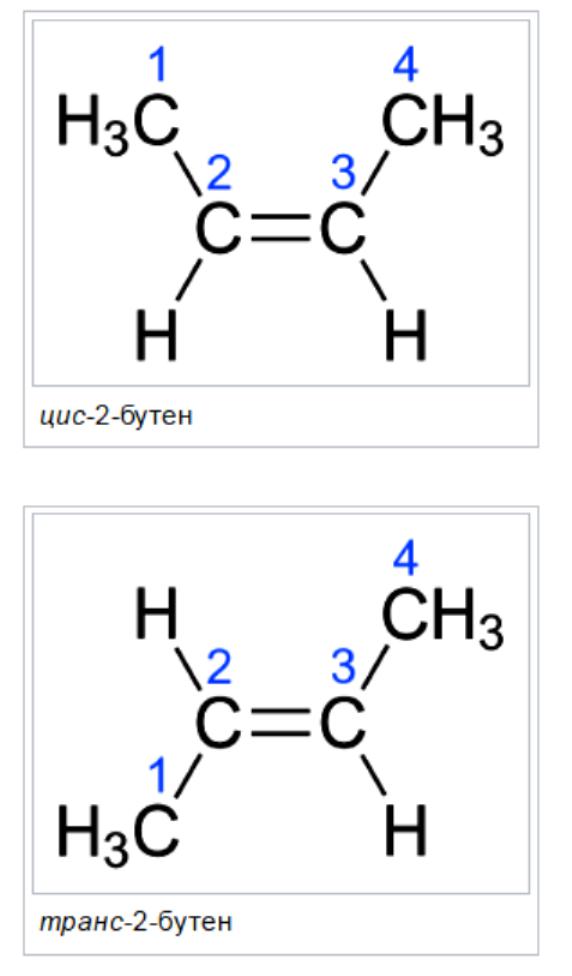
Entrambi gli atomi con un doppio legame hanno gli stessi due gruppi di questi due gruppi, ma differiscono l'uno dall'altro da uno dei due carboni. Il compito è complicato in quanto le catene laterali e i gruppi funzionali diventano più complessi.
La convenzione ufficiale di denominazione IUPAC è E / Z. Non esiste una relazione specifica tra cis / trans ed E / Z ei due sistemi non sono intercambiabili. La designazione E / Z utilizza le regole di priorità Cahn-Ingold-Prelog ed è considerata più affidabile. Il nome IUPAC dell'acido fumarico è l'isomero trans con la formula HO2CCH = CHCO2H e l'acido maleico è l'acido cis-butandiico.
Ad
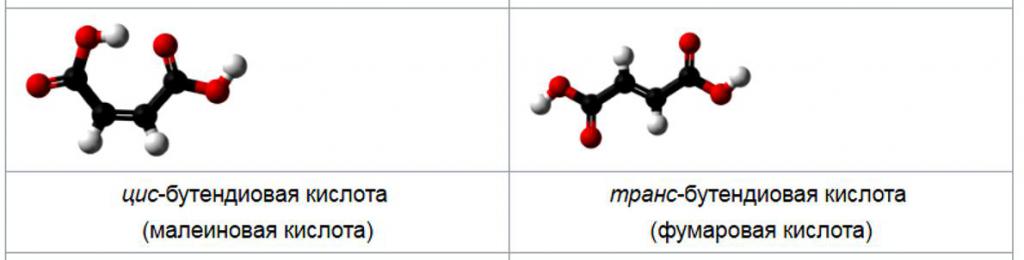
IUPAC è l'Unione internazionale di chimica pura e applicata, che stabilisce norme e standard internazionali per l'etichettatura di prodotti chimici in tutte le lingue.
Composti ciclici
In una connessione ciclica, la rotazione tra il singolo legame di carbonio è limitata. Pertanto, l'isomerismo è anche possibile per questo tipo di composto se due diversi gruppi sono collegati a ciascun carbonio. Ci sono due isomeri di 1,2-dimetilciclopropano.
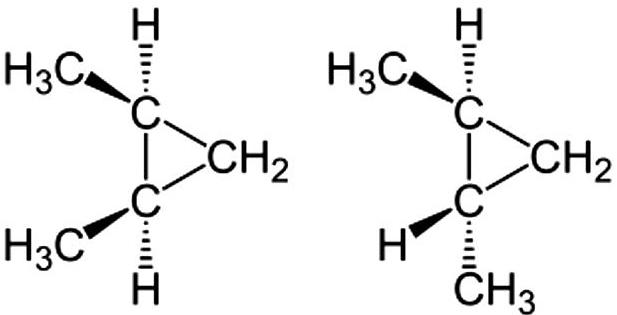
Uno di questi è l'isomero cis, dove i due gruppi metilici sono da un lato, e l'altro è l'isomero trans, dove i due gruppi metilici si trovano dall'altro lato.
Gli isomeri geometrici differiscono nelle loro proprietà fisiche. Ciò è dovuto alla forma degli isomeri e al momento di dipolo totale. Ad esempio, differiscono nel punto di ebollizione. Il punto di ebollizione degli isomeri cis e trans dell'1,2-dicloroetilene è rispettivamente di 60,3 ° C e 47,5 ° C.
Nell'isomero cis, la presenza di due legami dipolari (C-Cl) dà il dipolo molecolare totale. Questo porta a forze dipolo-dipolo intermolecolari. Per questa forza, l'isomero cis ha un punto di ebollizione più alto dell'isomero trans, in cui due legami dipolari (C-Cl) vengono annullati a causa della loro posizione nella direzione opposta.
Il motivo per cui non è possibile ruotare il doppio legame carbonio-carbonio è che ci sono due legami che uniscono gli atomi di carbonio insieme e devi rompere il legame pi. Le connessioni Pi si formano durante la sovrapposizione laterale tra orbitali p. Se cerca di trasformare un doppio legame carbonio-carbonio, gli orbitali p non si allineano più, e quindi il legame pi sarà rotto. L'energia è spesa su questo, e questo succede solo se il composto è molto caldo.
Costruzione di formule strutturali
È molto facile omettere elementi importanti degli isomeri geometrici durante la costruzione di formule strutturali durante la contrazione. Ad esempio, è molto allettante disegnare but-2-ene. Se l'utente scrive questo in modo errato, il composto non sarà più un isomero. Se c'è anche il minimo indizio che possa essere usato un isomero, è sempre necessario usare composti contenenti doppi legami carbonio-carbonio che mostrino gli angoli corretti (120 °) attorno agli atomi di carbonio alle estremità del legame. In altre parole, è necessario utilizzare il formato mostrato nella figura.
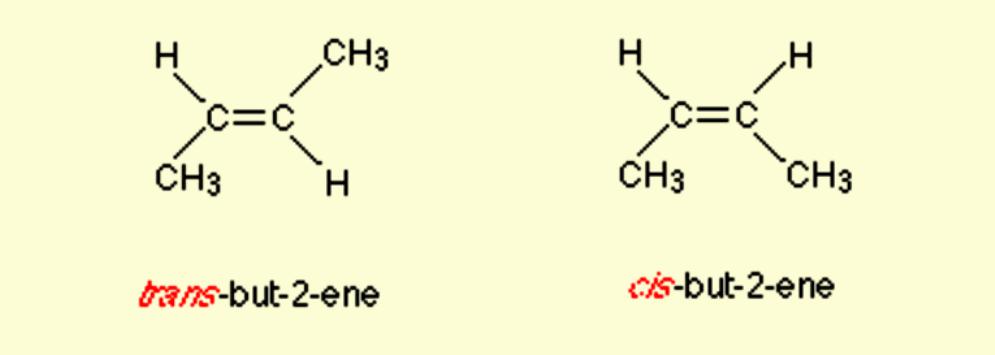
I composti contenenti un doppio legame carbonio-carbonio hanno una rotazione limitata. Per ottenere gli isomeri, devono essere soddisfatte le seguenti condizioni:
- rotazione limitata, solitamente con un doppio legame carbonio-carbonio;
- due gruppi diversi all'estremità sinistra del collegamento e due gruppi diversi all'estremità destra.
Non importa se i gruppi di sinistra coincidono con il giusto o no.
Alcheni: formule molecolari e strutturali
Gli isomeri geometrici degli alcheni includono un numero di composti che consistono in atomi di carbonio e atomi di carbonio in una catena di carbonio. Questo gruppo include una serie omologa con la formula CnH2n. L'alchene più semplice è etene, ha due atomi di carbonio e la formula C2H4.
La formula strutturale per l'etene è mostrata nella figura sopra. In catene alchene più lunghe, gli atomi di carbonio addizionali sono attaccati l'un l'altro usando dei legami covalenti. Ogni atomo di carbonio è anche collegato a sufficienti atomi di idrogeno per produrre un totale di quattro singoli legami covalenti.
In catene con quattro o più atomi di carbonio, il doppio legame può essere posizionato in posizioni diverse, il che porta alla formazione di isomeri strutturali. Oltre agli isomeri strutturali, gli alcheni formano anche stereoisomeri. Poiché la rotazione attorno al legame multiplo è limitata, i gruppi collegati agli atomi con un doppio legame rimangono sempre nelle stesse posizioni relative.
Queste posizioni "bloccate" consentono ai chimici di identificare vari isomeri dai sostituenti per determinare quale sostanza ha isomeri geometrici. Ad esempio, un isomero strutturale C5H10 ha i seguenti stereoisomeri.
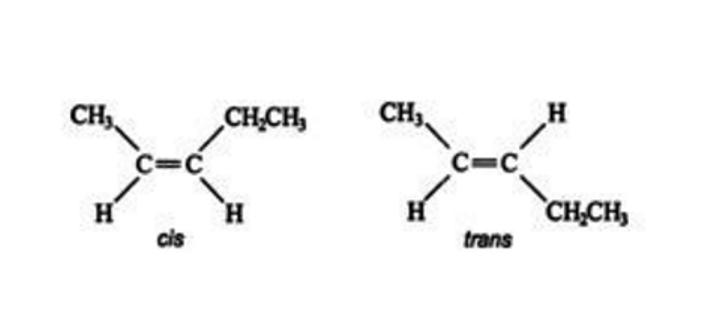
L'isomero a sinistra, in cui due sostituenti (gruppi metilico ed etilico) si trovano sullo stesso lato del doppio legame, è chiamato isomero cis, mentre l'isomero a destra con due sostituenti non idrogeno su lati opposti è l'isomero trans.
Ad esempio, il cloro ha la precedenza perché è più pesante. Sul lato destro, il bromo è superiore al carbonio. Terzo, vengono determinate le posizioni di due atomi di rango superiore. Se due atomi sono nella posizione cis, la posizione è Z (dal tedesco zusammen, che significa "insieme"). Se gli atomi oi gruppi sono in una posizione trans, la posizione è E (dal tedesco entgegen, che significa "il contrario").
Composti a doppio legame dure
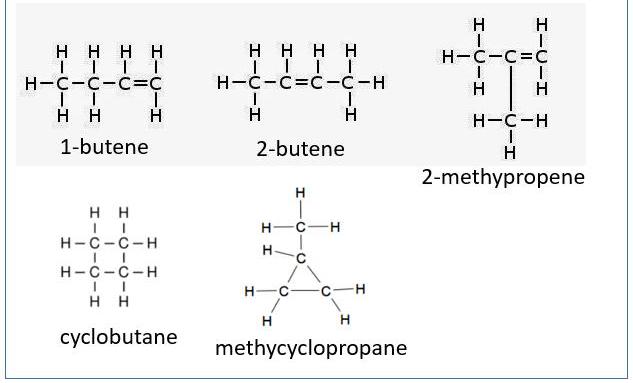
Gli isomeri geometrici butene è un alchene con un doppio legame duro. Ciò significa che ci sono in realtà quattro isomeri, non tre, nella posizione di un doppio legame. Vi sono il quinto e il sesto idrocarburi della stessa composizione, ma non sono alcheni, nonostante la stessa formula.
La formazione di anelli di ciclobutano o metilciclopropano occupa lo spazio di due atomi di idrogeno come un doppio legame, il che porta al fatto che hanno formule identiche a butenoli diversi.
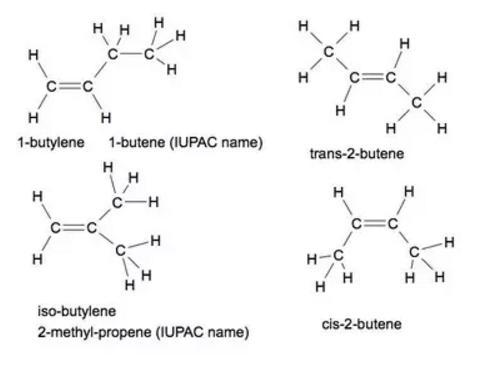
Esempi di isomeri geometrici:
- 1-butilene (1-butene);
- iso-butilene (2-metil-propene);
- cis-2-butilene (cis-2-butene);
- trans-2-butilene (trans-2-butene).
E i bonus: ciclobutano e metilciclopropano, entrambi con la stessa formula empirica degli isomeri del butene, ma non sono alcheni. Il primo nome è "comune" o "banale" nome e il nome tra parentesi è il nome IUPAC.
Isomeri di butene
Butene ha molti usi, dal carburante in auto ai sacchetti della spesa che ogni giorno trasportano centinaia di milioni di persone in tutto il mondo. La formula chimica del butene: C4H8, che significa che è composta da quattro atomi di carbonio e otto atomi di carbonio, il composto si riferisce a un alchene.
Esistono diversi isomeri o strutture molecolari che possono formare questo composto (i nomi IUPAC sono mostrati tra parentesi):
- alfa-butilene (but-1-ene);
- cis-beta-butilene - ((2Z) -but-2-ene);
- trans-beta-butilene - ((2E) -but-2-ene);
- isobutilene (2-metilprop-1-ene).
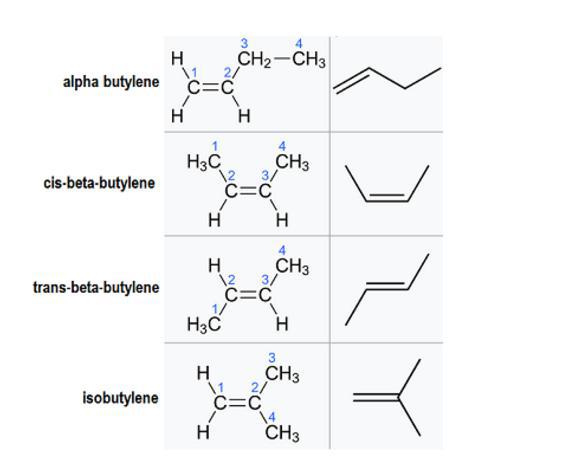
Sebbene abbiano tutti la stessa formula, le loro strutture sono diverse. I rapporti tra ciascuno di questi isomeri geometrici sono fondamentalmente costituzionali, il che significa che hanno la stessa formula molecolare, ma legami diversi. L'eccezione è cis-beta-butilene e trans-beta-butilene.
Molte persone sanno che i grassi trans sono dannosi per l'uomo e i grassi insaturi sono buoni per loro. L'unica differenza tra questi due grassi è che uno ha un legame trans e l'altro ha un link cis, tuttavia questa piccola differenziazione può influenzare significativamente la funzione della molecola.
Con cis-beta-butilene e trans-beta-butilene, gli atomi sono nello stesso ordine, ma le polarità sono diverse. L'isomero cis è polare, con entrambi i gruppi CH3 sullo stesso lato. Ciò lo rende davvero ingombrante e complesso: l'isomero trans è non polare, i gruppi volumetrici di CH3 si alternano, il che dà più spazio nella molecola. Questo rapporto si chiama cis-trans-isomerismo. Gli isomeri cis sono polari, mentre gli isomeri trans non lo sono.
Nonostante il fatto che ciascuno di questi isomeri di butene sia costituito dagli stessi materiali, ognuno di essi ha proprietà fisiche diverse. Ad esempio, il punto di ebollizione:
- Cis-beta-butilene: 3,7 ° C.
- Trans Beta Butilene: 0,8 ° C.
- Isobutilene: -6,9 ° C.
- Alfa butilene: -6,3 ° C.
Materiale per la produzione di materie plastiche
I buteni sono alcheni con quattro atomi di carbonio, C4H8. Esistono diversi isomeri strutturali o configurazionali di butene, compresi isomeri geometrici e ottici. Tutti e quattro i buteni hanno proprietà fisiche simili, essendo gas incolori, pesanti nell'acqua, facilmente solubili in etere e alcani. Le differenze nelle proprietà fisiche sono spiegate dalla struttura delle molecole. Ad esempio, cis-But-2-en ha un punto di ebollizione più alto di trans-But-2-en, perché è un dipolo più forte.
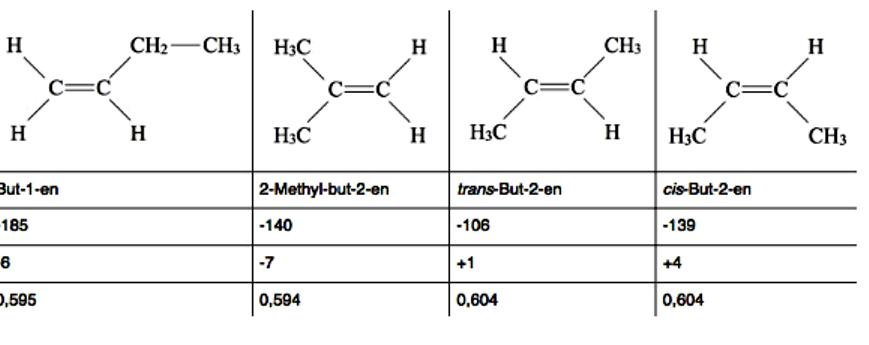
I due gruppi alchilici dell'isomero cis lavorano con il loro effetto + I in una direzione e quindi aumentano, mentre i due gruppi alchilici degli isomeri trans agiscono in direzioni opposte e, quindi, si indeboliscono l'un l'altro. Le formule per gli idrocarburi con isomeri geometrici sono indicate dagli standard IUPAC. Ma 1-en ha un punto di fusione così basso, poiché CC è un legame singolo tra il secondo e il terzo atomo di carbonio, la rotazione libera e il gruppo etile può ruotare attorno all'asse di rotazione in tutte le direzioni.
Ciò rende difficile classificare una molecola in una solida struttura cristallina. I restanti tre buteni con un doppio legame tra il 2 ° e il 3 ° C sono molto rigidi e possono essere facilmente classificati nella struttura cristallina. Pertanto, hanno punti di fusione relativamente alti. Questi argomenti non sono sempre validi, come nell'esempio 2-Methyl-but-2-en (o isobutene). I due gruppi metilici con i loro effetti + I agiscono nella stessa direzione di cis-But-2-en, e in effetti devono essere migliorati. Tuttavia, l'isobutene ha un punto di ebollizione molto basso di solo -7 ° C.
Ma-1-en e But-2-ene sono usati per produrre butadiene e butan-2-olo. Inoltre, gli alcheni sono usati come agenti alchilanti. Quindi un importante combustibile 2,2,4-trimetil-pentano, meglio noto come isoottano, viene ottenuto da isobutene e isobutano. Infine, i butenes sono i materiali di partenza per la produzione di alcune materie plastiche, in quanto sono facili da polimerizzare. La plastica nota su base But-1-en è il polibutene-1, dal quale vengono prodotti i tubi.
Pentano, n-pentano, isopentano
Il pentano, o n-pentano, è uno degli idrocarburi saturi di alcano. L'n-pentano quasi inodore è un liquido in condizioni ambientali ed è un isomero di herakethite di 3 isomeri. Gli isoalcani liquidi ramificati C5 - C16 sono sempre più utilizzati come carburante (Otto, Diesel). Inoltre, questi alcani sono presenti negli oli di riscaldamento e negli oli lubrificanti. Forniscono la masterizzazione completa. Prima di conoscere le caratteristiche di tali composti, è necessario specificare le formule degli idrocarburi con isomeri geometrici:
- Stato fisico - fluido.
- Colore: incolore
- Odore - quasi no.
- Facilmente infiammabile
- I vapori possono formare miscele esplosive se esposti all'aria.
- L'idrosolubilità è molto bassa (praticamente insolubile).
- Connessione molto instabile.
Nome | N-pentano |
Segno chimico | C5H12 |
Massa molare | 72,1488 kg / kmol |
Punto di infiammabilità | 224 K |
infiammazione | 533 bar |
Punto di ebollizione: 1,013 bar | 309,2 K |
Temperatura critica | 469,8 K |
Pressione critica | 33,6 bar |
Calore di evaporazione al punto di ebollizione | 357,46 kJ / kg (25,79 kJ / mol) |
LEL | 1,4% in volume (41 g / m3) |
TTU | 7,8% in volume (235 g / m3) |
L'esplosione | 9,5 bar |
Le fonti più importanti di pentano sono gli oli di petrolio, che differiscono in modo significativo nella loro composizione a seconda della loro origine. La separazione avviene per distillazione frazionata. Le seguenti frazioni sono ottenute qui:
- Olio di paraffina (punto di ebollizione> 320 ° C).
- Olio (punto di ebollizione 180 a 250 ° C).
- Riscaldamento / gasolio (punto di ebollizione 250 a 320 ° C).
- Benzina grezza (punto di ebollizione fino a circa 180 ° C).
- Nella nafta ci sono idrocarburi ramificati (alcani) da C5 a C10.
- Combustione di pentano con ossigeno (stechiometrico).
- I prodotti finali sono anidride carbonica e acqua. Formule di isomeri geometrici: C5H12 + 8O2 ⟹ 5CO2 + 6H2O.
Nome | simboli | Potere calorifico HU [MJ / kg] | Potere calorifico HU [kWh / kg] |
metano | CH4 | 50,013 | 13.89 |
etano | C2H6 | 47,486 | 13.19 |
propano | C3H8 | 46,354 | 12.88 |
N-butano | C4H10 | 45,715 | 12.70 |
N-pentano | C5H12 | 45.0 | 12,50 |
N-esano | C6H14 | 44.64 | 12.40 |
N-eptano | C7H16 | 44.64 | 12.40 |
N-ottani | C8H18 | 44.64 | 12.40 |
N-nonane | C 9 H 20 | 44.64 | 12.40 |
N-decano | C10H22 | 44.64 | 12.40 |
L'isomero geometrico pentene-2 è un solvente universale. È usato per schiumare resina fenolica e polistirolo. È anche richiesto come sostanza di riferimento nella gascromatografia e come propellente nei cilindri a spruzzo.