Ossido di bario: preparazione e uso
La diversità del mondo non cessa di stupire l'umanità. I ricercatori stanno aprendo nuovi orizzonti per noi, sulla base dei risultati della generazione precedente. In questo senso, la chimica è una scienza che non può essere completamente studiata: le moderne soluzioni tecnologiche trovano i campi di applicazione più ottimali e necessari per elementi già noti all'umanità. Il XIX secolo fu un periodo di scoperta, XXI - un periodo di uso più efficiente di essi. Ad esempio, l'ossido di bario è una sostanza studiata a livello multilaterale, ma chissà quali saranno le nuove tecnologie ad essa associate in futuro.
bario
Il metallo alcalino-terroso, che fa parte della crosta, attirò l'attenzione dei chimici nel XVIII secolo. La prima menzione di questo elemento è associata al suo composto di ossigeno: l'ossido di bario. Ha una densità molto alta per il suo tipo, quindi ha ricevuto il nome "pesante", che in seguito divenne il nome dell'elemento stesso. Il metallo è chimicamente attivo, quindi per ottenerlo nella sua forma pura è necessario condurre una serie di reazioni in presenza di un catalizzatore. Il minerale più comune in natura contenente il bario è il suo solfato BaSO 4 (barite con sparo pesante) e BaCO 3 (witterite). È con questi composti che è associato il processo di ottenimento di una sostanza come l'ossido di bario. In futuro, viene utilizzato per isolare il metallo nella sua forma pura e ha le sue direzioni di applicazione.
Ad

I composti più importanti
Come tutti i metalli tipici, il bario entra in una reazione chimica con l'ossigeno, con la sostanza risultante a seconda delle condizioni di processo e del catalizzatore. Ad esempio, la semplice reazione di un ossido con acqua rende possibile la formazione di Ba (OH) 2 - idrossido di bario. L'ossido di bario è ottenuto da nitrato. Composti tipici con tutti gli alogeni: BaF 2 , BaCI 2 , BaI 2 , BaS, BaBr 2 . La formazione di nitrati, solfuri, solfati si verifica a causa dell'interazione di minerali con le corrispondenti soluzioni acide. Oggi vengono utilizzati tutti i più importanti composti di bario. Ma è impossibile escludere nuove scoperte nel campo dell'uso di questa sostanza, con la crescita dell'efficacia tecnologica dei dispositivi, il suo valore aumenterà solo sia a livello industriale che a livello domestico.
Ad

ossidi
Il legame binario di un elemento chimico con l'ossigeno è la forma più comune di sostanza in natura. In questo caso, gli ossidi formano metalli e non metalli. È la caratteristica di un elemento quando interagisce con l'ossigeno che è diventato la base per la formazione della tavola periodica.Mendeleev DI.Per l'industria metallurgica, il processo di produzione di ossido è il modo più accettabile per estrarre una sostanza. Il minerale naturale pre-metallo (sali metallici) è soggetto a varie influenze chimiche volte ad ottenere l'ossido. Di norma, questo processo è accompagnato dal riscaldamento alla temperatura richiesta. L'ossido di bario non fa eccezione. La formula della sostanza ottenuta è: BaO. Gli ossidi possono essere ottenuti in altri modi. Ad esempio, da idrossidi, sali e ossidi più alti stessi stati di ossidazione.
Ad
Ossido di bario
Prima di tutto, va notato che tutti i composti di questo metallo sono tossici (un'eccezione è solfato), quindi è necessario osservare le regole di sicurezza di base quando si lavora. Questo vale per molti elementi chimici. Un altro nome - barite anidra - non va confuso con il solfato, che è un minerale naturale. In condizioni normali (standard), i cristalli bianchi o in polvere, a volte incolori con un tipico reticolo di aspetto cubico, sono un composto di metallo con ossigeno e sono chiamati ossido di bario. La formula della sostanza è BaO. La modifica tecnica dell'ossido può avere un colore grigio, che gli conferisce carbone, non completamente rimosso dalla composizione.

Proprietà fisiche
Il tipico stato aggregato dell'ossido è solido, la densità è 5,72 (20 ° C), la massa molare è 153,34 g / mol. Il composto ha una conduttività termica piuttosto alta di 4,8-7,8 W / (mK) (80-1100K), e la refrattarietà del punto di ebollizione è di 2000 ° C, la temperatura di fusione è di 1920 ° C. L'ossido di bario è stato scoperto nel 1774 da Scheele Karl Wilhelm.
reception
Esistono diversi modi per isolare una sostanza come l'ossido di bario. Sono utilizzati in conformità con lo scopo previsto e la quantità di sostanza ottenuta. Tutti i metodi sono adatti per condizioni di laboratorio e industriali, quindi il produttore sceglie come ottenere l'ossido di bario. Metodi applicabili:
- Calcolo del nitrato di bario pre-precipitato, che si verifica con il rilascio di ossigeno puro. 2Ba (NO 3 ) 2 = 2BaO + 4NO 2 + O 2 .
- Il bario reagisce con l'ossigeno. 2Ba + O 2 = 2BaO. Il catalizzatore ha una temperatura di 500-600 ° C, in questo caso è possibile la produzione di perossido. 2Ba + O 2 = 2BaO 2 . Dopo un ulteriore riscaldamento a 700 ° C, la sostanza si decompone in ossigeno libero e ossido di bario.
- Per il processo di decomposizione del carbonato di bario in ossido e anidride carbonica è richiesta un'esposizione alle alte temperature. BaCO 3 = BaO + CO 2 . Per ottenere una sostanza finale più pulita, è necessario rimuovere l'eccesso di anidride carbonica.
Proprietà chimiche
La maggior parte dei composti di metalli binari con ossigeno presenta proprietà di base. L'equazione dell'ossido di bario (formula BaO) mostra che questa sostanza appartiene specificamente a tali ossidi. Inoltre, questo composto è salino. Le interazioni chimiche tipiche si verificano con le seguenti classi di sostanze:
- L'interazione con l'acqua avviene abbastanza rapidamente, con il rilascio di calore e la formazione di una soluzione alcalina. BaO + H 2 O = Ba (OH) 2 .
- L'ossido interagisce con l'ossigeno in presenza di un catalizzatore (alta temperatura di 600-500 0 C), il risultato è perossido, che viene ulteriormente scomposto nelle sue parti costitutive per l'estrazione di metallo puro o ossido. In questo caso, è necessario aumentare il riscaldamento fino a 700 ° C. 2Ba + O 2 = 2BaO 2 .
- Quanto tipico ossido di base il bario interagisce con gli acidi, a seguito di una reazione chimica si ottengono acqua e il corrispondente sale. BaO + H 2 SO 4 = H 2O + BaSO 4 o BaO + 2HCI = H 2 O + BaCI 2.
- Ossidi acidi reagire con BaO, il risultato dell'interazione sono i sali. BaO + CO 2 = BaCO 3 o BaO + SO 3 = BaSO 4 .
- Al fine di liberare il bario puro, l'ossido viene calcinato con metalli che assorbono l'ossigeno escreto. Questi sono silicio, alluminio, zinco o magnesio.
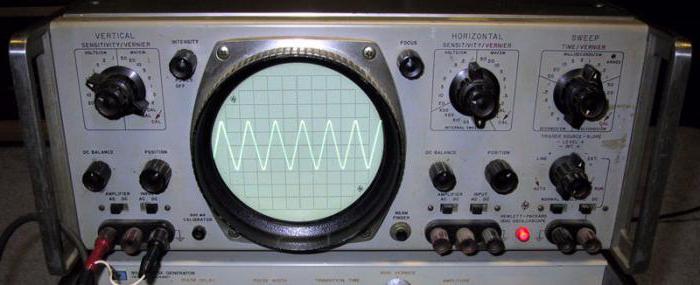
applicazione
Il bario e i suoi composti conferiscono una luminosità del colore molto potente quando si ricopre la superficie di altre sostanze. Pertanto, il manganese e gli ossidi di bario sono le unità di misura del coefficiente di luminosità. È usato per ottenere il colore verde in pirotecnica, con decorazioni decorative composte da smalti e smalti. Il costo piuttosto basso della lavorazione e della produzione, l'elevato livello di generazione di calore rende possibile l'utilizzo dell'ossido come catalizzatore quando si eseguono reazioni chimiche. In particolare, questa sostanza viene utilizzata per isolare il metallo puro (Ba), per ottenere idrossido e perossido. Fabbricazione di ceramiche utilizzate alle temperature più basse (azoto liquido), si verifica con ossido di bario. Il processo di sintesi include metalli delle terre rare e ossido di rame. Il campo di applicazione della sostanza nella realizzazione degli strumenti è piuttosto ampio. L'ossido di bario viene utilizzato per coprire tubi oscillografici e televisivi, vari tipi di catodi e prodotti per vuoto elettronici. Serve da massa attiva per potenti batterie di ossido di rame. L'ossido di bario è uno degli elementi principali nella composizione del vetro, che ha una direzione d'uso piuttosto specifica, viene utilizzato per rivestire la superficie delle barre di uranio. Per creare occhiali da vista questa sostanza è anche indispensabile.