Proprietà chimiche dei metalli alcalino-terrosi. Elenco dei metalli alcalino-terrosi
Il secondo gruppo del sistema periodico di DI Mendeleev contiene un gruppo di elementi che sono molto simili nelle loro proprietà metalli alcalini tuttavia, sono inferiori nell'attività. Contiene berillio e magnesio, oltre a calcio, stronzio, bario e radio. Sono conosciuti con il nome generale - elementi di terra alcalina. Nel nostro articolo familiarizzeremo con la loro distribuzione nella natura e nell'applicazione nell'industria, e studieremo anche le principali proprietà chimiche dei metalli alcalino-terrosi.

Caratteristiche generali
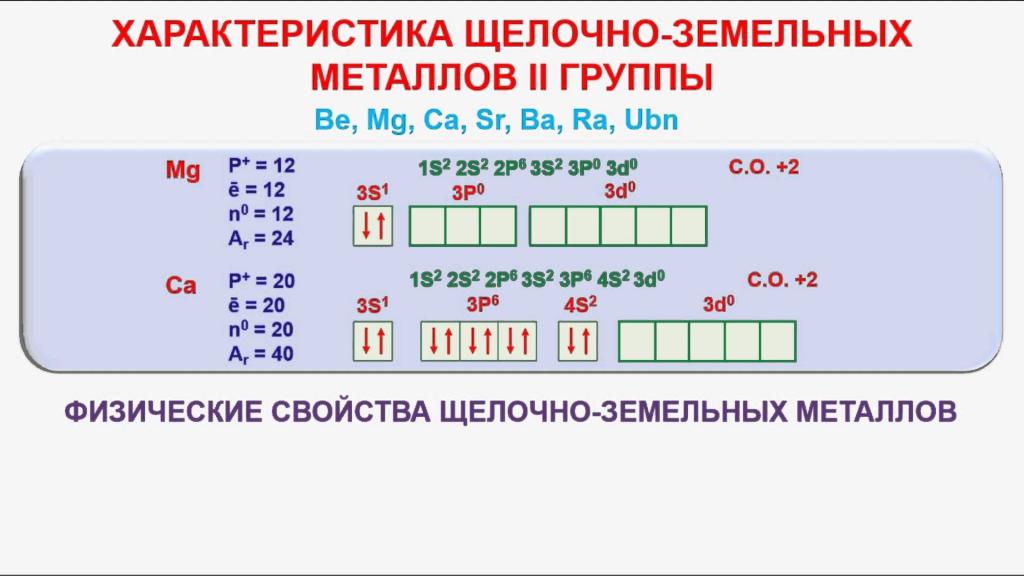
Tutti gli atomi sopra gli elementi elencati contengono due elettroni nello strato di energia esterna. Interagendo con altre sostanze, rinunciano sempre alle loro particelle negative, passando allo stato di cationi con una carica di 2+. Nelle reazioni redox, gli elementi si comportano come forti agenti riducenti. All'aumentare della carica nucleare, aumentano le proprietà chimiche dei metalli alcalino-terrosi e la loro attività. Si ossidano rapidamente nell'aria, formando un film di ossido sulla loro superficie. La formula generale per tutti gli ossidi è RO. Corrispondono agli idrossidi con la formula R (OH) 2 . Le loro proprietà di base e la solubilità in acqua aumentano anche con l'aumento del numero di serie dell'elemento.
Proprietà speciali di berillio e magnesio
In alcune delle loro proprietà, i primi due rappresentanti del sottogruppo principale del secondo gruppo differiscono in qualche modo da altri elementi alcalino-terrosi. Ciò si manifesta, in particolare, durante la loro interazione con l'acqua. Ad esempio, le proprietà chimiche del berillio sono tali da non reagire affatto con H 2 O. Il magnesio interagisce con l'acqua solo quando riscaldato. Ma tutti gli elementi alcalino-terrosi reagiscono facilmente con esso a temperatura normale. Quali sostanze si formano allo stesso tempo?
Ad

Basi di metallo alcalino terroso
Calcio, bario e altri membri del gruppo stanno rapidamente sostituendo l'idrogeno dall'acqua, con conseguente loro idrossidi. L'interazione dei metalli alcalino-terrosi con l'acqua scorre rapidamente, con il rilascio di calore. Soluzioni di basi di calcio, bario, stronzio, lenitive al tatto, quando vengono a contatto con la pelle e le mucose degli occhi, causano gravi ustioni. Il primo aiuto in questi casi sarà il trattamento della superficie della ferita con una soluzione debole di acido acetico. Neutralizza gli alcali e riduce il rischio di necrosi dei tessuti danneggiati.
Proprietà chimiche dei metalli alcalino-terrosi
L'interazione con ossigeno, acqua e non metalli è l'elenco principale delle proprietà dei metalli inclusi nel secondo gruppo del sistema periodico di elementi chimici. Ad esempio, il calcio anche in condizioni normali reagisce con alogeni: fluoro, cloro, bromo e iodio. Quando riscaldato, si combina con zolfo, carbonio e azoto. Ossidazione dura: bruciore, termina con la formazione ossido di calcio: 2Ca + O 2 = 2 CaO. L'interazione dei metalli con l'idrogeno porta alla comparsa di idruri. Sono sostanze refrattarie bianche con reticoli cristallini ionici. Le importanti proprietà chimiche dei metalli alcalino-terrosi includono la loro interazione con l'acqua. Come accennato in precedenza, il prodotto di questa reazione di sostituzione è l'idrossido di metallo. Si noti inoltre che nel sottogruppo principale del secondo gruppo, il calcio occupa il posto più significativo. Pertanto, ci soffermiamo sulle sue caratteristiche in modo più dettagliato.
Ad
Calcio e suoi composti
Il contenuto dell'elemento nella crosta è fino al 3,5%, il che indica la sua ampia distribuzione nella composizione di minerali come calcare, gesso, marmo e calcite. La composizione del calcio naturale comprende sei tipi di isotopi. Si trova anche nelle fonti d'acqua naturali. I composti di metalli alcalini sono studiati in dettaglio nel corso della chimica inorganica. Ad esempio, nella classe 9, gli studenti impareranno che il calcio è un metallo bianco-argento leggero ma forte. I suoi punti di fusione e di ebollizione sono più alti di quelli degli elementi alcalini. Il principale metodo per ottenere - l'elettrolisi di una miscela di sali fusi di cloruro e fluoruro di calcio. Le principali proprietà chimiche sono le sue reazioni con ossigeno, acqua e non metalli. Tra i composti di metalli alcalini, l'ossido e il calcio sono i più importanti per l'industria. Il primo composto è ottenuto da gesso o calcare bruciandoli.
Ad

Inoltre, l'idrossido di calcio è formato da ossido di calcio e acqua. La sua miscela con sabbia e acqua è chiamata malta da costruzione. Continua ad essere usato come intonaco e per unire i mattoni durante la posa delle pareti. La soluzione di idrossido di calcio, chiamata acqua di calce, viene utilizzata come reagente per rilevare il biossido di carbonio. Quando si passa anidride carbonica attraverso una soluzione acquosa trasparente di Ca (OH) 2 , si osserva la sua torbidità a causa della formazione di precipitato insolubile. carbonato di calcio.
Il magnesio e le sue caratteristiche
La chimica dei metalli alcalino-terrosi studia le proprietà del magnesio, concentrandosi su alcune delle sue caratteristiche. È un metallo bianco molto leggero, argentato. Il magnesio sciolto in un'atmosfera altamente umida assorbe attivamente le molecole di idrogeno dal vapore acqueo. Raffreddandosi, il metallo li rilascia quasi completamente in aria. Reagisce molto lentamente con l'acqua a causa della formazione di un composto poco solubile, l'idrossido di magnesio. Gli alcali non agiscono affatto sul magnesio. Il metallo non reagisce con alcuni acidi: solfato concentrato ed idrofluorico, grazie alla sua passivazione e alla formazione di un film protettivo sulla superficie. La maggior parte degli acidi minerali scioglie il metallo, che è accompagnato dal rapido rilascio di idrogeno. Il magnesio è un forte agente riducente, sostituisce molti metalli dai loro ossidi o sali:
Ad
BeO + Mg = MgO + Be.
Il metallo insieme al berillio, al manganese, all'alluminio è usato come agente legante per l'acciaio. Proprietà particolarmente preziose sono le leghe contenenti magnesio - elettroni. Sono utilizzati nella produzione di aerei e automobili, nonché nei dettagli della tecnologia ottica.
Il ruolo degli elementi nell'attività vitale degli organismi
Diamo esempi di metalli alcalino-terrosi, i cui composti sono comuni nella fauna selvatica. Il magnesio è l'atomo centrale nelle molecole di clorofilla nelle piante. Partecipa al processo di fotosintesi e fa parte dei centri attivi del pigmento verde. Gli atomi di magnesio fissano l'energia della luce, trasformandola in energia di legami chimici di composti organici: glucosio, amminoacidi, glicerina e acidi grassi. Un ruolo importante è svolto dall'elemento come componente necessario degli enzimi che regolano il metabolismo nel corpo umano. Il calcio è un macronutriente che assicura il passaggio efficiente degli impulsi elettrici attraverso il tessuto nervoso. La presenza dei suoi sali di fosfato nella composizione delle ossa e dello smalto dei denti conferisce loro durezza e forza.
Berillio e le sue proprietà
I metalli alcalino-terrosi includono anche berillio, bario e stronzio. Considera il berillio. L'elemento non è ampiamente distribuito in natura, principalmente nella composizione dei minerali, ad esempio il berillo. Le sue varietà contenenti impurità multicolore formano gemme: smeraldi e acquemarine. Una caratteristica delle proprietà fisiche è la fragilità e l'elevata durezza. Una caratteristica distintiva di un atomo di un elemento è la presenza sul secondo livello di energia esterna non otto, come tutti gli altri metalli alcalino-terrosi, ma solo due elettroni.
Ad

Pertanto, il raggio dell'atomo e dello ione è sproporzionatamente piccolo, l'energia di ionizzazione è grande. Provoca un'alta resistenza. reticolo cristallino metallo. Le proprietà chimiche del berillio si distinguono anche da altri elementi del secondo gruppo. Reagisce non solo con acidi, ma anche con soluzioni alcaline, spostando l'idrogeno e formando idrossibutilati:
Be + 2NaOH + 2H 2 O = Na 2 [Be (OH) 4 ] + H 2 .
Il metallo ha un numero di caratteristiche uniche. Grazie alla possibilità di saltare i raggi X, viene utilizzato per la fabbricazione di tubi a raggi X di Windows. Nell'industria nucleare, l'elemento è considerato il miglior moderatore e riflettore dei neutroni. In metallurgia, viene utilizzato come prezioso additivo legante che migliora le proprietà anti-corrosione delle leghe.
Stronzio e bario
Gli elementi sono abbastanza comuni in natura e, proprio come il magnesio alcalino terroso, sono parte dei minerali. Chiamiamoli: è barite, celestina, stronzio. Il bario ha l'aspetto di un metallo plastico di colore bianco-argento. Come il calcio, è rappresentato da diversi isotopi. Nell'aria interagisce attivamente con i suoi componenti, ossigeno e azoto, per formare ossido di bario e nitruro. Per questo motivo, il metallo viene stoccato sotto uno strato di paraffina o olio minerale, evitando il suo contatto con l'aria. Entrambi i metalli formano perossidi quando riscaldati a 500 ° C.

Di questi, il perossido di bario, usato come candeggina per tessuti, ha un'applicazione pratica. Le proprietà chimiche dei metalli alcalino-terrosi, del bario e dello stronzio sono simili alle proprietà del calcio. Tuttavia, la loro interazione con l'acqua è molto più attiva e le basi risultanti sono più forti dell'idrossido di calcio. Il bario viene utilizzato come additivo per liquidi refrigeranti metallici, riducendo la corrosione, nell'ottica, nella fabbricazione di dispositivi elettronici per vuoto. Lo stronzio è richiesto nella produzione di celle fotovoltaiche e fosfori.
Reazioni qualitative usando ioni di metalli alcalino-terrosi
Composti di bario e stronzio sono esempi di metalli alcalino-terrosi ampiamente utilizzati in pirotecnica a causa della loro brillante colorazione della fiamma con gli ioni. Pertanto, il solfato di stronzio o il carbonato conferiscono un bagliore rosso carminio alla fiamma e i corrispondenti composti di bario ne danno uno giallo-verde. Per la rilevazione degli ioni di calcio in laboratorio, sulla fiamma del bruciatore vengono versati diversi granuli di cloruro di calcio, la fiamma è dipinta in un colore rosso mattone.

Una soluzione di cloruro di bario viene utilizzata in chimica analitica per rilevare il residuo acido dell'acido solfato nella soluzione. Se un precipitato bianco di solfato di bario si forma quando le soluzioni vengono versate, significa che c'erano SO 4 2 particelle in esso.
Nel nostro articolo abbiamo studiato le proprietà dei metalli alcalino-terrosi e abbiamo fornito esempi della loro applicazione in vari settori.