Legame covalente: concetto, segni, significato chimico
Un importante tipo di legame tra gli atomi
Il legame covalente con quello ionico è il tipo principale legame chimico. Caratterizza l'abilità degli atomi di interagire tra loro e creare gusci densi a livello di elettroni che fungono da base per molecole con proprietà completamente nuove.
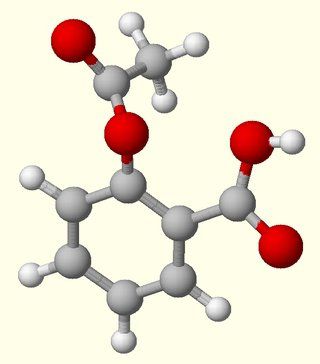
Il concetto e il significato chimico di questo tipo di legame chimico
Secondo la regola, il legame covalente è molto comune in natura. tipo di legame chimico in cui avviene l'unione degli elettroni degli atomi, con la conseguente formazione di un comune orbitale molecolare Questo guscio appena formato permette agli atomi di portare il numero dei loro elettroni al numero che la loro orbita esterna può ospitare. Di conseguenza, la molecola acquisisce stabilità e stabilità.
Ad

Caratteristiche chiave e proprietà
Il termine "legame covalente" indica il desiderio degli atomi di interagire con altri atomi, la loro capacità di formare un composto stabile. Tale legame può verificarsi sia tra atomi identici (ad esempio idrogeno o cloro), sia tra atomi diversi (ad esempio, nelle molecole di idrogeno solforato, acido cloridrico). Nel primo caso, si forma una nuvola di elettroni specifica, le cui particelle elementari, localizzate sugli orbitali esterni, iniziano a servire entrambi i nuclei, senza prestare attenzione al fatto che siano "loro" o "alieni".
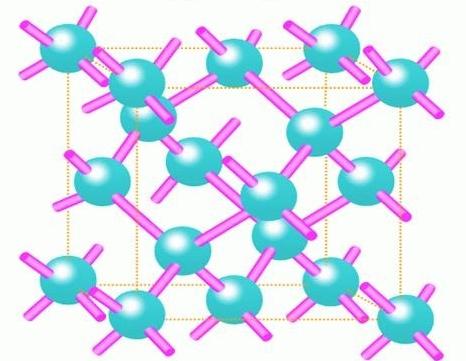
Sforzarsi di ridurre i costi energetici
La ragione principale per cui gli atomi tendono a portare l'elettrone mancante al loro involucro esterno è il loro desiderio di ridurre i costi energetici. Dopo tutto, è noto da tempo che l'energia totale di una molecola dello stesso idrogeno è molto più bassa della somma delle energie di due atomi dello stesso elemento. Quindi, il legame covalente è una reazione naturale della materia al desiderio di ridurre significativamente il costo delle risorse per la sua esistenza.
Ad
Un'altra importante conseguenza
Nella formazione e nell'ulteriore esistenza di questi composti, vi è un'altra importante regolarità. Il fatto è che il legame covalente si basa su certe distanze tra gli atomi nella molecola. Non possono essere inferiori ad un certo valore, perché altrimenti il sistema perderà la sua stabilità e la sua energia aumenterà rapidamente. Questa proprietà viene utilizzata attivamente in vari settori dell'economia nazionale, ad esempio nell'industria nucleare.
La famosa regola di Lewis
Il legame covalente, le cui proprietà sono attivamente studiate al momento, funziona sulla base della famosa regola dell'ottetto-doppietto, che fu formulata all'epoca dal famoso chimico Lyis. Secondo il suo concetto, la formazione di questo tipo di legame richiede un tale numero di elettroni che i gusci esterni degli atomi diventano completi, come quella che è la struttura dei gas inerti. Ad esempio, in una molecola di idrogeno i suoi elementi costituenti assomigliano all'elio e in una molecola di cloro, l'argon.