Meccanismo donatore-accettore - che cos'è?
Il meccanismo donatore-accettore della formazione di un legame chimico comporta il trasferimento di carica tra l'accettore e il donatore senza creare un legame chimico comune tra di loro. È anche possibile trasferire una coppia solitaria di elettroni all'accettore dal donatore, risultante in un legame.
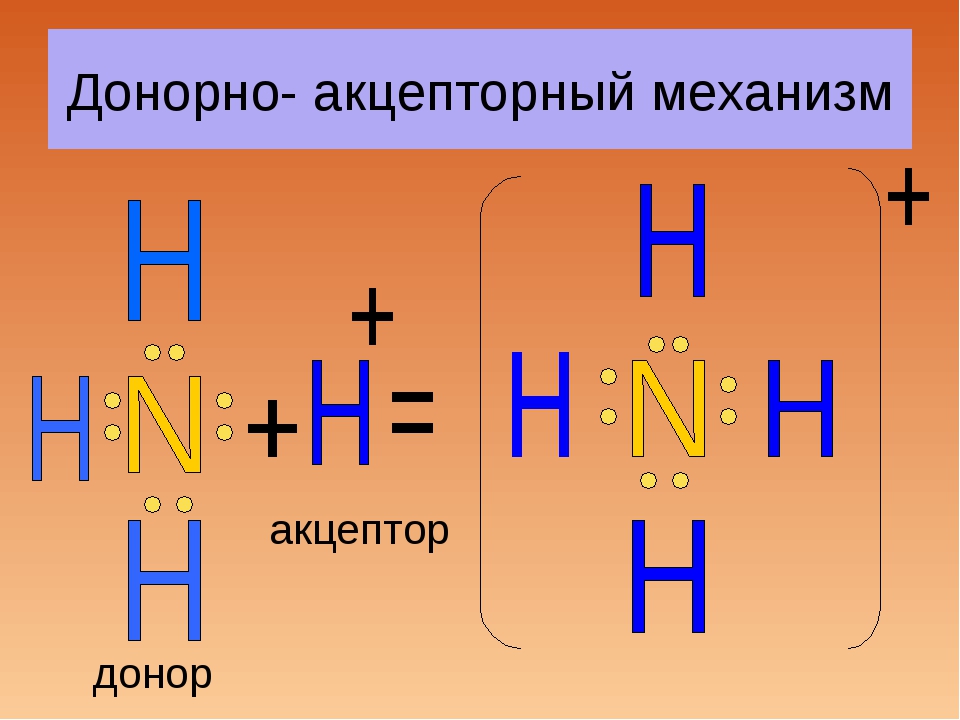
La formazione di sali di ammonio
Si consideri il meccanismo di donatore-accettore sull'esempio di sali di ammonio. Iniziamo con l'interazione di ammoniaca (NH3) e trifluoruro di boro (BF3). Durante la reazione, vengono liberati 171,4 kJ / mol di energia. L'interazione procede secondo l'equazione:
NH 3 + BF 3 = NH 3 BF 3
Dei quattro orbitali presenti nell'atomo di boro, tre sono pieni di elettroni, quindi c'è un orbitale libero. Nella molecola di ammoniaca, quattro orbitali di azoto sono dotati di elettroni e tre di essi sono integrati da elettroni di idrogeno attraverso un meccanismo di scambio. Un orbitale ha una coppia di elettroni che appartiene solo all'atomo di azoto. Si chiama una coppia di elettroni solitari. È grazie a lei che è possibile il meccanismo di donatore-accettore.
Ad
La connessione tra ammoniaca e trifluoruro di boro è possibile a causa del fatto che la coppia di elettroni liberi ammoniaca è posta sugli orbitali liberi del fluoruro di boro.
Questo è il meccanismo donatore-accettore per la formazione di legami covalenti. L'atomo di azoto aumenta la valenza attraverso l'uso di una coppia di elettroni solitari per un ulteriore legame. Il boro aumenta la valenza collocando elettroni aggiuntivi nell'orbitale.
Pertanto, la valenza di questi elementi chimici è caratterizzata sia da elettroni spaiati, sia da coppie di elettroni solitari e orbitali liberi a livello di energia esterna.
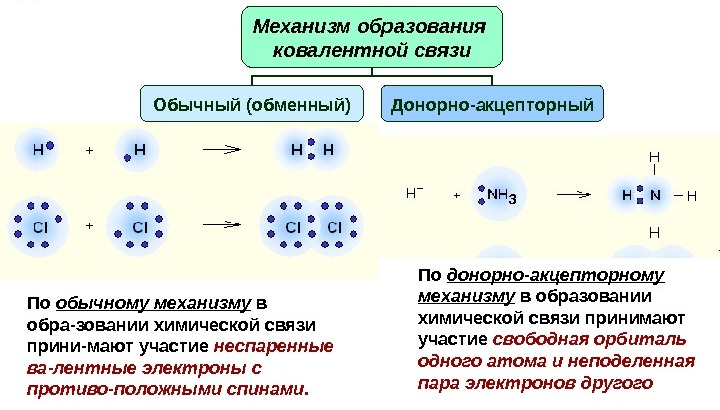
definire
Il donatore in questo esempio è l'atomo di azoto, che dona la sua coppia di elettroni per formare un legame chimico. Accettatore è boro, avendo un orbitale libero, accettando una coppia elettronica.
Il processo è accompagnato da una diminuzione dell'energia potenziale di questo sistema, il rilascio di una quantità equivalente di energia. Le domande riguardanti il meccanismo di formazione di questo tipo di legame covalente sono incluse nel corso del programma scolastico in chimica, sono proposte nelle prove finali per i laureati della scuola secondaria.
Ad
La formazione del catione di ammonio
Un legame covalente formato da un meccanismo donatore-accettore è caratteristico dei sali di ammonio. Soffermiamoci sulle sue caratteristiche. Quindi, è dal meccanismo donatore-accettore che si forma il legame tra atomi di azoto e idrogeno nella reazione:
NH 3 + H + = NH 4 +
L'accettore è l'orbita vuota del catione di idrogeno. L'azoto nel catione di ammonio mostra valenza 4. La formazione di un legame si verifica anche a causa di una coppia di elettroni che appartenevano all'azoto prima dell'inizio dell'interazione.
Questo è un legame covalente dal meccanismo donatore-accettore. Come risultato dell'interazione, si forma un catione di ammonio, che dal meccanismo ionico sarà combinato con gli anioni contenuti negli acidi.

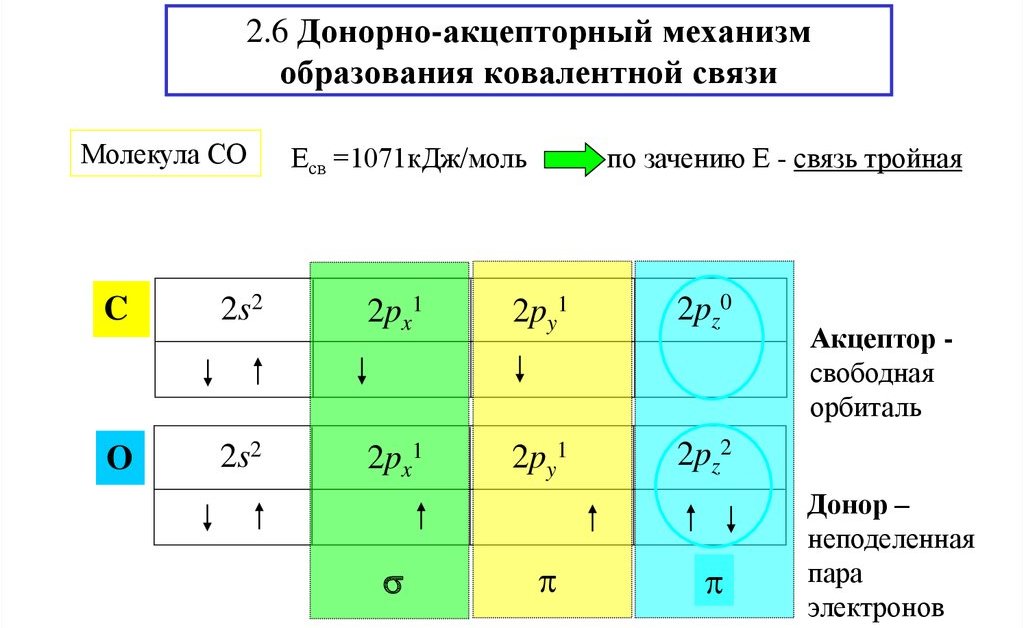
Formazione di monossido di carbonio
Il meccanismo donatore-accettore può essere considerato utilizzando la molecola di CO come esempio. All'atomo di carbonio sul livello di energia esterna ci sono due elettroni spaiati. Lo stesso numero di elettroni spaiati è all'atomo di ossigeno. Di conseguenza, si crea un doppio legame tra gli atomi.
A causa di una coppia di elettroni di ossigeno e di un orbitale di carbonio vuoto, viene utilizzato un meccanismo donatore-accettore per ottenere il legame.
Molecola di acido nitrico
A causa della presenza di tre elettroni spaiati, l'atomo di azoto in questo composto forma tre varianti di legami: con doppio ossigeno, singolo ossigeno con gruppo ossidrile. Secondo il meccanismo donatore-accettore, si crea un legame tra un altro atomo di ossigeno e azoto.
Gli elettroni spaiati vengono posizionati su un orbitale, mentre uno viene rilasciato.
Si può anche supporre che l'atomo di azoto sia dato all'ossigeno dall'elettrone. Trasformato in un catione di ammonio con 4 elettroni spaiati, mantiene l'anione dovuto alle forze dell'interazione elettrostatica.
Ad
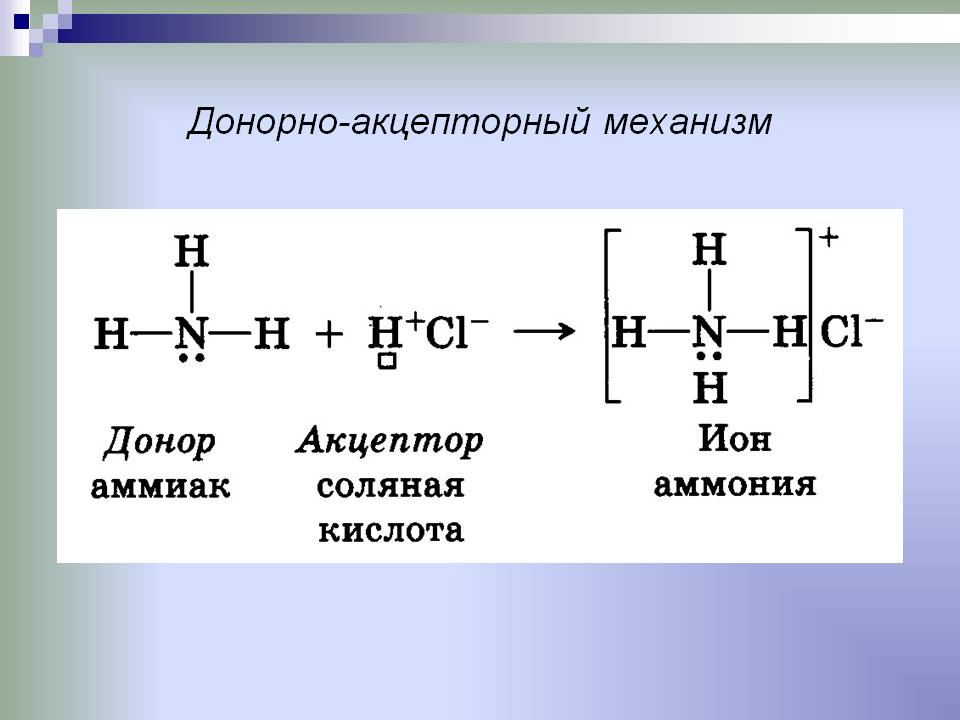
Proprietà di comunicazione
Come donatore, ci sono molecole in cui ci sono atomi di N, O, F, Cl, associati agli atomi di altri elementi chimici. L'accettore è una particella con livelli elettronici vuoti. Ad esempio, questi possono essere rappresentanti di famiglie-d che hanno d-orbitali non riempiti.
Nella molecola di ammoniaca si usano tre elettroni spaiati dell'atomo di azoto per formare il legame e un elettrone di 1s di tre atomi di idrogeno è coinvolto. Le connessioni sono lungo i tre assi degli orbitali p. La molecola ha una variante di una piramide regolare, agli angoli dei quali si trovano gli atomi di idrogeno e all'apice - azoto di azoto. L'angolo tra i legami è di 107 gradi. Molecole similiformi formano i seguenti elementi con l'idrogeno: antimonio, arsenico, fosforo.
Ad
Le proprietà del legame covalente, che è formato dal meccanismo donatore-accettore, non differiscono dalle caratteristiche del legame formato dal meccanismo di scambio. I donatori possono essere azoto, zolfo, fosforo, atomi di ossigeno, che possiedono coppie di elettroni solitari su piccoli orbitali di valenza.
La funzione dell'accettore viene eseguita da cationi di idrogeno, parte di metalli p, ad esempio alluminio, che formano lo ione AlH 4 .
Inoltre, gli accettori sono elementi d, che hanno una cella di energia vuota nello strato elettronico esterno.
Va notato che tutte le principali caratteristiche, come la saturazione, la lunghezza, la molteplicità, sono applicate a questo meccanismo di formazione della comunicazione.
Caratteristiche dei composti organici
L'interazione del meccanismo di scambio è possibile per i donatori biologici. In particolare, tra questi ci sono i donatori di π, un tipico esempio dei quali è il tetrakis (dimetilammino) etilene (TDAE), accettori organici (fullereni), chinodimetani con sostituenti accettore.
L'interazione chimica di tali composti crea un complesso con trasferimento di carica. In esso, un donatore con carica positiva interagisce con un accettore caricato negativamente a causa delle forze di natura elettrostatica. Significativi sono i sistemi in cui il trasferimento di carica nello stato elettronico di terra si verifica parzialmente, e nel caso di eccitazione fotografica, viene osservato il suo trasferimento completo.
Tali sistemi, le diadi donatore-accettore, le triadi all'interno delle quali esiste un gruppo ponte tra l'accettore e il donatore, che consente di aumentare la durata dello stato con il trasferimento di carica elettrica, sono utilizzati per produrre dispositivi che convertono l'energia solare. Un fenomeno simile associato al trasferimento di carica in una qualsiasi delle sue forme è utilizzato in molti processi biologici.
Ad
Questo è il motivo per cui le caratteristiche dell'interazione attraverso il meccanismo donatore-accettore nei composti organici sono esaminate in dettaglio, le possibilità di accelerare (rallentare) processi simili, vengono analizzate le opzioni per introdurre sostanze aggiuntive (catalizzatori).
Riassumiamone alcuni
L'interazione donatore-accettore è una delle manifestazioni più importanti del legame chimico polare covalente. Presta particolare attenzione alla chimica inorganica, analitica e organica.
Ad esempio, è proprio dal punto di vista del meccanismo donatore-accettore che viene spiegata la formazione di legami covalenti localizzati in ioni molecolari di composti (complessi) di coordinazione. Il legame in essi è creato a causa della coppia di elettroni solitari del ligando e degli orbitali liberi dell'agente complessante. Il meccanismo di accettazione dei donatori spiega anche la formazione di prodotti intermedi. In particolare, questa è la creazione di complessi con trasferimento di carica.
Esiste un modello di meccanismo donatore-accettatore solo nel quadro del concetto di valenza come la possibilità di localizzare la densità elettronica nel processo di formazione di legami covalenti. Questo meccanismo è la base per la formazione di vari composti complessi. Tale interazione è necessaria per le trasformazioni acido-base correlate al trasferimento di ioni idrogeno (accettore), la formazione di nanostrutture.