Caratteristiche della struttura dell'atomo di idrogeno
L'elemento più comune nello spazio, costituito dagli atomi più leggeri, è l'idrogeno. Fu scoperto nel 14 ° secolo dal grande alchimista Paracelso. Gli scienziati sono giustamente considerati i fondatori non solo della medicina, ma anche della chimica. La struttura dell'atomo di idrogeno è stata ulteriormente rivista da Niels Bohr. L'elemento è stato poi scoperto dagli astronomi come parte del Sole e di altri pianeti, così come nelle nebulose a stelle di gas. Il processo di trasformazione degli atomi di idrogeno in atomi di elio si verifica in essi, in altre parole, si osserva una reazione nucleare. Nel nostro articolo studieremo non solo la struttura dell'atomo di idrogeno, ma considereremo anche le caratteristiche delle proprietà di questo elemento chimico.
Il posto dell'elemento nel sistema periodico
L'idrogeno è l'unico elemento chimico che si trova immediatamente in due gruppi del sistema periodico: 1 e 7. Il seguente fatto può essere spiegato: esibisce proprietà chimiche doppie. La speciale struttura dell'atomo di idrogeno gli consente di donare il suo unico elettrone agli atomi, per esempio, degli elementi attivi - non metalli. Questi sono principalmente alogeni: aggressivi nelle loro proprietà fluoro, cloro, bromo e iodio. H 2 interagisce facilmente con calcogeni: zolfo, ossigeno, selenio. In questo caso, gli atomi di idrogeno vengono convertiti in cationi - particelle caricate positivamente.
Ad
A causa di questa caratteristica, l'elemento prende il suo posto nel primo gruppo del sistema periodico. Il meccanismo della reazione tra metalli e idrogeno sembra diverso. Secondo la teoria della struttura dell'atomo di idrogeno secondo N. Bohr, un elemento ha un elettrone spaiato. L'atomo H accetta elettroni da atomi attivi di metalli alcalini o alcalino-terrosi. Pertanto, la sua configurazione elettronica diventa simile a una particella di un gas inerte di elio. L'unico strato di energia è ora completamente completato. In questi processi, la struttura dell'atomo di idrogeno cambia e cambia nella forma di anione. È per questo motivo che un elemento si trova contemporaneamente nella tavola periodica anche nel suo 7 ° gruppo.

Tutto in confronto
Continuando a studiare le caratteristiche strutturali delle particelle di idrogeno, vediamo come la loro struttura interna influisce sul comportamento di un elemento nelle reazioni. Per fare ciò, fai attenzione ai suoi vicini più prossimi nel sistema periodico e determina quale sia la struttura degli atomi di idrogeno, elio e litio. Con le particelle di un gas inerte, l'idrogeno combina la stessa quantità di livelli di energia, con il litio, una struttura simile dello strato di energia esterna, su cui si trova un elettrone. Tuttavia, le proprietà dell'idrogeno sono molto diverse sia dal gas inerte che dal metallo alcalino. Questo fatto dimostra che tutte le caratteristiche di un elemento chimico sono determinate dalla struttura della cavità dell'atomo e dalla molecola di idrogeno, cioè il numero di livelli di energia e la distribuzione di elettroni su di essi.
Dare vita all'acqua
Il nome dell'elemento indica che la combinazione dei suoi atomi con particelle di ossigeno porta all'emergere di una sostanza così unica e importante per la Terra, come l'acqua. In condizioni normali, questa reazione non si verifica, la temperatura di combustione della miscela di gas raggiunge 2800 ° C. In laboratorio, l'interazione tra H 2 e O 2 in un rapporto 2: 1 causa un'esplosione. La miscela stessa è chiamata gas detonante, e il processo che si svolge in esso, procede con un meccanismo di radicali liberi. Se non controllato, la reazione termina con un problema serio: una potente esplosione. Per questo motivo, nonostante la sua eccezionale leggerezza, l'idrogeno è stato abbandonato come riempitivo per aerei aviotrasportati. La triste causa fu il crollo del dirigibile di Hindenburg diretto in America nel 1937. Vediamo ora come la struttura dell'atomo di idrogeno influisce sulle caratteristiche fisiche di un gas.
Ad

Idrogeno, Deuterio, Trizio
Non essere sorpreso dall'elenco di termini sopra riportato. Si tratta dello stesso elemento chimico dell'idrogeno, la carica nucleare di un atomo è +1. Il secondo e il terzo nome sono i nomi degli isotopi. La ragione delle loro differenze sta nel numero di neutroni nel nucleo, mentre il numero di protoni di tutti e tre i tipi di particelle è lo stesso. Il deuterio ha due neutroni, il trizio ne ha 3 e l'idrogeno stesso ha 1 neutrone nel suo nucleo. L'acqua contenente deuterio nelle sue molecole è chiamata pesante. Può essere trovato negli stagni di raffreddamento delle centrali nucleari, così come nel citoplasma delle cellule che hanno alterato il normale metabolismo.
Struttura elettronica dell'atomo di idrogeno
Lo schema seguente ci aiuterà a comprendere il comportamento specifico di una sostanza semplice H 2 in varie interazioni chimiche.
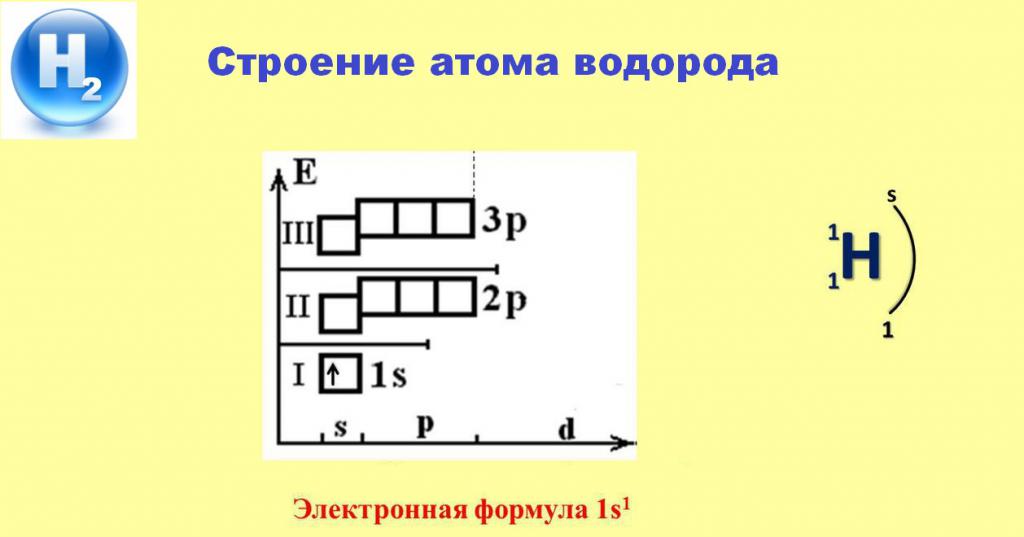
La presenza di un singolo elettrone che occupa l'orbitale s del primo livello di energia garantisce la costante valenza dell'idrogeno, pari a 1. Nella maggior parte dei casi, questo elettrone lascia lo spazio dell'atomo e assume più elementi elettronegativi. Solo le reazioni con i metalli consentono all'idrogeno di attingere un elettrone dagli atomi di elementi attivi alcalini o alcalino-terrosi nella sfera di influenza del proprio nucleo, formando composti cristallini bianchi - i loro idruri.
Attivo e aggressivo
L'idrogeno atomico, per così dire, è facile da sollevare. Altri agenti riducenti come il carbonio oi suoi ossidi possono invidiare la sua velocità nel ridurre i metalli dai loro ossidi. Gli atomi di H sono anche attivamente combinati con particelle di zolfo, ossigeno e fosforo. Un bruciatore di fiamma con idrogeno atomico dà un riscaldamento superiore a 4000 ° C. Per questo motivo, tali dispositivi sono facili da lavorare su superfici metalliche: tagliare o saldare.
Ad

L'idrogeno atomico è ben consolidato come agente riducente di metalli puri - tungsteno, molibdeno - dai loro minerali, rappresentati principalmente da ossidi. Quando incontra gli stessi atomi di se stesso, l'idrogeno forma una struttura stabile e passiva, una molecola. Entrambi gli atomi di H si attaccano l'un l'altro con l'aiuto di una coppia di elettroni comuni, essendo un modello di legame covalente stabile non polare. È durevole e garantisce la stabilità delle molecole di H 2 sia in condizioni terrestri che nello spazio. L'industria alimentare, in cui viene utilizzata per l'idrogenazione degli oli e la produzione di spread a basso contenuto calorico che sono di moda nella moderna dietetica, non è stata priva di idrogeno.

Nel nostro articolo abbiamo esaminato la struttura dell'atomo di idrogeno e abbiamo scoperto come influisce sulle proprietà di una sostanza semplice.