Come realizzare un'equazione di reazione chimica: una sequenza di azioni
Parliamo di come creare un'equazione di reazione chimica. È proprio questa domanda che causa serie difficoltà agli scolari. Alcuni non riescono a capire l'algoritmo per la compilazione di formule di prodotto, altri inseriscono erroneamente i coefficienti nell'equazione. Considerando che tutti i calcoli quantitativi sono eseguiti con precisione mediante equazioni, è importante capire l'algoritmo delle azioni. Proviamo a capire come recuperare le equazioni delle reazioni chimiche.
Formulazione di formule di valenza
Per registrare correttamente i processi che si verificano tra diverse sostanze, è necessario imparare come scrivere le formule. I composti binari tengono conto delle valenze di ciascun elemento. Ad esempio, nei metalli dei sottogruppi principali, corrisponde al numero del gruppo. Nel redigere la formula finale, il più piccolo multiplo viene determinato tra questi indicatori, quindi gli indici sono disposti.
Ad

Qual è l'equazione
Con questo si intende una registrazione simbolica che mostra gli elementi chimici interagenti, le loro relazioni quantitative, nonché quelle sostanze che si ottengono come risultato del processo. Uno dei compiti offerti agli studenti del nono grado nella certificazione chimica finale ha la seguente dicitura: "Formulare le equazioni di reazione che caratterizzano le proprietà chimiche della classe di sostanze proposta". Per far fronte all'attività, gli studenti devono avere un algoritmo di azione.
Algoritmo di azione
Ad esempio, è necessario scrivere il processo di bruciare il calcio, usando simboli, coefficienti, indici. Parliamo di come rendere l'equazione di una reazione chimica, usando la procedura. Nella parte sinistra dell'equazione, scriviamo nei segni "+" con i segni della sostanza che sono coinvolti in questa interazione. Poiché la combustione avviene con la partecipazione di ossigeno dell'aria, che appartiene alle molecole biatomiche, scriviamo la sua formula O2.
Ad
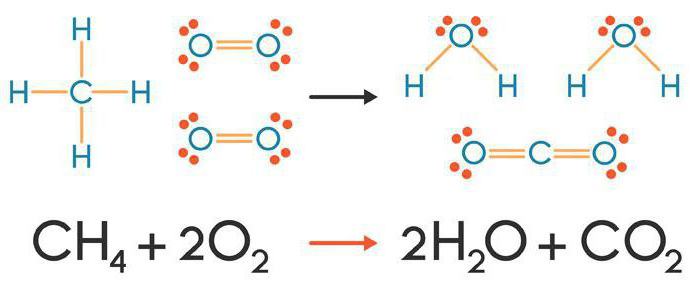
Seguendo il segno di uguale, formiamo la composizione del prodotto di reazione utilizzando le regole dell'accordo di valenza:
2Ca + O2 = 2CaO.
Continuare la conversazione su come creare un'equazione reazione chimica, Prendiamo atto della necessità di utilizzare la legge della costanza della composizione, nonché la conservazione della composizione delle sostanze. Consentono di eseguire il processo di regolazione, per disporre i coefficienti mancanti nell'equazione. Questo processo è uno degli esempi più semplici di interazioni che si verificano nella chimica inorganica.
Aspetti importanti
Per capire come recuperare l'equazione di una reazione chimica, prendiamo nota di alcune domande teoriche su questo argomento. Legge sulla conservazione di massa le sostanze, formulate da M. V. Lomonosov, spiegano la possibilità della distribuzione dei coefficienti. Poiché il numero di atomi di ciascun elemento prima e dopo l'interazione rimane invariato, è possibile eseguire calcoli matematici.

Quando si equalizzano i lati sinistro e destro dell'equazione, viene utilizzato il multiplo comune più piccolo, nello stesso modo in cui la formula composta viene formulata tenendo conto delle valenze di ciascun elemento.
Interazioni redox
Dopo che gli studenti avranno elaborato un algoritmo di azioni, saranno in grado di comporre un'equazione di reazioni che caratterizzano le proprietà chimiche delle sostanze semplici. Ora puoi procedere all'analisi di interazioni più complesse, come ad esempio il verificarsi di un cambiamento stati di ossidazione agli elementi:
Ad
Fe + CuSO4 = FeSO4 + Cu.
Esistono alcune regole in base alle quali gli stati di ossidazione sono fissati in sostanze semplici e complesse. Ad esempio, per le molecole biatomiche, questo indicatore è zero, nei composti complessi la somma di tutti gli stati di ossidazione dovrebbe essere pari a zero. Nella preparazione dell'equilibrio elettronico determinano gli atomi o gli ioni che donano elettroni (agente riducente), li assumono (ossidante).

Tra questi indicatori è determinato dal più piccolo multiplo, così come i coefficienti. La fase finale dell'analisi dell'interazione redox è la distribuzione dei coefficienti nello schema.
Equazioni ioniche
Una delle questioni importanti che viene considerata nel corso della chimica scolastica è l'interazione tra le soluzioni. Ad esempio, il compito è dato come segue: "Creare un'equazione per la reazione chimica dello scambio ionico tra cloruro di bario e solfato di sodio." Si tratta di scrivere un'equazione ionica molecolare, completa, abbreviata. Per considerare l'interazione a livello di ioni, è necessario indicarlo per ogni materiale di partenza, il prodotto di reazione dalla tabella di solubilità. Ad esempio:
BaCl2 + Na2SO4 = 2NaCl + BaSO4
Le sostanze che non si dissolvono in ioni sono registrate in forma molecolare. Lo scambio di ioni procede completamente in tre casi:
- formazione di sedimenti;
- rilascio di gas;
- produzione di una sostanza a bassa dissociazione, ad esempio acqua.

Se una sostanza ha un coefficiente stereochimico, viene presa in considerazione quando si scrive l'equazione ionica completa. Dopo che è stata scritta l'equazione ionica completa, viene eseguita la riduzione di quegli ioni che non erano legati in soluzione. Il risultato finale di qualsiasi compito che implichi la considerazione del processo che si verifica tra le soluzioni di sostanze complesse sarà una registrazione della reazione ionica ridotta.
conclusione
Le equazioni chimiche ci permettono di spiegare con l'aiuto di simboli, indici, coefficienti quei processi che si osservano tra le sostanze. A seconda del processo in corso, ci sono alcune sottigliezze di scrivere l'equazione. L'algoritmo generale per la compilazione di reazioni, discusso sopra, si basa sulla valenza, sulla legge di conservazione della massa di sostanze, sulla costanza della composizione.