Peso molecolare: principi di base della definizione
La massa molecolare è uno dei concetti base della chimica moderna. La sua introduzione è stata resa possibile dopo la convalida scientifica dell'affermazione di Avogadro secondo cui molte sostanze consistono in minuscole particelle - molecole, ognuna delle quali, a sua volta, è costituita da atomi. La scienza deve questo giudizio al chimico italiano Amadeo Avogadro, chi scientificamente provato struttura molecolare le sostanze e la chimica hanno dato molti concetti e leggi importanti.

Unità di massa di elementi
Inizialmente, l'atomo di idrogeno era considerato l'elemento più leggero nell'Universo come unità di base del peso atomico e molecolare. Ma la maggior parte delle masse atomiche sono state calcolate in base ai loro composti di ossigeno, quindi è stato deciso di scegliere un nuovo standard per determinare le masse atomiche. Si supponeva che la massa atomica dell'ossigeno fosse 15, la massa atomica della sostanza più leggera sulla Terra, l'idrogeno, era 1. Nel 1961, il sistema di ossigeno per determinare il peso era comune, ma creava alcuni inconvenienti.
Ad
Nel 1961 fu adottata una nuova scala. masse atomiche relative Il riferimento per cui era l'isotopo di carbonio 12 C. L'unità di massa atomica (Amu abbreviato) è 1/12 della massa di questo standard. Al momento, la massa atomica è la massa di un atomo, che dovrebbe essere espressa in amu.
Massa di molecole
La massa di una molecola di qualsiasi sostanza è uguale alla somma delle masse di tutti gli atomi che formano una data molecola. Il peso molecolare più leggero di un gas è in idrogeno, il suo composto è scritto come H 2 e ha un valore vicino a due. Una molecola d'acqua è composta da un atomo di ossigeno e due atomi di idrogeno. Ciò significa che il suo peso molecolare è 15.994 + 2 * 1.0079 = 18.0152 amu. I più grandi pesi molecolari hanno composti organici complessi - proteine e amminoacidi. La massa molecolare dell'unità strutturale proteica varia da 600 a 10 6 e superiore, a seconda del numero di catene peptidiche in questa struttura macromolecolare. 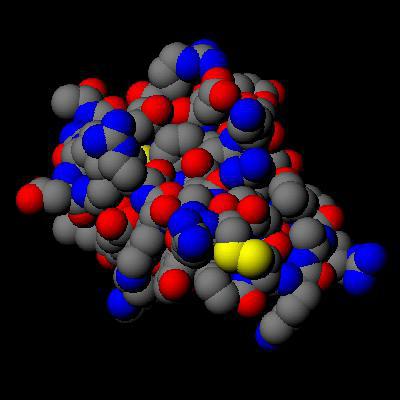
talpa
Allo stesso tempo con le unità standard di massa e volume, una unità di sistema molto speciale, la talpa, viene utilizzata in chimica.
Una talpa è la quantità di una sostanza che contiene tante unità strutturali (ioni, atomi, molecole, elettroni), tanto è contenuta in 12 grammi dell'isotopo 12 C.
Quando si applica la misura della quantità di una sostanza, è necessario indicare quali unità strutturali si intendono. Come segue dal concetto di "talpa", in ogni singolo caso, dovrebbe indicare con precisione a quali unità strutturali si fa riferimento - per esempio, la mole di ioni H + , la mole di molecole di H 2 e così via.
Ad
Peso molare e molecolare
La massa della sostanza in 1 mol è misurata in g / mol e viene chiamata massa molare. La relazione tra massa molecolare e molare può essere scritta come un'equazione.
ν = k × m / M, dove k è il coefficiente di proporzionalità.
È facile dire che per ogni rapporto il coefficiente di proporzionalità sarà uguale a uno. Infatti, l'isotopo di carbonio ha una massa molecolare relativa di 12 AU.m e, per definizione, la massa molare di questa sostanza è di 12 g / mol. Il rapporto tra peso molecolare e molare è 1. Quindi possiamo concludere che il peso molecolare e molare hanno gli stessi valori numerici.
Volumi di gas
Come sapete, tutte le sostanze che ci circondano possono essere in uno stato aggregativo solido, liquido o gassoso. Per i solidi, la misura base più comune è la massa, per i solidi e i liquidi, il volume. Ciò è dovuto al fatto che i solidi mantengono la loro forma e le dimensioni finali: le sostanze liquide e gassose non hanno dimensioni finite. Una caratteristica di ogni gas è che la distanza tra le sue unità strutturali - molecole, atomi, ioni - è molte volte maggiore delle stesse distanze nei liquidi o nei solidi. Ad esempio, una mole di acqua in condizioni normali occupa un volume di 18 ml - approssimativamente la stessa misura si adatta a un cucchiaio. Il volume di una mole di sale cristallino è di 58,5 ml, e il volume di 1 mole di zucchero è 20 volte più mole d'acqua. Più spazio è richiesto per i gas. Una mole di azoto in condizioni normali occupa un volume di 1.240 volte superiore a una mole di acqua. 
Pertanto, i volumi di sostanze gassose sono significativamente diversi dai volumi di liquido e solido. Ciò è dovuto alla differenza nelle distanze tra le molecole di sostanze in diversi stati di aggregazione.
Condizioni normali
Lo stato di qualsiasi gas dipende in larga misura dalla temperatura e dalla pressione. Ad esempio, l'azoto alla temperatura di 20 ° C occupa un volume di 24 litri e a 100 ° C alla stessa pressione - 30,6 litri. I chimici hanno preso in considerazione questa dipendenza, quindi è stato deciso di ridurre tutte le operazioni e le misurazioni con sostanze gassose in condizioni normali. In tutto il mondo, i parametri delle condizioni normali sono gli stessi. Per i prodotti chimici gassosi, questi sono:
Ad
- Temperatura a 0 ° C.
- Pressione di 101,3 kPa.
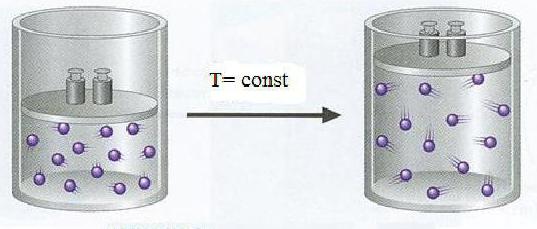
Per condizioni normali è accettata un'abbreviazione speciale - n. A volte questa designazione non è scritta nei compiti, quindi dovresti rileggere attentamente le condizioni del problema e riportare i parametri del gas in condizioni normali.
Calcola il volume di 1 mole di gas
Ad esempio, è facile calcolare una mole di qualsiasi gas, ad esempio l'azoto. Per fare ciò, devi prima trovare il valore del suo peso molecolare relativo:
M r (N 2 ) = 2 × 14 = 28.
Poiché la massa molecolare relativa di una sostanza è numericamente uguale a molare, M (N 2 ) = 28 g / mol.
È stato trovato sperimentalmente che in condizioni normali la densità di azoto è 1,25 g / litro.
Sostituiamo questo valore in una formula standard nota dal corso di fisica della scuola, in cui:
- V è il volume di gas;
- m è la massa di gas;
- ρ è la densità del gas.
Otteniamo che il volume molare di azoto in condizioni normali
V (N 2 ) = 25 g / mol: 1,25 g / litro = 22,4 l / mol.
Si scopre che una mole di azoto richiede 22,4 litri.
Se esegui un'operazione del genere con tutte le sostanze gassose esistenti, puoi giungere a una conclusione sorprendente: il volume di qualsiasi gas in condizioni normali è di 22,4 litri. Indipendentemente dal tipo di gas coinvolto, qual è la sua struttura e le sue caratteristiche fisico-chimiche, una mole di questo gas occuperà un volume di 22,4 litri.
Ad

Il volume molare di gas è una delle costanti più importanti in chimica. Questa costante consente di risolvere molti problemi chimici associati alla misurazione delle proprietà dei gas in condizioni normali.
risultati
Il peso molecolare delle sostanze gassose è importante per determinare la quantità di una sostanza. E se il ricercatore conosce la quantità di una sostanza di un gas, può determinare la massa o il volume di tale gas. Per la stessa porzione di sostanza gassosa le condizioni sono soddisfatte contemporaneamente:
ν = m / M ν = V / V m.
Se rimuoviamo la costante ν, possiamo equalizzare queste due espressioni:
m / M = V / V m.
In questo modo è possibile calcolare la massa di una porzione della sostanza e del suo volume e anche il peso molecolare noto della sostanza in esame. Usando questa formula, si può facilmente calcolare il rapporto volume / massa. Quando si cola questa formula nella forma M = m V m / V, la massa molare del composto desiderato sarà nota. Per calcolare questo valore, è sufficiente conoscere la massa e il volume del gas di prova.
Va ricordato che la stretta corrispondenza tra la massa molecolare reale della sostanza e quella trovata dalla formula è impossibile. Qualsiasi gas contiene una massa di impurità e additivi che apportano determinati cambiamenti nella sua struttura e influenzano la determinazione della sua massa. Ma queste fluttuazioni apportano modifiche nella terza o quarta cifra dopo il punto decimale nel risultato trovato. Pertanto, per problemi scolastici ed esperimenti, i risultati trovati sono abbastanza plausibili.