Elemento chimico radioattivo Elemento radioattivo artificiale
Fino alla fine del XIX secolo, tutti gli elementi chimici sembravano permanenti e indivisibili. Non c'era alcuna domanda su come convertire elementi immutabili. Ma la scoperta della radioattività ha capovolto il mondo a noi noto e ha spianato la strada alla scoperta di nuove sostanze.
Scoperta della radioattività
L'onore della scoperta della trasformazione degli elementi appartiene al fisico francese Antoine Becquerel. Per uno esperienza chimica lui aveva bisogno di cristalli solfato di potassio uranile. Ha avvolto la sostanza in carta nera e ha messo la borsa vicino al piatto fotografico. Dopo aver sviluppato il film, lo scienziato ha visto i contorni dei cristalli di uranile nella foto. Nonostante lo spesso strato di carta, erano chiaramente distinguibili. Becquerel ripeté questo esperimento più volte, ma il risultato fu lo stesso: i contorni dei cristalli contenenti uranio erano chiaramente visibili sulle lastre fotografiche.
Ad
I risultati della scoperta Becquerel annunciarono nel corso del prossimo incontro, che si tenne all'Accademia delle scienze di Parigi. Il suo rapporto iniziò con le parole "radiazione invisibile". Così ha descritto i risultati dei suoi esperimenti. Dopo di ciò, il concetto di radiazione è entrato in uso dai fisici.
Esperimenti Curie
I risultati delle osservazioni di Becquerel interessarono gli scienziati francesi Marie e Paul Curie. Giustamente hanno considerato che non solo l'uranio potrebbe avere proprietà radioattive. I ricercatori hanno notato che i residui di minerale da cui viene estratta questa sostanza sono ancora altamente radioattivi. La ricerca di elementi diversi da quelli iniziali ha portato alla scoperta di una sostanza con proprietà simili all'uranio. Un nuovo elemento radioattivo ha ricevuto il nome di polonio. Tale nome Marie Curie ha dato la sostanza in onore della loro patria - la Polonia. In seguito fu scoperto il radio. L'elemento radioattivo era il prodotto del decadimento dell'uranio puro. Dopo di ciò, un'era di novità, non precedentemente incontrata in natura, è iniziata in chimica. prodotti chimici.
Ad
elementi
La maggior parte dei nuclei attualmente conosciuti di elementi chimici è instabile. Nel corso del tempo, tali composti si disgregano spontaneamente in altri elementi e in varie minuscole particelle. L'elemento genitore più pesante nella comunità dei fisici è chiamato il materiale sorgente. I prodotti formati durante la decomposizione di una sostanza sono indicati come bambini o prodotti di decomposizione. Il processo stesso è accompagnato dal rilascio di varie particelle radioattive.
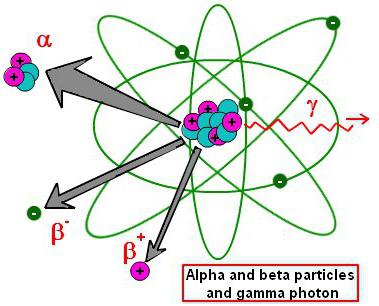
isotopi
L'instabilità degli elementi chimici può essere spiegata dall'esistenza di diversi isotopi della stessa sostanza. Gli isotopi sono variazioni di alcuni elementi del sistema periodico con le stesse proprietà, ma con un diverso numero di neutroni nel nucleo. Molte sostanze chimiche ordinarie hanno almeno un isotopo. Il fatto che questi elementi siano ampiamente distribuiti e ben studiati conferma che essi sono in uno stato stabile per un tempo arbitrariamente lungo. Ma ognuno di questi elementi "longevi" contiene isotopi. I loro scienziati producono nuclei nel corso delle reazioni di laboratorio. Un elemento radioattivo artificiale prodotto da mezzi sintetici non può esistere per lungo tempo in uno stato stabile e decade nel tempo. Questo processo può andare in tre modi. Con il nome di particelle elementari, che sono sottoprodotti di una reazione termonucleare, tutti e tre i tipi di decadimento hanno il loro nome.
Ad
Decadimento alfa
L'elemento chimico radioattivo può essere trasformato secondo il primo schema di decadimento. In questo caso, una particella alfa, la cui energia raggiunge i 6 milioni di eV, viene espulsa dal nucleo. Uno studio dettagliato dei risultati della reazione, è stato trovato che questa particella è un atomo di elio. Prende due protoni dal nucleo, quindi l'elemento radioattivo risultante avrà un numero atomico nel sistema periodico di due posizioni inferiore a quello della sostanza madre.
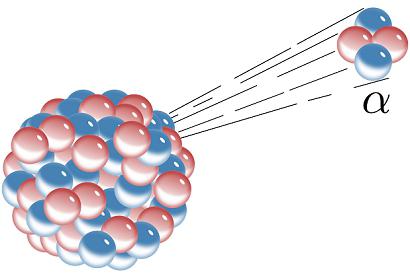
Decadimento beta
La reazione di decadimento beta è accompagnata dall'emissione di un elettrone dal nucleo. L'aspetto di questa particella in un atomo è associato al decadimento di un neurone in un elettrone, un protone e un neutrino. Quando l'elettrone lascia il nucleo, l'elemento chimico radioattivo aumenta il suo numero atomico di un'unità e diventa più pesante del suo genitore.
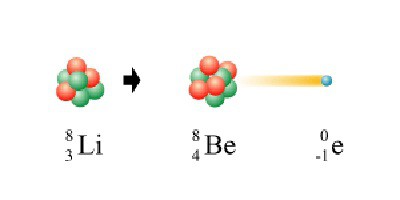
Decadimento gamma
Con il decadimento gamma, il nucleo emette un fascio di fotoni con energie diverse. Questi raggi sono chiamati radiazioni gamma. In questo processo, l'elemento radioattivo non viene modificato. Perde solo la sua energia.
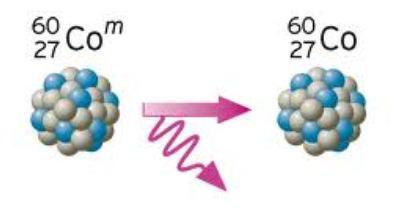
Di per sé, l'instabilità che un elemento radioattivo possiede non significa affatto che con una certa quantità di isotopi la nostra sostanza scompaia improvvisamente, rilasciando un'enorme energia. In realtà, la disintegrazione del nucleo assomiglia alla cottura dei popcorn - il movimento caotico dei chicchi di mais in una padella, ed è completamente sconosciuto quale di essi verrà rivelato per primo. La legge della reazione di decadimento radioattivo può garantire solo che per un certo periodo di tempo il numero di particelle, proporzionale al numero di nucleoni rimasti nel nucleo, volerà fuori dal nucleo. Nel linguaggio della matematica, questo processo può essere descritto dalla seguente formula:
Ad
dN = λNdt.
Qui sulla faccia è la dipendenza proporzionale del numero di nucleoni dN che lascia il nucleo per il periodo dt, sul numero di tutti i nucleoni N. nel nucleo. Il coefficiente λ è la costante di radioattività della sostanza in decomposizione.
Il numero di nucleoni rimasti nel nucleo al tempo t è descritto dalla formula:
N = N 0 e -λt ,
in cui N 0 è il numero di nucleoni nel nucleo all'inizio dell'osservazione.
Ad esempio, l'elemento alogeno radioattivo con numero atomico 85 è stato scoperto solo nel 1940. La sua emivita è piuttosto lunga - 7,2 ore. Il contenuto di alogeno radioattivo (astato) sull'intero pianeta non supera un grammo di sostanza pura. Quindi, in 3,1 ore, la sua quantità in natura dovrebbe, in teoria, essere dimezzata. Ma i processi costanti di decadimento dell'uranio e del torio danno origine a nuovi e nuovi atomi di astato, anche se in dosi molto piccole. Pertanto, la sua quantità in natura rimane stabile.
Mezza vita
La costante di radioattività serve a determinare con il suo aiuto quanto velocemente decadrà l'elemento in studio. Ma per problemi pratici, i fisici usano spesso una quantità chiamata emivita. Questo indicatore indica per quanto tempo la sostanza perderà esattamente la metà dei suoi nucleoni. Per diversi isotopi, questo periodo varia da piccole frazioni di secondo a miliardi di anni.
Ad
È importante capire che il tempo in questa equazione non si somma, ma si moltiplica. Ad esempio, se durante un periodo di tempo t una sostanza perde metà dei suoi nucleoni, allora per un periodo di 2 t perderà un'altra metà del resto - cioè un quarto del numero originale di nucleoni.
L'emergere di elementi radioattivi
Naturalmente, le sostanze radioattive si formano nell'atmosfera superiore della Terra, nella ionosfera. Sotto l'azione della radiazione cosmica, il gas ad alta quota subisce vari cambiamenti che trasformano una sostanza stabile in un elemento radioattivo. Il gas più comune nella nostra atmosfera è N 2 , ad esempio, da un isotopo stabile, l'azoto-14 viene convertito in un isotopo radioattivo di carbonio-14.
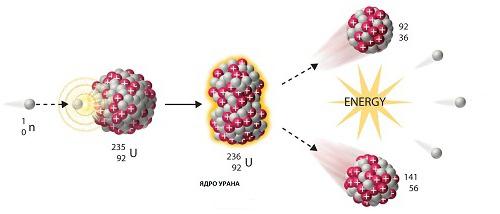
Oggigiorno, molto più spesso un elemento radioattivo sorge nella catena delle reazioni artificiali della fissione atomica. Questo è il nome del processo in cui il nucleo di una sostanza madre si scompone in due filiali e poi in quattro nipoti radioattivi. Un classico esempio è l'isotopo dell'uranio 238. La sua emivita è di 4,5 miliardi di anni. Quasi il nostro pianeta esiste. Dopo dieci fasi di decadimento, l'uranio radioattivo viene trasformato in piombo stabile 206. L'elemento radioattivo ottenuto artificialmente non è diverso nelle sue proprietà dalla sua controparte naturale.
Il significato pratico della radioattività
Dopo il disastro di Chernobyl, molti hanno seriamente parlato di frenare i programmi di sviluppo. centrali nucleari. Ma in termini domestici, la radioattività porta enormi benefici all'umanità. Lo studio delle possibilità della sua applicazione pratica è impegnato nella scienza della radiografia. Ad esempio, il fosforo radioattivo viene somministrato a un paziente per ottenere un quadro completo delle fratture ossee. L'energia nucleare serve anche a generare calore ed elettricità. Forse in futuro stiamo aspettando nuove scoperte in questo incredibile campo della scienza.