La formula generale delle ammine. Proprietà e struttura delle ammine
Basi organiche: questo nome viene spesso utilizzato in chimica per composti derivati dall'ammoniaca. Gli atomi di idrogeno nella sua molecola sono sostituiti da radicali di idrocarburi. Stiamo parlando di ammine - composti che ripetono le proprietà chimiche dell'ammoniaca. Nel nostro articolo faremo conoscenza con la formula generale delle ammine e le loro proprietà.
Struttura molecolare
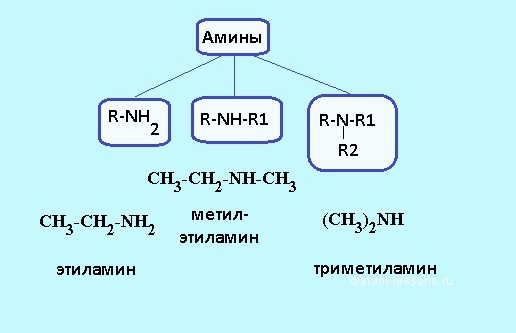
A seconda di quanti atomi di idrogeno vengono sostituiti da radicali di idrocarburi, si distinguono le ammine primarie, secondarie e terziarie. Ad esempio, la metilammina è l'ammina primaria in cui la particella di idrogeno è stata sostituita dal gruppo -CH 3 . La formula strutturale delle ammine è R-NH 2 , può essere usata per determinare la composizione della sostanza organica. Un esempio di un'ammina secondaria può essere dimetilammina, che ha la seguente forma: NH 2 -NH-NH 2 . In molecole di composti terziari, tutti e tre gli atomi di idrogeno di ammoniaca sono sostituiti da radicali di idrocarburi, per esempio, trimetilammina ha la formula (NH 2 ) 3 N. La struttura delle ammine influisce sulle loro proprietà fisiche e chimiche.
Caratteristica fisica
Lo stato aggregato di ammine dipende da cosa massa molare radicali. Più piccolo è, più basso è il peso specifico della sostanza. Le ammine di classe inferiore sono rappresentate da gas (ad esempio metilammina). Hanno un odore di ammoniaca pronunciato. Le ammine medie sono liquidi dall'odore lieve e i composti con una grande massa di radicali di idrocarburi sono solidi inodori. La solubilità delle ammine dipende anche dalla massa del radicale: più è grande, più la sostanza si dissolve in acqua. Pertanto, la struttura delle ammine determina il loro stato fisico e le loro caratteristiche.
Proprietà chimiche
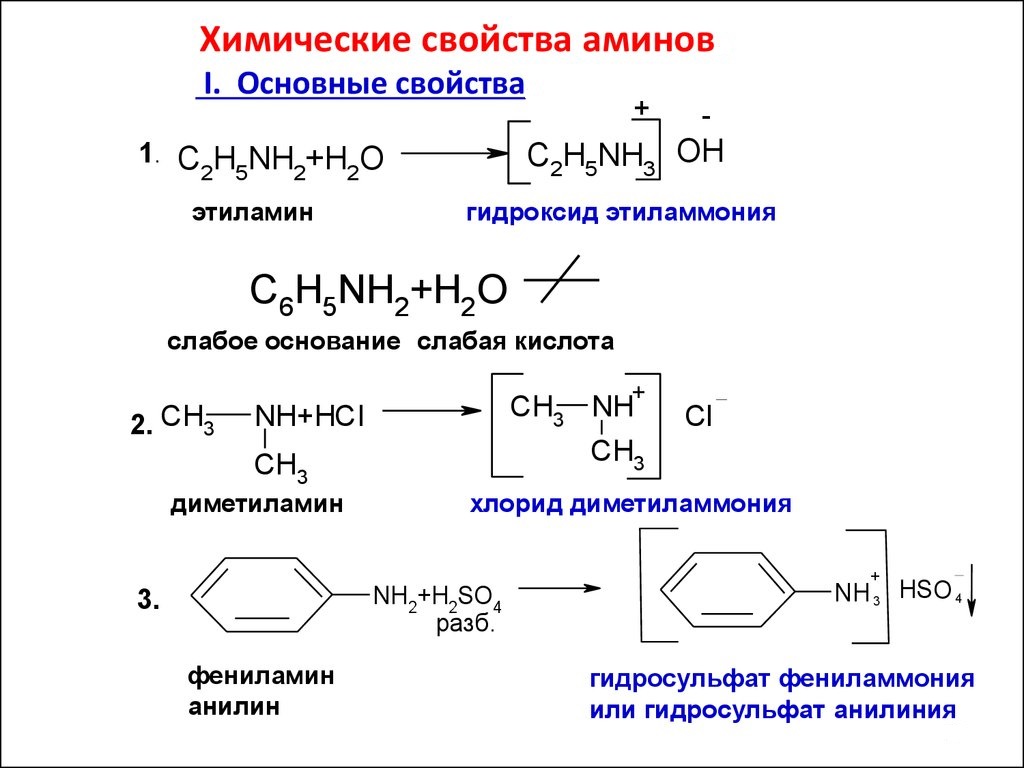
La caratteristica delle sostanze dipende principalmente dalle trasformazioni del gruppo amminico, in cui il ruolo principale è assegnato alla sua coppia di elettroni solitaria. Così come materia organica le ammine classiche sono derivati dell'ammoniaca, sono capaci di reazioni caratteristiche di NH 3 . Ad esempio, i composti si dissolvono in acqua. I prodotti di questa reazione saranno sostanze che mostrano le proprietà degli idrossidi. Ad esempio, la metilammina, la cui composizione atomica obbedisce alla formula generale delle ammine saturi R - NH 2 , forma un composto con acqua - idrossido di metilammonio:
CH 3 - NH 2 + H 2 O = [CH 3 - NH 3 ] OH
Le basi organiche interagiscono con gli acidi inorganici e il sale viene rilevato nei prodotti. Pertanto, la metilammina con acido cloridrico dà cloruro di ammonio metilico:
CH 3 -NH 2 + HCl -> [CH 3 NH 3 ] Cl
Reazioni di ammine, la cui formula generale è R-NH 2 , con acidi organici sono sostituiti sostituendo l'atomo di idrogeno del gruppo amminico con un anione complesso del residuo acido. Sono chiamate reazioni di alchilazione. Come nella reazione con l'acido nitrico, gli acil derivati possono formare solo ammine primarie e secondarie. Trimetilammina e altre ammine terziarie non sono in grado di tali interazioni. Inoltre, aggiungiamo che l'alchilazione nella chimica analitica viene utilizzata per separare le miscele di ammine, ma serve anche risposta qualitativa su ammine primarie e secondarie. Tra le ammine cicliche, l'anilina è importante. Viene estratto dal nitrobenzene mediante riduzione di quest'ultimo con idrogeno in presenza di un catalizzatore. L'anilina è una materia prima per la produzione di materie plastiche, coloranti, esplosivi e droghe.

Caratteristiche delle ammine terziarie
I derivati dell'ammoniaca terziaria differiscono nelle loro proprietà chimiche da composti mono o bi-sostituiti. Ad esempio, possono interagire con i derivati alogeni degli idrocarburi saturi. Di conseguenza, si formano sali di tetraalchilammonio. L'ossido d'argento reagisce con le ammine terziarie, mentre le ammine vengono convertite in idrossidi di tetraalchilammonio, che sono basi forti. Si possono formare acidi aprotici, come il trifluoruro di boro, con trimetilammina composti complessi.
Test qualitativo per ammine primarie
L'acido nitroso può fungere da reagente con cui rilevare ammine a uno o due sostituzioni. Poiché non esiste nello stato libero, per ottenerlo in soluzione, eseguire prima una reazione tra acido cloridrico diluito e nitrito di sodio. Quindi aggiungere l'ammina primaria disciolta. La composizione delle sue molecole può essere espressa usando la formula generale delle ammine: R-NH 2. Questo processo è accompagnato dalla comparsa di molecole di idrocarburi insaturi, che può essere determinata dalla reazione con acqua di bromo o da una soluzione di permanganato di potassio. La reazione isonitrilica può essere considerata qualitativa. In esso, le ammine primarie interagiscono con il cloroformio in un mezzo con un'eccessiva concentrazione di anioni idrossili. Il risultato è la formazione di isonitrili con un odore sgradevole specifico.

Caratteristiche della reazione delle ammine secondarie con acido nitrito
La tecnologia per produrre il reagente HNO 2 è descritta da noi sopra. Quindi un derivato ammonico organico contenente due radicali idrocarburici, ad esempio la dietilammina, la cui molecola corrisponde alla formula generale di ammine secondarie NH 2 -R-NH 2 , viene aggiunta alla soluzione contenente il reagente. Nei prodotti di reazione troviamo il composto nitro: N-nitrosodietilammina. Se si agisce con acido cloridrico, il composto viene decomposto nel sale cloruro dell'ammina iniziale e del nitrosil cloruro. Aggiungiamo anche che le ammine terziarie non sono in grado di reazioni con acido nitroso. Ciò è spiegato dal fatto seguente: l'acido nitrito appartiene agli acidi deboli e i suoi sali, quando interagiscono con ammine contenenti tre radicali idrocarburici, sono completamente idrolizzati in soluzioni acquose.
Modi per ottenere
Le ammine, la cui formula generale è R-NH 2 , possono essere ottenute mediante riduzione di composti contenenti azoto. Ad esempio, questa può essere la riduzione dei nitroalcani in presenza di un catalizzatore - nichel metallico - quando riscaldata a +50 ° C e a pressioni fino a 100 atm. Nitroetano, nitropropano o nitrometano vengono convertiti in ammine come risultato di questo processo. Le sostanze di questa classe possono anche essere ottenute riducendo l'idrogeno dei composti del gruppo nitrile. Questa reazione avviene in solventi organici, con la presenza di un catalizzatore di nichel. Se il sodio metallico viene utilizzato come agente riducente, in questo caso il processo viene eseguito in una soluzione alcolica. Citiamo come esempi altri due metodi: l'amminazione di alogenoalcani e alcoli.
Nel primo caso, si forma una miscela di ammine. L'amminazione degli alcoli viene effettuata come segue: una miscela di metanolo o vapori di etanolo con ammoniaca viene fatta passare attraverso l'ossido di calcio, che funge da catalizzatore. Le ammine primarie, secondarie e terziarie risultanti possono di solito essere separate per distillazione.
Nel nostro articolo, abbiamo studiato la struttura e le proprietà dei composti organici contenenti azoto - ammine.