L'agente ossidante è un atomo che accetta l'elettrone.
L'agente ossidante e l'agente riducente sono utilizzati per formulare la reazione in chimica organica e inorganica. Considerare le principali caratteristiche di tali interazioni, identifichiamo l'algoritmo per la compilazione dell'equazione e la disposizione dei coefficienti.

definire
Un ossidante è un atomo o uno ione che, interagendo con altri elementi, accetta elettroni. Il processo di produzione degli elettroni è chiamato riduzione ed è associato ad una diminuzione del grado di ossidazione.
Nel corso chimica inorganica Vengono considerati i due metodi principali di impostazione del coefficiente. L'agente riducente e l'agente ossidante nelle reazioni sono determinati dalla produzione dell'equilibrio di elettroni o dal mezzo metodo di reazione. Ci soffermeremo sul primo metodo di posizionamento dei coefficienti in OVR.
Ad
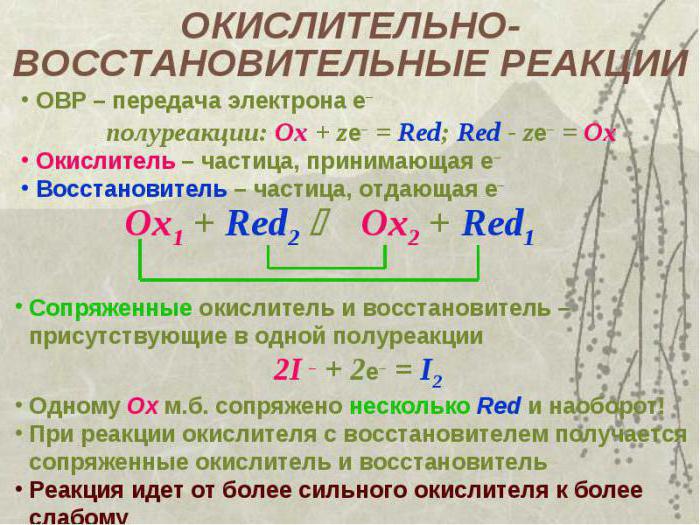
Stati di ossidazione
Prima di determinare l'ossidante nella reazione, è necessario posizionarlo stati di ossidazione tutti gli elementi nelle sostanze coinvolte nella trasformazione. Rappresenta la carica di un atomo di un elemento calcolato secondo certe regole. Nelle sostanze complesse, la somma di tutti gli stati di ossidazione positivi e negativi dovrebbe essere zero. Per i metalli dei sottogruppi principali, corrisponde alla valenza e ha un valore positivo.
Per i non metalli, che si trovano nella formula alla fine, il grado è determinato sottraendo il numero del gruppo da otto e ha un valore negativo.
Per sostanze semplici, è uguale a zero, poiché non vi è alcun processo di accettazione o rilascio di elettroni.
Per composti complessi costituiti da diversi elementi chimici, vengono utilizzati calcoli matematici per determinare i gradi di ossidazione.
Quindi, l'ossidante è un atomo, che nel processo di interazione abbassa il suo stato di ossidazione, e l'agente riducente, al contrario, aumenta il suo valore.
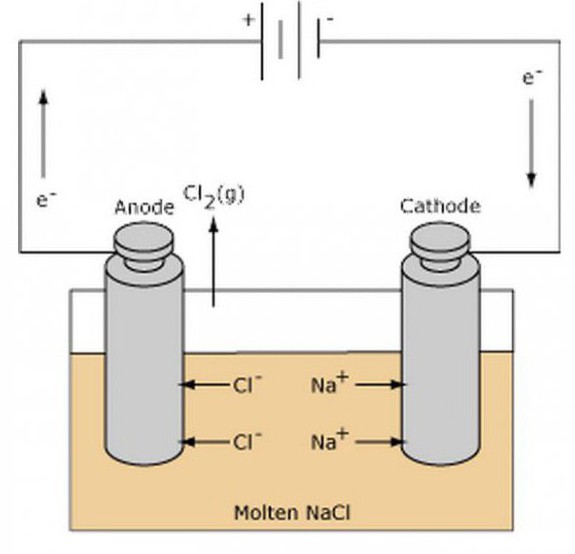
Esempi iad
La caratteristica principale dei compiti relativi alla distribuzione dei coefficienti nelle reazioni redox è la definizione delle sostanze mancanti e la formulazione delle loro formule. Un agente ossidante è un elemento che accetterà gli elettroni, ma in aggiunta ad esso, un agente riducente che li dà via deve partecipare alla reazione.
Ad
Diamo un algoritmo generalizzato con il quale è possibile eseguire le attività offerte ai diplomati delle scuole superiori in un unico esame di stato. Considera alcuni esempi specifici per capire che l'ossidante non è solo un elemento in una sostanza complessa, ma anche una sostanza semplice.
Innanzitutto, è necessario disporre i valori degli stati di ossidazione per ciascun elemento utilizzando determinate regole.
Successivamente, è necessario analizzare gli elementi che non hanno partecipato alla formazione di sostanze e creare una formula per loro. Dopo aver eliminato tutti gli spazi vuoti, è possibile procedere al processo di elaborazione dell'equilibrio elettronico tra l'agente ossidante e l'agente riducente. I coefficienti risultanti vengono inseriti nell'equazione, se necessario, aggiungendoli a quelle sostanze che non sono incluse nel bilancio.
Ad esempio, utilizzando il metodo di bilancia elettronica, è necessario completare l'equazione proposta, inserire i coefficienti necessari prima delle formule.
H 2 O 2 + H 2 SO 4 + KMnO 4 = MnSO 4 + O 2 + ... + ...
Per cominciare, determineremo i valori degli stati di ossidazione, otterremo
+K + Mn +7 O 4 -2 = Mn +2 S +6 O 4 -2 + O 2 0 + …+… H 2+ O 2 - + H 2+ S +6 O 4 -2 + K + Mn +7 O 4 -2 = Mn + 2 S +6 O 4 -2 + O 2 0 + ... + ...
Nello schema proposto, variano in ossigeno, e anche in manganese in permanganato di potassio. Quindi, l'agente riducente e l'agente ossidante sono trovati da noi. Nella parte destra non c'è sostanza in cui ci sarebbe il potassio, quindi, invece di omissioni, formiamo la formula del suo solfato.
Ad
Successivamente, scriviamo il saldo elettronico. L'ossigeno in questo caso mostrerà proprietà riducenti, rinunciando a due elettroni. Il manganese li prende, mostrando una capacità ossidante.
Il passo finale in questo compito è impostare i coefficienti.
5H 2 O 2 + 3H 2 SO 4 + 2KMnO 4 = 2Mn SO 4 + 5O 2 + 8H 2 O + K 2 SO 4
Acidi, permanganato di potassio, perossido di idrogeno. Tutti i metalli mostrano proprietà riducenti, trasformandosi in reazioni in cationi con carica positiva.
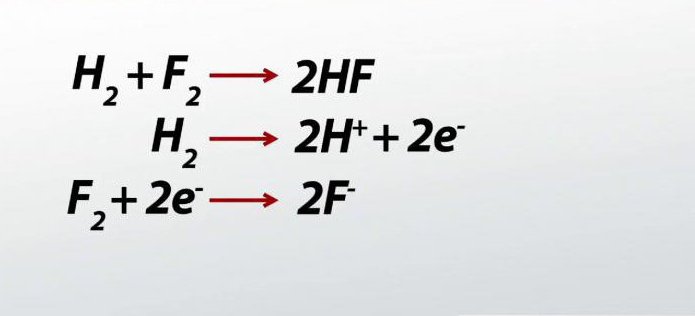
conclusione
I processi relativi all'accettazione e al rilascio di elettroni negativi si verificano non solo nella chimica inorganica. Il metabolismo, che viene effettuato negli organismi viventi, è una chiara variante del decorso delle reazioni redox in chimica organica. Ciò conferma l'importanza dei processi considerati, la loro rilevanza per la natura animata e inanimata.