La formula strutturale del nitrobenzene
I composti nitro sono indispensabili nella sintesi di vari coloranti azoici e nella fabbricazione di prodotti pirotecnici ed esplosivi. In particolare, il nitrobenzene, la cui formula è riportata di seguito, viene utilizzato come reagente principale nella maggior parte delle industrie simili, poiché le caratteristiche della sua natura chimica determinano l'importanza dell'utilizzo di questo semplice rappresentante dei nitroareni.
Struttura di connessione
In chimica, la formula del nitrobenzene è rappresentata come un anello aromatico a cui è attaccato un gruppo nitro, che ha pronunciate proprietà elettrocettore. Lo ione nitronico NO 2 + priva il composto della capacità di ulteriore sostituzione elettrofila. Questo sostituente degrada la densità elettronica dell'anello aromatico nella formula strutturale del nitrobenzene a se stesso (esempio 1), rendendolo quindi poco reattivo a qualsiasi reazione simile, inclusa la sintesi di Friedel-Crafts.
Ad
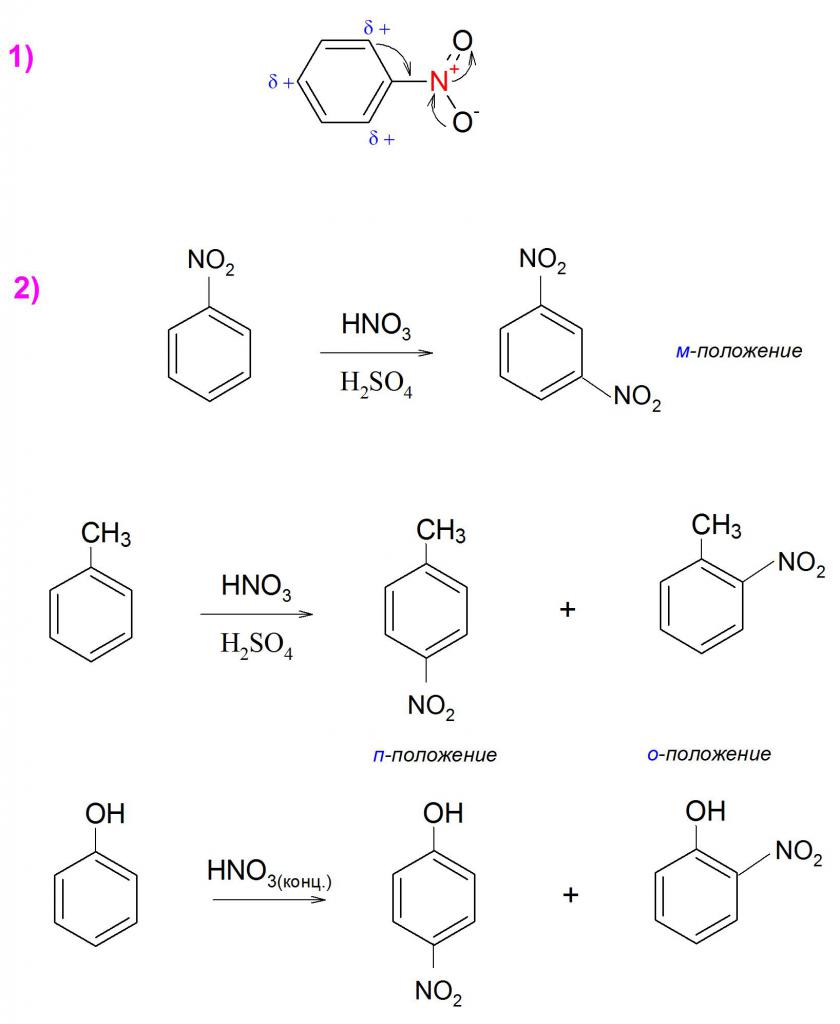
Questa caratteristica si esprime anche nell'incapacità di polinizzare facilmente tali composti, quindi, per la produzione diretta di dinitro e trinitrobenzeni sono necessarie condizioni piuttosto dirette e agenti aggiuntivi, come alte temperature o catalizzatori. Tuttavia, la presenza di eventuali sostituenti donatori di elettroni nella molecola, come il gruppo metilico o idrossi, facilita non solo le reazioni di addizione, ma facilita anche una sostituzione nucleofila più semplice. Questa caratteristica spiega tutta la stessa densità ottyagirovaniana dell'anello, solo in questo caso è distribuita tra gli orientanti in base alla forza dei loro effetti induttivi e mesomerici.
Funzionalità Vice
Poiché -NO 2 è un secondo tipo di orientante, il suo effetto disattivante sull'anello aromatico porta alla definizione di sostituenti, principalmente nella posizione meta. Ma quando si ottengono nitroderivati, ad esempio toluene o fenolo, -NO 2 diventa in posizione orto o para, poiché questi sostituenti determinano il posto del gruppo nitro nel composto (esempio 2) aggiungendo densità elettronica (effetto mesomerico). In parole povere, la presenza di orientanti di prima classe regola l'impostazione di -NO 2 nella formula chimica del nitrobenzene è più forte della presenza di gruppi del secondo tipo.
Ad
Ottenere nitrobenzene
L'ottenimento di questa sostanza nell'industria avviene mediante nitrazione diretta del benzene con una miscela di acidi solforici (H 2 SO 4 ) e nitrici (HNO 3 ) con una resa dal 96 al 99% (esempio 3). Raramente in condizioni di laboratorio, la formula del nitrobenzene viene sintetizzata sostituendo o modificando i gruppi esistenti, poiché la resa in tali reazioni è molto bassa e il processo stesso richiede condizioni speciali.
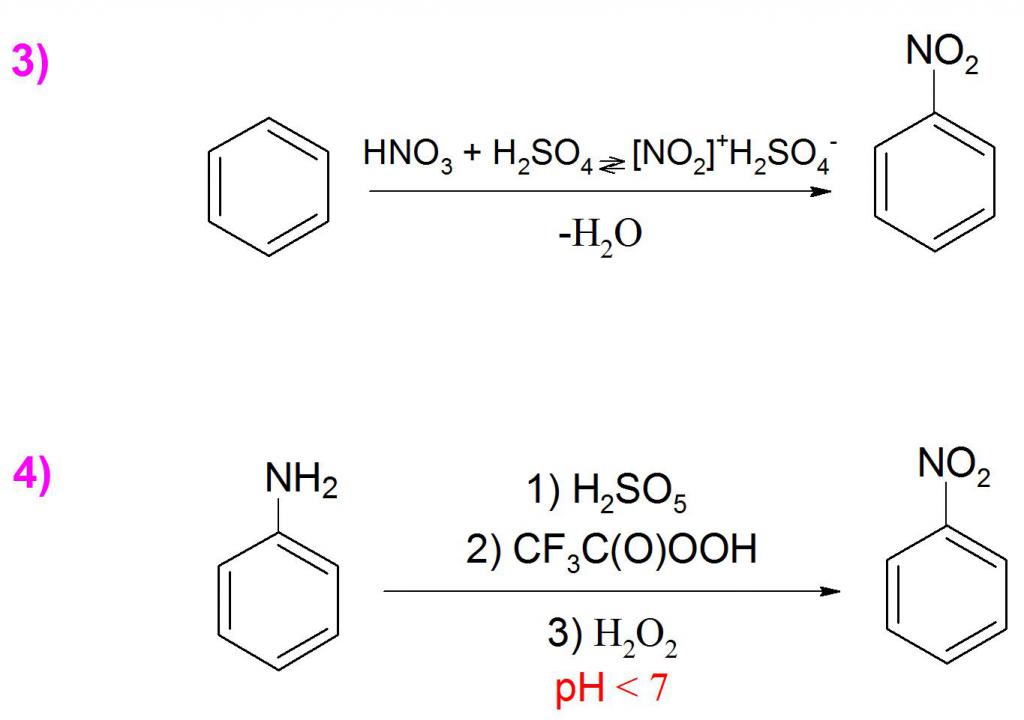
Un altro metodo di produzione è l'ossidazione di anilina da composti perossidici, ad esempio acido perossisolfurico (H 2 SO 5 ) o acido perossitrifluoroacetico (CF 3 C (O) OOH), e anche perossido di idrogeno (H 2 O 2 ). Questa reazione richiede il monitoraggio del pH del mezzo, dal momento che nel mezzo alcalino si forma prevalentemente azoxybenzene (Esempio 4).
Proprietà fisiche
Il nitrobenzene è un liquido oleoso, insolubile in acqua, con un odore specifico di mandorle amare e molto tossico per l'uomo. Tuttavia, è altamente solubile in solventi organici come benzene e dietil etere. Nel caso della preparazione diretta dal benzene, viene separato dalla miscela non reagita mediante distillazione a vapore.
Ad
Interazione con reagenti elettrofili
Come menzionato sopra, la presenza di un gruppo nitro nella composizione della formula di nitrobenzene rende il composto meno reattivo alla sostituzione elettrofila, ma il processo di ulteriore nitrazione può ancora avvenire sotto l'azione di acidi forti e alte temperature.
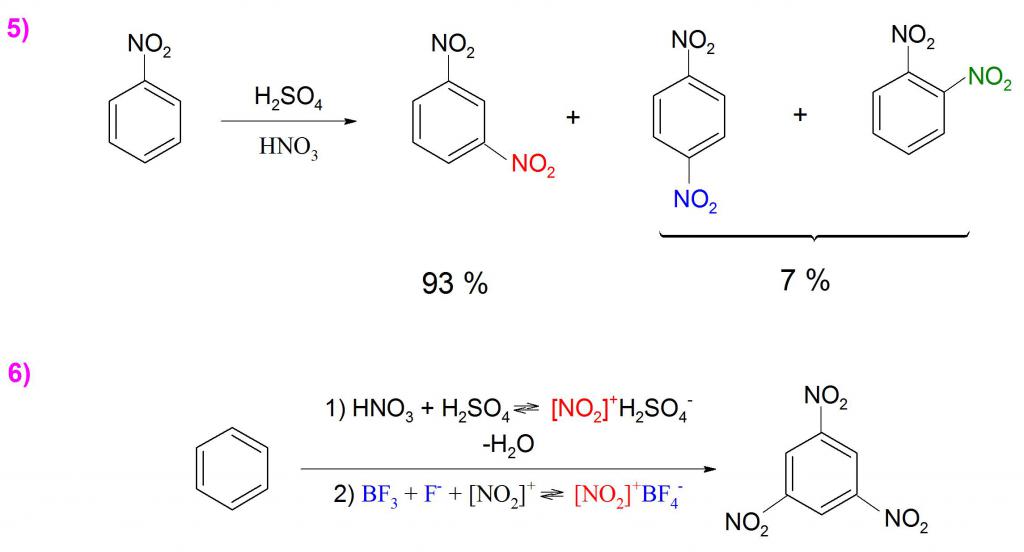
Per ottenere il dinitrobenzene, oltre all'utilizzo di una miscela di nitrati (H 2 SO 4 + HNO 3 ), è necessario un notevole effetto termico, ma il processo è molto difficile e di conseguenza si forma una miscela di una grande quantità del composto metanitrico e frazioni insignificanti di orto e para derivati (Esempio 5) ).
Il trinitrobenzene non è formato dalla nitrazione diretta, tuttavia, usando il trifluoruro di boro (BF 3 ) e le miscele di H 2 SO 4 concentrato e HNO 3, si ottiene con una resa piuttosto buona (Esempio 6).
Sostituzione nucleofila
Secondo la formula del nitrobenzene, si può giudicare che di per sé ha proprietà accettabili deboli, quindi può interagire solo con sostanze elettron donatrici molto forti. Più spesso, i reagenti agiscono sul gruppo nitro per formare composti azoici e azo, tuttavia, selezionando gli agenti ossidanti corretti, è possibile ottenere una piccola resa di derivati fenolici. Un esempio è la sintesi degli isomeri del nitrofenolo mediante l'introduzione diretta di un gruppo idrossile in un anello aromatico (Esempio 7). Tali reazioni avvengono lentamente e richiedono condizioni molto dure.
Ad
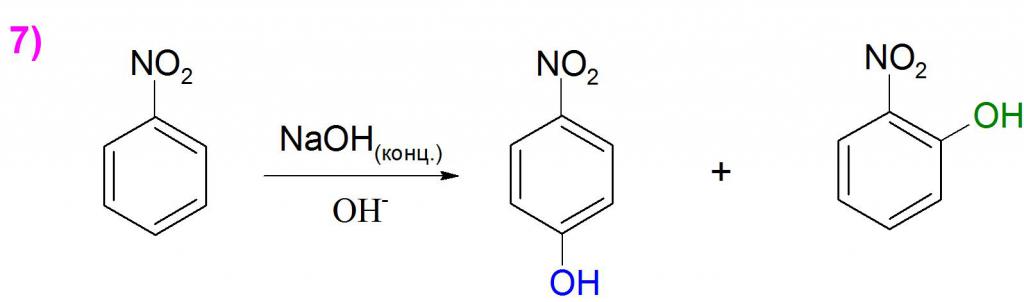
All'aumentare del numero di gruppi nitro, tali composti mostrano proprietà dell'accettore molto più forti, il che facilita la reazione con reagenti nucleofili e basici deboli.
Il ruolo della struttura del nitrobenzene nella produzione di ammine primarie
Il gruppo nitro è un sostituente che può essere ridotto a una varietà di prodotti in ambienti acidi, neutri e alcalini. L'intero processo di ripristino della formula strutturale del nitrobenzene nell'ammina primaria può essere rappresentato come un processo a più stadi.
Prima di tutto, con l'aggiunta di 2 atomi di idrogeno, si forma il nitrosobenzene, che è difficile da isolare nella sua forma pura (Fig. 1A).
La fase successiva di recupero consiste nell'ottenere l'arilidrossilamina, che in un mezzo acido (pH <6) si trasforma facilmente in anilina (figura 1B). È anche possibile che un riarrangiamento secondario di questo composto intermedio si verifichi negli amminofenoli (Figura 1B). Nella sua forma pura, l'arilidrossilamina si ottiene regolando i valori del pH in valori neutri.
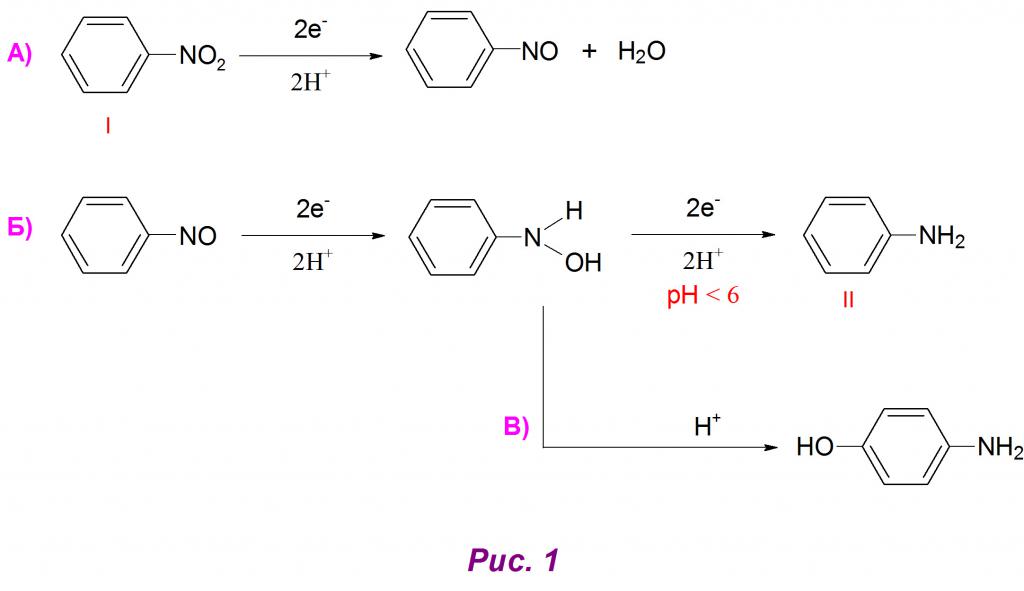
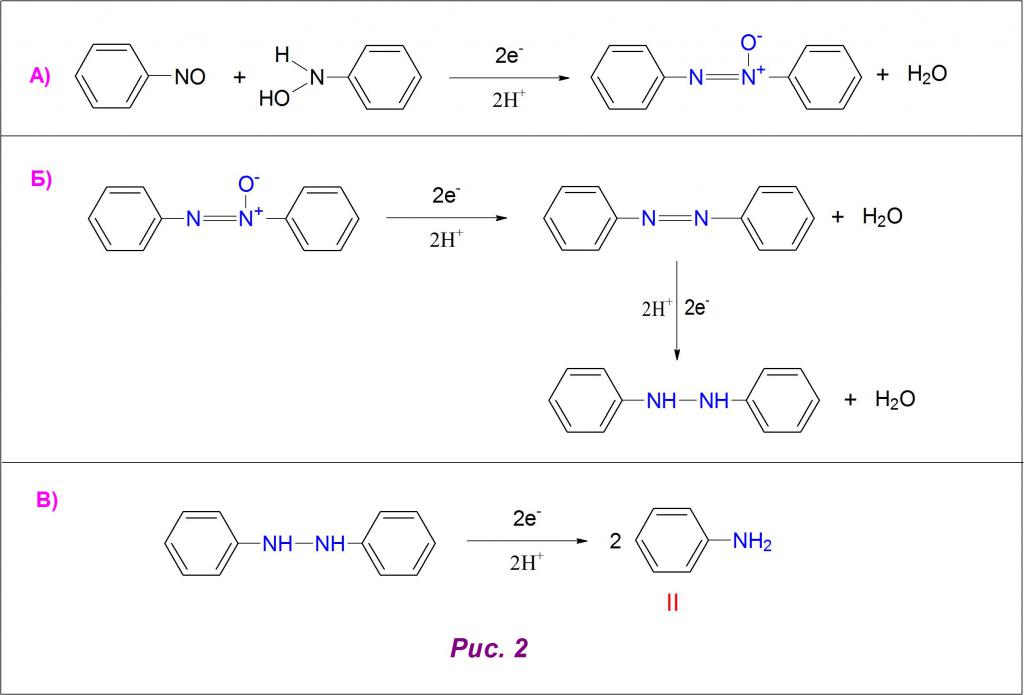
Il mezzo alcalino (pH> 8) influenza il decorso della reazione con la formazione di composti azoici e azo come prodotti di condensazione di arilidrossilammina e nitrosobenzene, quest'ultimo viene ripristinato molto lentamente in queste condizioni. L'azoossibenzene ottenuto dopo acidificazione dà un azo-derivato (figura 2A), e, a sua volta, reagisce con atomi di idrogeno per formare un composto idrazo (figura 2B).
Quando quest'ultimo viene ripristinato, si ottiene un'arylamina pronta (Figura 2B). Formule strutturali nitrobenzene e anilina sono rappresentati con numeri romani I e II nelle figure 1 e 2.
Reazione alla zinina
Nel 1842, lo scienziato russo Zinin N.N. sintetizzato dal nitrobenzene formula di anilina riducendo il primo solfuro di ammonio ((NH 4 ) 2 S) (esempio 8).
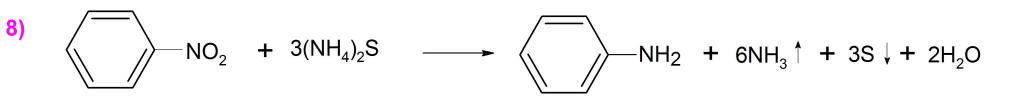
Nel tempo, lo scienziato ha confermato la fattibilità dell'uso della reazione nella preparazione di ammine aromatiche da altri composti nitro, che ha permesso di sviluppare una produzione su larga scala di coloranti sintetici, esplosivi e preparazioni farmaceutiche speciali.