Qual è la distribuzione di elettroni nei livelli di energia di diversi elementi chimici?
La distribuzione di elettroni nei livelli di energia spiega le proprietà metalliche e non metalliche di qualsiasi elemento.
Formula elettronica
Esiste una certa regola secondo cui le particelle negative libere e accoppiate sono poste a livelli e sottolivelli. Consideriamo più in dettaglio la distribuzione di elettroni per livelli di energia.
Al primo livello di energia ci sono solo due elettroni. Gli orbitali sono riempiti da loro mentre aumenta la riserva di energia. La distribuzione di elettroni nell'atomo dell'elemento chimico corrisponde al numero di sequenza. A livelli di energia con un numero minimo di più pronunciati forza di attrazione elettroni di valenza al nucleo.
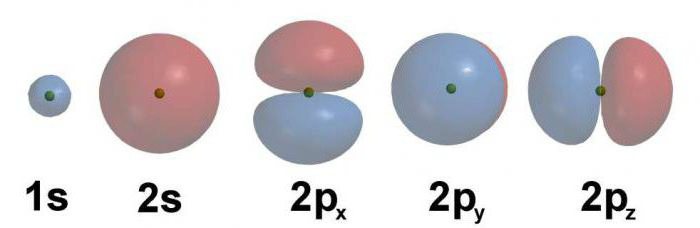
Un esempio della formula elettronica
Considera la distribuzione di elettroni di livelli di energia dall'esempio di un atomo di carbonio. Il suo numero di sequenza è 6, quindi, sei protoni con carica positiva si trovano all'interno del nucleo. Dato che il carbonio è un rappresentante del secondo periodo, è caratterizzato dalla presenza di due livelli di energia. Sul primo ci sono due elettroni, sul secondo - quattro.
Ad
La regola Hund spiega la disposizione nella stessa cella di soli due elettroni che hanno spin diversi. Al secondo livello di energia ci sono quattro elettroni. Di conseguenza, la distribuzione di elettroni in un atomo di un elemento chimico ha la seguente forma: 1s22s22p2.
Ci sono alcune regole in base alle quali la distribuzione di elettroni da parte di sottolivelli e livelli.
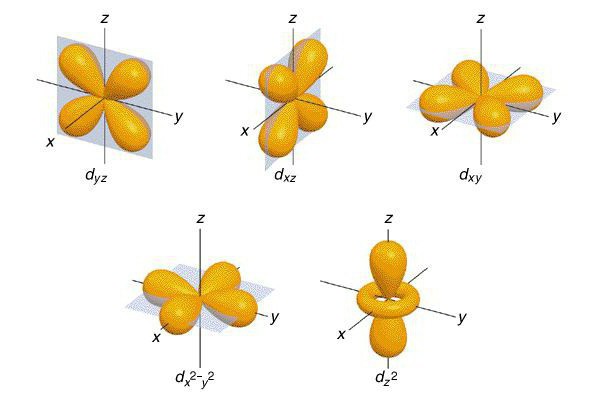
Principio di Pauli
Questo principio fu formulato da Pauli nel 1925. Lo scienziato concordò sulla possibilità di collocare nell'atomo solo due elettroni che hanno gli stessi numeri quantici: n, l, m, s. Si noti che la distribuzione di elettroni nei livelli di energia avviene quando aumenta lo stock di energia libera.
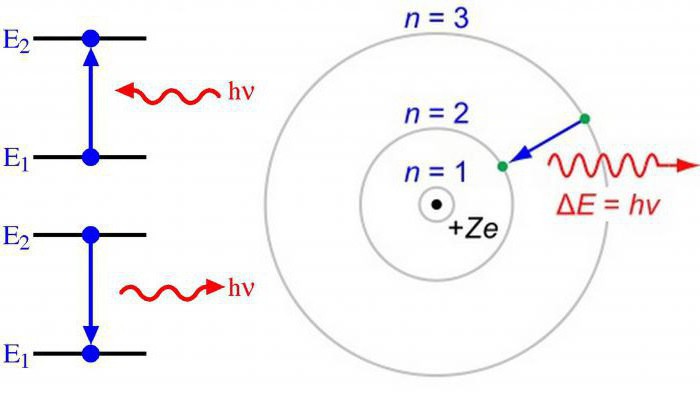
Regola Klechkovsky
Il riempimento degli orbitali energetici viene effettuato in base ad un aumento dei numeri quantici n + l ed è caratterizzato da un aumento della riserva di energia.
Considera la distribuzione di elettroni in un atomo di calcio.
Nello stato normale, la sua formula elettronica ha la seguente forma:
Ca 1s2 2s2 2p6 3s2 3p6 3d0 4s2.
Elementi di sottogruppi simili relativi agli elementi d- ed f, c'è un "fallimento" di un elettrone dal sottolivello esterno, che ha una riserva di energia inferiore, al precedente sottotitoli d- o f. Un fenomeno simile è caratteristico di rame, argento, platino, oro.
Ad
La distribuzione di elettroni in un atomo implica il riempimento dei sottolivelli con elettroni spaiati che hanno gli stessi spin.
Solo dopo che gli orbitali liberi sono completamente pieni di elettroni singoli, le cellule quantiche sono integrate con seconde particelle negative dotate di spin opposti.
Ad esempio, nello stato non eccitato dell'azoto:
1s2 2s2 2p3.
Le proprietà delle sostanze hanno un effetto configurazione elettronica elettroni di valenza. Con il loro numero, è possibile determinare la valenza superiore e inferiore, l'attività chimica. Se l'elemento si trova nel sottogruppo principale della tavola periodica, è possibile tramite il numero del gruppo impostare il livello di energia esterna, determinarlo stati di ossidazione. Ad esempio, il fosforo, che è nel quinto gruppo (sottogruppo principale), contiene cinque elettroni di valenza, quindi è in grado di accettare tre elettroni o di dare cinque particelle a un altro atomo.
Ad
Le eccezioni a questa regola sono tutti i rappresentanti dei sottogruppi della tabella periodica.
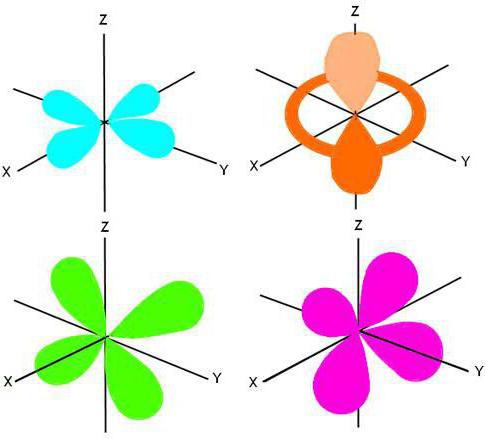
Caratteristiche familiari
A seconda della struttura del livello di energia esterna, vi è una suddivisione di tutti gli atomi neutri nella tavola periodica in quattro famiglie:
- Gli elementi s sono nel primo e nel secondo gruppo (sottogruppi principali);
- la famiglia p si trova nei gruppi III-VIII (sottogruppi A);
- gli elementi d possono essere trovati in sottogruppi simili dal gruppo I a VIII;
- La famiglia f consiste di attinidi e lantanidi.
Tutti gli elementi s nello stato normale hanno elettroni di valenza sul s-sottolivello. La presenza di elettroni liberi nei sottotitoli s e p è caratteristica degli elementi p.
Gli elementi D nello stato non eccitato hanno elettroni di valenza sia sull'ultimo s- sia sull'ultimo ma un sottotavolo d.
conclusione
Lo stato di qualsiasi elettrone in un atomo può essere descritto usando una serie di numeri di base. A seconda delle caratteristiche della sua struttura, possiamo parlare di una certa quantità di energia. Usando la regola di Hund, Klechkovsky, Pauli per qualsiasi elemento incluso nella tavola periodica, puoi creare una configurazione atom neutra.
Gli elettroni situati ai primi livelli hanno la più piccola quantità di energia nello stato non eccitato. Quando un atomo neutro viene riscaldato, viene osservata una transizione di elettroni, che è sempre accompagnata da un cambiamento nel numero di elettroni liberi, portando ad un cambiamento significativo nel tasso di ossidazione dell'elemento e ad un cambiamento nella sua attività chimica.