Metalli alcalini Struttura, proprietà fisiche e chimiche, applicazione
Metalli alcalini - il nome comune degli elementi del 1 ° gruppo del sistema periodico di elementi chimici. La sua composizione: litio (Li), sodio (Na), potassio (K), rubidio (Rb), cesio (Cs), francio (Fr), e l'elemento ipotetico - ununenium (Uue). Il nome del gruppo deriva dal nome di idrossidi solubili di sodio e di potassio, che hanno una reazione alcalina e sapore. Considerare le caratteristiche strutturali generali degli atomi degli elementi, le proprietà, la produzione e l'uso di sostanze semplici.
Numerazione di gruppo obsoleta e nuova
Secondo il sistema di numerazione obsoleto, i metalli alcalini che occupano la colonna verticale più a sinistra della tavola periodica appartengono al gruppo IA. Nel 1989, l'International Chemical Union (IUPAC) propose come opzione principale un'altra opzione (lungo periodo). I metalli alcalini secondo la nuova classificazione e la numerazione continua appartengono al 1o gruppo. Un rappresentante del 2 ° periodo - il litio - apre questo aggregato, completa il suo elemento radioattivo del 7 ° periodo - la Francia. Tutti i metalli del 1 ° gruppo nel guscio esterno degli atomi contengono un elettrone s, che facilmente danno via (vengono ripristinati).
Ad
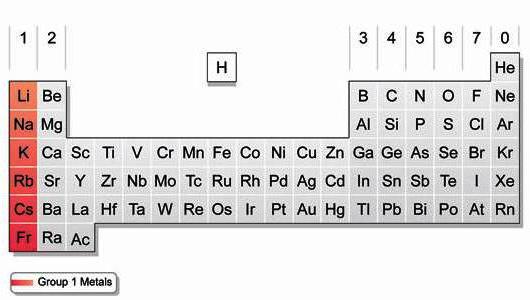
La struttura degli atomi di metallo alcalino
Gli elementi del 1 ° gruppo sono caratterizzati dalla presenza di un secondo livello di energia, ripetendo la struttura del precedente gas inerte. Il litio ha 2 elettroni nell'ultimo strato e 8 elettroni negli altri. Nelle reazioni chimiche, gli atomi rilasciano facilmente un s-elettrone esterno, acquisendo una configurazione energeticamente favorevole di un gas nobile. Gli elementi del primo gruppo hanno piccoli valori di energia di ionizzazione ed elettronegatività (EO). Formano facilmente ioni positivi caricati singolarmente. Durante la transizione dal litio alla Francia, il numero di protoni ed elettroni aumenta, il raggio dell'atomo. Il rubidio, il cesio e il francio donano più facilmente un elettrone esterno rispetto agli elementi che li precedono nel gruppo. Pertanto, nel gruppo dall'alto verso il basso, la capacità riducente aumenta.
Ad
Contenuto nella crosta
 La facile ossidabilità dei metalli alcalini porta al fatto che gli elementi del primo gruppo esistono in natura sotto forma di composti dei loro cationi caricati singolarmente. Il contenuto di sodio crosta terrestre - 2,0%, potassio - 1,1%. Altri elementi in esso sono in piccole quantità, ad esempio, scorte di Francia - 340 g. Cloruro di sodio dissolto in acqua di mare, salamoia di laghi salati ed estuari, forma depositi di pietra o sale. Insieme con l'alite, si trovano NaCl • KCl e sylvin KCl di sylvinite. feldspato formato da alluminosilicato di potassio K 2 [Al 2 Si 6 O 16 ]. Nell'acqua di un numero di laghi dissolti carbonato di sodio e le riserve di solfato dell'elemento sono concentrate nel Mar Caspio (Kara-Bogaz-Gol). Ci sono depositi nitrato di sodio in Cile (salnitro cileno). Esiste un numero limitato di composti del litio naturale. Il rubidio e il cesio si trovano sotto forma di impurità nei composti del 1 ° gruppo di elementi e il francio si trova nella composizione dei minerali di uranio.
La facile ossidabilità dei metalli alcalini porta al fatto che gli elementi del primo gruppo esistono in natura sotto forma di composti dei loro cationi caricati singolarmente. Il contenuto di sodio crosta terrestre - 2,0%, potassio - 1,1%. Altri elementi in esso sono in piccole quantità, ad esempio, scorte di Francia - 340 g. Cloruro di sodio dissolto in acqua di mare, salamoia di laghi salati ed estuari, forma depositi di pietra o sale. Insieme con l'alite, si trovano NaCl • KCl e sylvin KCl di sylvinite. feldspato formato da alluminosilicato di potassio K 2 [Al 2 Si 6 O 16 ]. Nell'acqua di un numero di laghi dissolti carbonato di sodio e le riserve di solfato dell'elemento sono concentrate nel Mar Caspio (Kara-Bogaz-Gol). Ci sono depositi nitrato di sodio in Cile (salnitro cileno). Esiste un numero limitato di composti del litio naturale. Il rubidio e il cesio si trovano sotto forma di impurità nei composti del 1 ° gruppo di elementi e il francio si trova nella composizione dei minerali di uranio.
Sequenza di Scoperta del metallo alcalino
Il chimico e fisico britannico G. Devi nel 1807 eseguì l'elettrolisi dei fusi di alcali, ricevendo prima sodio e potassio in forma libera. Nel 1817, lo scienziato svedese Johann Arfvedson scoprì l'elemento litio in minerali, e nel 1825, G. Devi individuò il metallo puro. Il rubidio fu scoperto per la prima volta nel 1861 da R. Bunsen e G. Kirchhoff. Ricercatori tedeschi hanno analizzato la composizione degli alluminosilicati e hanno ottenuto nello spettro la linea rossa corrispondente al nuovo elemento. Nel 1939, un impiegato dell'Istituto di Radioattività di Parigi, Margarita Pere, stabilì l'esistenza dell'isotopo di Francia. Ha anche nominato l'elemento in onore della sua terra natale. Ununennius (eka-francia) è il nome provvisorio di un nuovo tipo di atomo con il numero di serie 119. Il simbolo chimico Uue viene temporaneamente utilizzato. Dal 1985, i ricercatori hanno tentato di sintetizzare un nuovo elemento, che sarà il primo dell'ottavo periodo, il settimo del primo gruppo.
Ad
Proprietà fisiche dei metalli alcalini
 Quasi tutti i metalli alcalini hanno un colore bianco-argenteo e una lucentezza metallica su un taglio fresco (il cesio ha un colore giallo dorato). Lo scintillio si attenua nell'aria, appare un film grigio, sul litio è nero-verdastro. Questo metallo ha la più alta durezza tra i suoi vicini nel gruppo, ma è inferiore al talco - il minerale più morbido che apre la scala di Mohs. Il sodio e il potassio si piegano facilmente, possono essere tagliati. Il rubidio, il cesio e il francio in forma pura rappresentano una massa pastosa. La fusione dei metalli alcalini avviene ad una temperatura relativamente bassa. Per il litio raggiunge 180,54 ° C. Il sodio si scioglie a 97,86 ° C, il potassio a 63,51 ° C, il rubidio a 39,32 ° C, il cesio a 28,44 ° C. La densità dei metalli alcalini è inferiore alle sostanze correlate. Il litio galleggia nel cherosene, sale sulla superficie dell'acqua, anche il potassio e il sodio galleggiano in esso.
Quasi tutti i metalli alcalini hanno un colore bianco-argenteo e una lucentezza metallica su un taglio fresco (il cesio ha un colore giallo dorato). Lo scintillio si attenua nell'aria, appare un film grigio, sul litio è nero-verdastro. Questo metallo ha la più alta durezza tra i suoi vicini nel gruppo, ma è inferiore al talco - il minerale più morbido che apre la scala di Mohs. Il sodio e il potassio si piegano facilmente, possono essere tagliati. Il rubidio, il cesio e il francio in forma pura rappresentano una massa pastosa. La fusione dei metalli alcalini avviene ad una temperatura relativamente bassa. Per il litio raggiunge 180,54 ° C. Il sodio si scioglie a 97,86 ° C, il potassio a 63,51 ° C, il rubidio a 39,32 ° C, il cesio a 28,44 ° C. La densità dei metalli alcalini è inferiore alle sostanze correlate. Il litio galleggia nel cherosene, sale sulla superficie dell'acqua, anche il potassio e il sodio galleggiano in esso.
Stato cristallino
La cristallizzazione dei metalli alcalini avviene in una sinagoga cubica (centrata sul corpo). Gli atomi nella sua composizione hanno una banda di conduzione, ai livelli liberi di cui gli elettroni possono trasferire. Sono queste particelle attive che portano uno speciale legame chimico - metallico. La struttura comune dei livelli di energia e la natura dei reticoli cristallini spiegano la somiglianza degli elementi del primo gruppo. Durante la transizione dal litio al cesio, le masse degli atomi degli elementi aumentano, il che porta ad un aumento regolare della densità, nonché a un cambiamento in altre proprietà.
Ad
Proprietà chimiche dei metalli alcalini
L'unico elettrone esterno negli atomi di metallo alcalino è debolmente attratto dal nucleo, quindi hanno una bassa energia di ionizzazione, un'affinità elettronica negativa o vicina a zero. Gli elementi del 1 ° gruppo, in possesso di un'attività riducente, non sono praticamente in grado di ossidarsi. Nel gruppo top-down, l'attività nelle reazioni chimiche aumenta:
- Sodio, potassio e litio con una leggera luce di riscaldamento nell'aria. Per i primi due metalli, la formazione di perossidi e perpossidi in questa reazione è caratteristica, e per il litio, l'ossido Li 2 O. Rubidio e cesio nell'aria autoincendiaria.
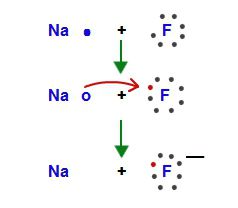 I metalli alcalini possono persino ridurre l'idrogeno. Una volta riscaldato, interagire con gli atomi dell'elemento più leggero e ripristinarlo sullo ione H caricato negativamente. Nella reazione, si ottengono idruri, per esempio, NaH, KH.
I metalli alcalini possono persino ridurre l'idrogeno. Una volta riscaldato, interagire con gli atomi dell'elemento più leggero e ripristinarlo sullo ione H caricato negativamente. Nella reazione, si ottengono idruri, per esempio, NaH, KH. - Le sostanze semplici corrispondenti agli elementi del primo gruppo interagiscono con l'acqua e formano alcali, ad esempio LiOH, NaOH, KOH. Il processo è accompagnato dal rilascio di idrogeno gassoso, che si autoincide o esplode. 2Na + 2H 2 O = 2NaOH + H 2 . Il rubidio e il cesio reagiscono anche con il ghiaccio. Lo stoccaggio di metalli alcalini è consentito sotto uno strato di olio minerale, in cherosene, in recipienti di vetro sigillati.
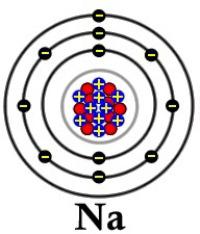
- I metalli del primo gruppo interagiscono attivamente con gli alogeni, la reazione con fluoro e cloro è particolarmente vigorosa e, se riscaldata, con zolfo e fosforo. La maggior parte dei sali risultanti ha una buona solubilità.
- Reazione di alta qualità: la decomposizione di sali di metalli alcalini nel fuoco di un bruciatore a gas. Le coppie colorano la fiamma in un colore specifico.
- Quando i metalli alcalini interagiscono con gli alcoli, si ottengono gli alcolati, con acidi carbossilici che forniscono i sali corrispondenti, ad esempio il formiato di sodio.
Preparazione e uso di metalli alcalini
I metalli appartenenti al 1 ° gruppo sono prodotti industrialmente mediante l'elettrolisi di fusione dei loro alogenuri e di altri composti naturali. Dopo la decomposizione sotto l'azione della corrente elettrica, gli ioni positivi al catodo attaccano gli elettroni e vengono ridotti a un metallo libero. L'anione è ossidato sull'elettrodo opposto.
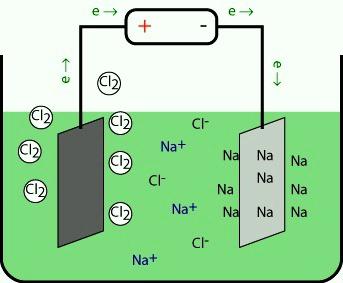
Durante l'elettrolisi dell'idrossido si scioglie sull'anodo, le particelle OH vengono ossidate, l'ossigeno si sviluppa e si ottiene acqua. Un altro metodo è la riduzione termica dei metalli alcalini da fusione dei loro sali di calcio. Le sostanze semplici e i composti di elementi del 1o gruppo sono di importanza pratica. Il litio è usato come materia prima nell'energia atomica, utilizzata nella tecnologia missilistica. In metallurgia, è usato per rimuovere l'idrogeno residuo, l'azoto, l'ossigeno e lo zolfo. L'idrossido è integrato con l'elettrolito in batterie alcaline.

Il sodio è necessario per l'energia nucleare, la metallurgia, la sintesi organica. Il cesio e il rubidio sono utilizzati nella produzione di celle fotovoltaiche. Idrossidi e sali, in particolare cloruri, nitrati, solfati, carbonati di metalli alcalini, sono ampiamente utilizzati. I cationi hanno attività biologica, gli ioni sodio e potassio sono particolarmente importanti per il corpo umano.