Carburo di calcio: proprietà e applicazione. Ottenere acetilene
I carburi sono un gruppo di composti di carbonio inorganici con metalli, nonché con silicio o boro (poiché questi elementi presentano proprietà metalliche). Il carburo di calcio è una delle sostanze più richieste di questo gruppo. Sulle proprietà e sull'applicazione del composto, leggi sotto.
Ricevere la cronologia
Il carburo di calcio è un composto ampiamente usato nell'industria moderna. Nel 1862, il chimico tedesco Friedrich Weler sintetizzò per la prima volta una molecola di questa sostanza. Ottenendo il carburo di calcio, ha effettuato come segue. Lo scienziato preparò un calcio fuso con lo zinco e poi lo scaldò con il carbone. Il risultato è carburo. La formula chimica del composto è CaC 2 . Il metodo industriale di produzione del carburo fu proposto dallo scienziato Moissan nel 1892. Altri nomi della sostanza sono calcio acetilato o carbonato di calcio. Il reticolo cristallino del composto è il seguente:
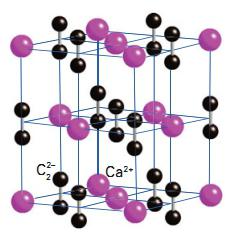
Proprietà fisiche
Secondo le sue proprietà fisiche, il carburo di calcio è una sostanza cristallina con un punto di fusione di 2300 o C. Questa cifra è valida solo per composti puri. Le impurità contenenti carburo possono avere altri punti di fusione. Il principale stato aggregativo della materia è solido e il colore varia dal grigio al marrone.
Proprietà chimiche
Il carburo di calcio assorbe bene l'acqua. Questo processo è accompagnato da una reazione di decomposizione chimica. È importante che la polvere di carburo abbia un effetto irritante sulle mucose, sulla pelle e organi respiratori. Pertanto, mentre si lavora con il composto, è necessario utilizzare maschere antigas o respiratori antipolvere. Il carburo di calcio interagisce con l'ossigeno ad alta temperatura per formare carbonato di calcio. La reazione con l'azoto porta alla sintesi del calcio cianammide. Anche a temperature elevate, il carburo di calcio reagisce con cloro, fosforo, arsenico. Ma ancora una delle proprietà più importanti di un composto è la decomposizione dell'acqua.

reception
La produzione di carburo di calcio è la seguente. Calce viva e coca cola pre-schiacciata sono miscelati. La miscela risultante viene fusa in forni elettrici. Coke e ossido di calcio sono presi in parti uguali in peso. Il processo avviene a una temperatura di 1900 ° C. Il fuso lascia la fornace e viene successivamente versato in forme speciali. Quindi, il carburo di calcio già indurito viene frantumato e ordinato in base alla dimensione dei pezzi. I granuli di una sostanza sono suddivisi in quattro frazioni secondo le loro dimensioni: 25 × 80, 15 × 25, 8 × 15, 2 × 8, che sono definiti da GOST 1460-56. Con la sua composizione, il carburo di calcio tecnico contiene il 75-80% della sostanza principale. La quota di impurità, come il carbonio, la calce e altri, rappresenta fino al 25% della massa totale della miscela. Inoltre, il solfuro e il fosfuro di calcio contenuti nel carburo tecnico causano un odore piuttosto sgradevole. Immagina la reazione di ottenere CaC 2 : CaO + 3C → CaC 2 + CO ↑. La formazione di calcio acetilico è accompagnata da assorbimento di calore. Pertanto, è logico supporre che la reazione della sua decomposizione, al contrario, corrisponda al rilascio di energia.

Trasporto e stoccaggio
A causa del fatto che l'umidità decompone istantaneamente il carburo con il rilascio di una grande quantità di calore e la formazione di un gas acetilene esplosivo, la sostanza deve essere conservata in fusti o barattoli ermeticamente chiusi. Va ricordato che l'acetilene è più leggero dell'aria e può accumularsi nelle zone superiori della stanza. Questo gas, oltre all'azione narcotica, ha la capacità di auto-accendersi. Pertanto, è necessario utilizzare il carburo di calcio con grande cura. Particolare attenzione viene dedicata al confezionamento in produzione. La sostanza finita viene posta in fusti speciali (un contenitore che assomiglia a lattine). Tale confezione richiede un'attenta apertura. Deve essere usato uno strumento che non porti alla formazione di scintille (un martello o un coltello speciale). Nel caso del carburo sulla pelle o sulle mucose, è necessario lavare immediatamente l'area interessata con acqua e trattare il posto con vaselina o crema grassa. Il trasporto della connessione viene effettuato utilizzando solo coperto tipi di trasporto. La consegna di carburo disperso nell'aria è proibita. I locali in cui è conservato il CaC 2 devono essere ben ventilati. Non è inoltre permesso conservare il carburo insieme ad altri prodotti chimici. Questo può portare a reazioni indesiderabili e probabilmente pericolose. La durata di conservazione del carburo è di sei mesi.

applicazione
La portata del carburo di calcio è estremamente ampia. Prima di tutto, è la sintesi industriale. Il carburo di calcio viene utilizzato per produrre gomma sintetica, acido acetico, acetone, etilene, cloruro di vinile, stirene. Trova anche applicazione nella preparazione del calcio cianammide. Questa sostanza è preziosa per il suo uso nella sintesi di vari fertilizzanti e sostanze cianidiche. In agricoltura, qualsiasi agronomo conosce un nome come regolatore carburo di carburo. È usato per regolare la crescita delle piante. E per ottenerlo si usa anche il carburo di calcio. Inoltre, questo composto viene utilizzato nella produzione di calcio cianammide. Questa reazione è basata sul riscaldamento del carburo di calcio con azoto. recupero metalli alcalini anche non senza l'uso della sostanza da noi descritta. Il carburo di calcio è utilizzato nel processo di saldatura a gas. Ad esempio, le lampade al carburo sono ampiamente utilizzate. Il principio del loro lavoro si basa sull'interazione in un contenitore speciale di carburo con acqua e combustione all'uscita dell'apparecchio della sostanza finale della reazione - acetilene. Guarda la foto della lampada al carburo.

Produzione di acetilene
Una delle applicazioni più importanti del carburo di calcio è il suo uso nella produzione di acetilene. Il merito per la scoperta di questo metodo appartiene anche al chimico tedesco Friedrich Vehler. La base di questo processo industriale è la reazione di decomposizione del carburo sotto l'influenza dell'acqua. CaC 2 + 2 H 2 O → C 2 H 2 + Ca (OH) 2 ↓. All'uscita si forma gas acetilene e calce idrata, precipita. Il processo è accompagnato dal rilascio di una grande quantità di calore. Il volume di gas all'uscita dipende da quanto è pulito il carburo di calcio per la reazione. L'acetilene prodotto come risultato può avere un volume diverso: 1 kg della sostanza iniziale può produrre da 235 a 290 litri di gas. Per quanto riguarda la velocità di reazione, dipende sia da una piccola percentuale di impurità nel carburo di calcio e dalla temperatura dell'acqua, sia dalla sua purezza. Se consideriamo la reazione teorica della produzione di acetilene dal carburo, sono sufficienti 560 ml di acqua per 1 kg di carburo. Tuttavia, in pratica, aumenta il volume d'acqua per la reazione. Per 1 kg di carburo di calcio nelle condizioni di sintesi industriale richiede da 5 a 20 litri di acqua. Questa quantità è necessaria per garantire che l'acetilene sia meglio raffreddato e per garantire una sicurezza ottimale durante il funzionamento. Di seguito il chimico tedesco Friedrich Veler.

Esperienza di laboratorio dell'acetilene
Molte delle lezioni di chimica a scuola hanno familiarità con la reazione dell'interazione acqua carburo. Tipicamente, questa esperienza ci permette di dimostrare la reazione per ottenere acetilene, così come le sue proprietà fisiche e chimiche. Allo stesso tempo, il processo di sviluppo del gas avviene in modo piuttosto vigoroso, quindi il tubo che drena l'acetilene dal pallone con i principi attivi viene posto in una ciotola con acqua. Ciò fornisce meno movimento attivo e rapido del gas. Inoltre, in laboratorio, è possibile utilizzare un altro metodo per effettuare una reazione non troppo violenta della decomposizione di tali composti come il carburo. L'acetilene in questo caso va in modo uniforme e calmo. Per fare questo, invece di acqua, devi prendere una soluzione satura di sale. Anche in laboratorio, quando si esegue questa reazione, l'acqua deve essere attentamente aggiunta al carburo posto nel matraccio volumetrico, e non viceversa.