Cloro: valenza, proprietà chimiche
La valenza determina la capacità del cloro di attaccare a sé gli atomi di altri elementi chimici.
Il cloro, la cui valenza ha significati diversi, si trova nel settimo gruppo, nel sottogruppo principale della tabella degli elementi. Cerchiamo di scoprire le caratteristiche strutturali dell'atomo di questo alogeno.
Cloro in buone condizioni
La valenza degli atomi di cloro è determinata dalle caratteristiche strutturali del suo livello esterno. Questo elemento è nel gruppo 7 (A), ha il diciassettesimo numero di sequenza. Dato che l'elemento è rappresentativo del quarto periodo, non ha solo s-, p-, ma anche d-orbitali.
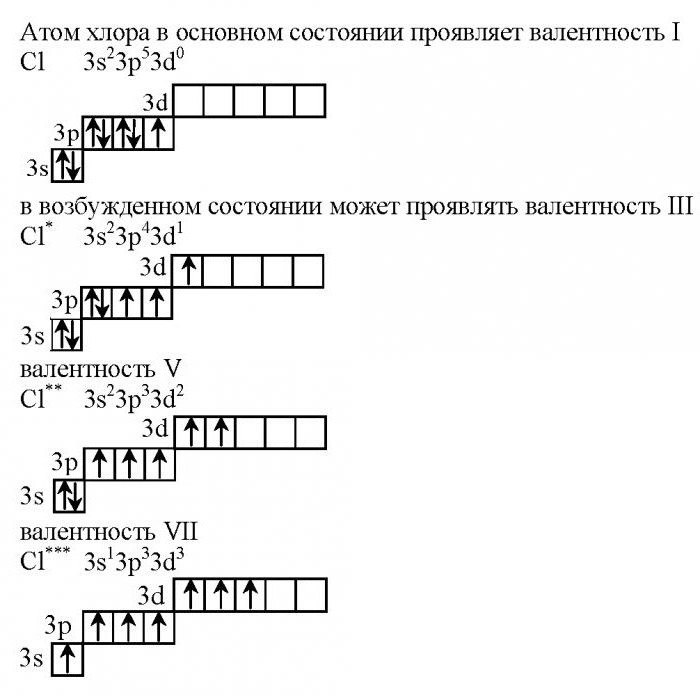
Configurazione elettronica dell'atomo
Quale formula elettronica ha il cloro? La valenza è associata alle caratteristiche dell'esterno livello di energia quindi, scriviamo la configurazione di questo elemento.
Nello stato non eccitato, solo due elettroni si trovano sul primo livello di cloro, il secondo è occupato da otto, al terzo livello ce ne sono 10. Nota che all'ultimo livello c'è un d-orbitale vuoto, che caratterizza le possibilità di valenza di questo alogeno.
Ad
- 1s22s22p63s23p53d0.
In questo caso, la valenza del cloro è uguale a I. Questo è tipico quando si interagisce con i metalli (si formano cloruri). La valenza più alta VII è il cloro in composti con non metalli, ad esempio in ossido di cloro (7), nonché in acido perclorico.
Diamo come esempio le formule dei composti del cloro in cui esibisce la seguente valenza: HClO 4 , Cl 2 O 7 .
L'ultimo livello elettronico nella chimica inorganica si chiama valenza, poiché è lui che spiega la capacità di un elemento di entrare in interazioni chimiche con altri atomi.

Stato eccitato
Come si comporta il cloro quando riscaldato? La sua valenza cambierà se l'atomo si trova in uno stato eccitato.
Dato che ogni livello di energia ha una certa quantità di energia, gli elettroni dei primi due livelli non cambiano la loro posizione originale. Si osserva una transizione di un elettrone p dal livello di energia 3p al sottolivello 3d. In che modo questo cambierà la loro partecipazione alle reazioni chimiche del cloro? La sua valenza cambierà, sarà uguale a tre.
Ad
Considera la configurazione elettronica che il cloro acquisisce in questo caso.
- 1s22s22p63s23p43d1.
Questa configurazione non è stabile, quindi i composti di cloro, nei quali mostrano un grado di ossidazione di +3, si decompongono rapidamente.
Poiché ci sono altre quattro cellule quantiche libere sugli orbitali 3d, è possibile la successiva transizione di un elettrone dal sottolivello 3p, che porta alla formazione di un'altra configurazione dell'atomo di cloro.
- 1s22s22p63s23p33d2.
In questo caso, ci sono cinque elettroni spaiati, quindi il cloro è in grado di mostrare la valenza V, lo stato di ossidazione +5.
Al massimo riscaldamento dell'atomo di cloro, l'elettrone viene trasferito dal sottolivello 3s all'orbitale 3d. In questo caso, il cloro ha una valenza massima di sette.
- 1s22s22p63s13p33d3.
A livello di energia esterna, ha sette elettroni spaiati, quindi la valenza di cloro nei composti è 7.
La distribuzione di elettroni per livelli, sottolivelli, la loro transizione viene effettuata in conformità con la regola Hund e il principio di Pauli.
Come viene indicato il cloro in questo caso? La valenza dell'elemento è solitamente indicata con numeri romani e lo stato eccitato dell'atomo è contrassegnato da un asterisco.
conclusione
Tutti i costi energia interna che vanno al processo di eccitazione dell'atomo di cloro, sono completamente compensati dall'energia che viene rilasciata durante la formazione legami covalenti. Questo spiega l'aumentata attività chimica del cloro in uno stato eccitato. Al suo massimo stati di ossidazione (+7) mostra le proprietà di un forte agente ossidante.
Ad
Le capacità di valenza di un atomo di un elemento chimico non sono limitate solo dal numero di elettroni spaiati in una forma stazionaria ed eccitata. Ad esempio, nella formazione di legami in molecole attraverso un meccanismo donatore-accettore, si assume anche l'uso di orbitali liberi.
Quali fattori influenzano la capacità di valenza dell'atomo di cloro? Riassumendo, diciamo che prima di tutto è necessario notare il numero di elettroni spaiati (orbitali vuoti). Inoltre, l'atomo deve avere un orbitale libero a cui gli elettroni si trasferiranno quando riscaldato.