È un metodo di analisi titrimetrica di cosa si tratta?
Il metodo di analisi titrimetrico (titolazione) consente di effettuare un'analisi quantitativa volumetrica ed è ampiamente utilizzato in chimica. Il suo principale vantaggio è una varietà di metodi e metodi, grazie ai quali può essere utilizzato per risolvere vari compiti analitici.
Principio di analisi
Il metodo di analisi titrimetrico si basa sulla misurazione del volume di una soluzione di una concentrazione nota (titolante) che ha reagito con la sostanza in esame.
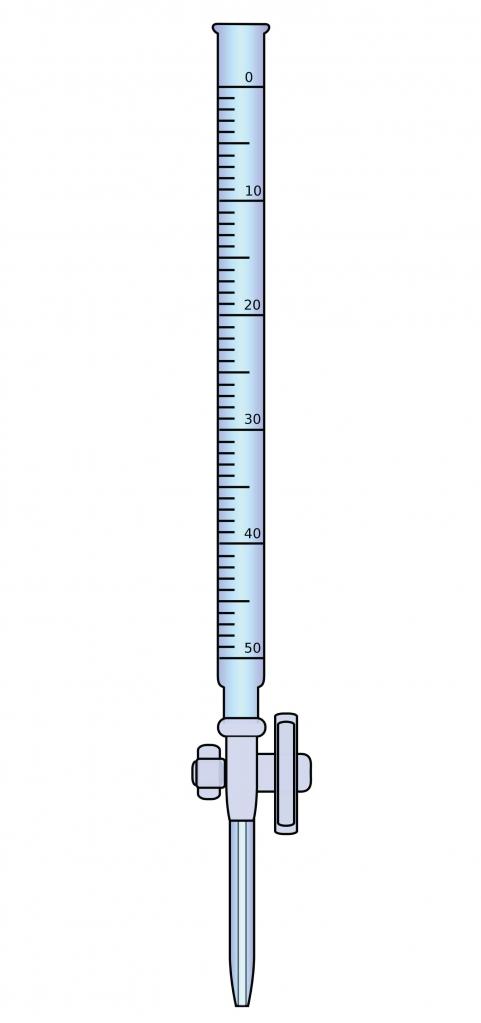
Per l'analisi, avrete bisogno di attrezzature speciali, vale a dire una buretta - un tubo di vetro sottile con una graduazione applicata. L'estremità superiore di questo tubo è aperta e nella parte inferiore c'è un rubinetto. La buretta calibrata che utilizza un imbuto riempie il titolante fino a zero. L'analisi viene eseguita fino al punto finale della titolazione (CTT), aggiungendo una piccola quantità di soluzione dalla buretta alla sostanza di prova. Il punto finale della titolazione è identificato da un cambiamento nel colore dell'indicatore o da una qualche proprietà fisico-chimica.
Il risultato finale è calcolato dal volume speso del titolante ed è espresso in titolo (T) - la massa della sostanza per 1 ml di soluzione (g / ml).
Processo di giustificazione
Il metodo titrimetrico di analisi quantitativa fornisce risultati accurati, poiché le sostanze reagiscono tra loro in quantità equivalenti. Ciò significa che il prodotto del loro volume e della loro quantità è identico l'uno con l'altro: C 1 V 1 = C 2 V 2 . Da questa equazione è facile trovare il valore sconosciuto di C 2 , se i restanti parametri sono impostati indipendentemente (C 1 , V 2 ) e vengono stabiliti durante l'analisi (V 1 ).
Rilevazione del punto finale della titolazione
Poiché la registrazione tempestiva della fine della titolazione è la parte più importante dell'analisi, è necessario scegliere i giusti metodi. L'uso di indicatori a colori o fluorescenti è considerato il più conveniente, ma possono essere utilizzati anche metodi strumentali come potenziometria, amperometria e fotometria.

La scelta finale del metodo per rilevare un CTT dipende dalla precisione richiesta e dalla selettività della determinazione, nonché dalla sua velocità e dalle sue capacità di automazione. Questo è particolarmente vero per soluzioni torbide e colorate, così come per i media aggressivi.
Requisiti di reazione alla titolazione
Affinché il metodo di analisi titrimetrico fornisca il risultato corretto, è necessario scegliere la giusta reazione che ne è alla base. I requisiti per esso sono i seguenti:
- stechiometria;
- portata elevata;
- alta costante di equilibrio;
- disponibilità di un metodo affidabile per fissare la fine sperimentale della titolazione.
Le reazioni adatte possono essere di qualsiasi tipo.
Tipi di analisi
La classificazione dei metodi di analisi titrimetrica si basa sul tipo di reazione. Su questa base, si distinguono i seguenti metodi di titolazione:
- acido-base;
- redox;
- complessometriche;
- Un decanter.
Ogni tipo è basato sul proprio tipo di reazione, i titani specifici sono selezionati, a seconda dei sottogruppi di metodi identificati nell'analisi.
Titolazione acido-base
Il metodo di analisi titrimetrico che utilizza la reazione dell'interazione di idrossido con uno ione idrossido (H 3 O + + OH - = H 2 O) è chiamato acido-base. Se una sostanza nota forma un protone in soluzione, tipico degli acidi, il metodo appartiene al sottogruppo acidimetria. Qui, l'acido cloridrico stabile HCl viene solitamente usato come titolante.
Se il titolante forma uno ione idrossido, il metodo è chiamato alcalimetria. Le sostanze utilizzate sono alcali, per esempio, NaOH, o sali ottenuti facendo reagire una base forte con un acido debole, come Na 2 CO 3 .
Indicatori utilizzati in questo colore. Sono composti organici deboli - acidi e basi, in cui la struttura e il colore delle forme protonate e non protonate differiscono. Molto spesso, l'indicatore monocromatico fenolftaleina (una soluzione limpida in un mezzo alcalino diventa lampone) e l'arancio metilico bicolore (la sostanza rossa diventa gialla in un mezzo acido) vengono utilizzati nella titolazione acido-base.

Il loro uso diffuso è associato ad un elevato assorbimento della luce, grazie al quale il loro colore è chiaramente visibile ad occhio nudo, e il contrasto e l'area di transizione dei colori stretti.
Titolazione redox
L'analisi titrimetrica redox è un metodo di analisi quantitativa basato sulla variazione del rapporto delle concentrazioni delle forme ossidate e ridotte: aOx 1 + bRed 2 = aRed 1 + bOx 2 .
Il metodo è suddiviso nei seguenti sottogruppi:
- permanganatometria (titolante - KMnO 4 );
- iodometria (I 2 );
- dicromatometria (K 2 Cr 2 O 7 );
- bromatometria (KBrO 3 );
- iodatometria (KIO 3 );
- cerimetria (Ce (SO 4 ) 2 );
- vanadometria (NH 4 VO 3 );
- titanometria (TiCl 3 );
- cromometria (CrCl 2 );
- ascorbometria (C 6 H 8 OH).
In alcuni casi, il ruolo di un indicatore può essere svolto da un reagente che partecipa alla reazione e cambia il suo colore con l'acquisizione di una forma ossidata o ridotta. Ma usano anche indicatori specifici, ad esempio:
- Nel determinare lo iodio, viene usato l'amido, che forma un composto blu scuro con I 3 - ioni;
- nella titolazione del ferro ferrico vengono usati ioni tiocionici, che formano complessi con il metallo, dipinti in colore rosso vivo.

Inoltre, ci sono speciali indicatori redox - composti organici con diversi colori delle forme ossidate e ridotte.
Titolazione complessometrica
In breve, il metodo di analisi titrimetrico, chiamato complexometric, si basa sull'interazione di due sostanze con la formazione di un complesso: M + L = ML. Se si utilizzano sali di mercurio, ad esempio Hg (NO 3 ) 2 , il metodo è chiamato mercurimetria, se l'acido etilendiamminotetraacetico (EDTA) è complessoonometria. In particolare, utilizzando il secondo metodo, viene utilizzato un metodo titrimetrico per analizzare l'acqua, ovvero la sua durezza.
Nella complessitonometria vengono utilizzati indicatori di metallo trasparente che acquisiscono colore nella formazione di complessi con ioni metallici. Ad esempio, quando si titolano sali di ferro ferrico con EDTA, viene usato come indicatore un acido solfosalicilico trasparente. Macchia la soluzione rossa quando complessata con il ferro.

Tuttavia, gli indicatori metallici hanno spesso il loro colore, che varia a seconda della concentrazione dello ione metallico. Come tali indicatori, si usano acidi polibasici, che formano complessi abbastanza stabili con metalli, che allo stesso tempo si deteriorano rapidamente quando esposti ad EDTA con discolorazione contrastante.
Titolazione della precipitazione
Il metodo di analisi titrimetrico, che si basa sulla reazione dell'interazione di due sostanze con la formazione di un composto solido che precipita (M + X = MX ↓), sta precipitando. Ha un valore limitato, poiché di solito i processi di deposizione procedono in modo non quantitativo e non stechiometrico. Ma a volte è ancora usato e ha due sottogruppi. Se nel metodo si utilizzano sali d'argento, ad esempio AgNO 3 , si parla di argentometria, se sali di mercurio, Hg 2 (NO 3 ) 2 , quindi mercurometria.
Per rilevare il punto finale della titolazione utilizzando i seguenti metodi:
- Il metodo di Mohr, in cui l'indicatore è uno ione cromato che forma un sedimento di mattoni rossi con argento;
- il metodo Folgard basato sulla titolazione di una soluzione di ioni d'argento con tiocianato di potassio in presenza di ferro ferrico, che forma un complesso rosso con il titolante in un mezzo acido;
- Metodo Faience che comporta la titolazione con indicatori di adsorbimento;
- Metodo Gay-Lussac, in cui la CTT è determinata dall'illuminazione o dall'annullamento della soluzione.

Quest'ultimo metodo non è stato praticamente usato di recente.
Metodi di titolazione
La titolazione è classificata non solo dalla reazione sottostante, ma anche dal metodo di implementazione. Su questa base, si distinguono i seguenti tipi:
- diretta;
- il contrario;
- titolazione del sostituente.
Il primo caso viene utilizzato solo in condizioni di una reazione ideale. Il titolante viene aggiunto direttamente alla sostanza da rilevare. Quindi con l'aiuto dell'EDTA determiniamo il magnesio, il calcio, il rame, il ferro e circa 25 metalli. Ma in altri casi più spesso usi metodi più complessi.
Titolazione posteriore
La reazione ideale non è sempre possibile scegliere. Molto spesso procede lentamente, oppure è difficile scegliere un metodo per fissare il punto finale della titolazione, o si formano composti volatili tra i prodotti, per i quali la sostanza da determinare viene parzialmente persa. Per superare questi inconvenienti, è possibile utilizzare il metodo di titolazione inversa. Per fare ciò, una grande quantità di titolante viene versata alla sostanza da rilevare in modo che la reazione sia completa, e quindi viene determinato quanta soluzione rimane non reagita. Per questo, i resti del titolante dalla prima reazione (T 1 ) sono titolati con un'altra soluzione (T 2 ), e la sua quantità è determinata dalla differenza dei prodotti dei volumi e delle concentrazioni in due reazioni: С T1 V T 1 -C T 2 V T 2 .
L'uso del metodo di analisi titrimetrico al contrario è alla base della determinazione del biossido di manganese. La sua interazione con il solfato di ferro è molto lenta, quindi il sale viene assunto in eccesso e la reazione viene accelerata dal riscaldamento. La quantità non reagita di ioni ferro è titolata con dicromato di potassio.

Titolare della titolazione
La titolazione del sostituente viene utilizzata nel caso di reazioni non stechiometriche o lente. La sua essenza è che per l'analita viene selezionata una reazione stechiometrica con un composto ausiliario, dopo di che il prodotto di interazione viene sottoposto a titolazione.
Questo è quello che fanno quando determinano il bicromato. Lo ioduro di potassio viene aggiunto ad esso, con conseguente rilascio di un equivalente di iodio equivalente alla sostanza da rilevare, che viene poi titolato con tiosolfato di sodio.
Pertanto, l'analisi titrimetrica consente di determinare il contenuto quantitativo di un'ampia gamma di sostanze. Conoscendo le loro proprietà e caratteristiche delle reazioni, si può scegliere il metodo ottimale e il metodo di titolazione, che darà un risultato con un alto grado di precisione.