Pressione osmotica nella natura e nella vita umana
Il materiale fornito per la tua recensione fornirà informazioni sulla pressione osmotica (g). Di seguito verranno presi in considerazione: la formulazione del termine, caratteristiche e proprietà, metodi di misurazione della pressione, il rapporto con la biologia e la relazione con soluzioni (pp) di diversi tipi.
Conoscenza della pressione osmotica
La pressione osmotica è l'eccesso di pressione idrostatica esercitata sulle soluzioni. Allo stesso tempo, le soluzioni stesse dovrebbero essere separate da un tipo di membrana semi-permeabile da solventi puri. Il processo di dissoluzione della diffusione attraverso la membrana in tali condizioni non si verifica. Lo scopo di questa pressione è di cercare di creare un equilibrio equo tra le concentrazioni di ogni soluzione, e il mezzo è l'incontro della diffusione molecolare tra il soluto e il solvente. La pressione osmotica è indicata dalla lettera "π" (pi).
Ad
A proposito di proprietà
La pressione osmotica ha il fenomeno della tonicità, che è una misura graduale della pressione osmotica. In altre parole, questo è il potenziale della differenza d'acqua in una coppia di p-fossa separata da una membrana semipermeabile. Soluzione ipertonica Nominare la sostanza avendo in confronto ad altra soluzione una pressione osmotica più alta. Una soluzione ipotonica, al contrario, ha un indice osmotico inferiore.
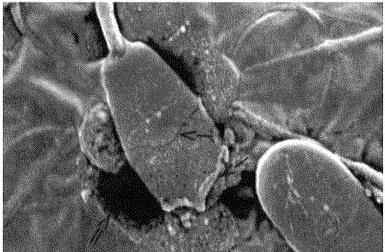
Se una tale soluzione viene collocata in uno spazio chiuso, ad esempio, in una cella del sangue, allora vedremo che la pressione osmotica può rompersi membrana cellulare. I farmaci introdotti nel sangue vengono prima mescolati con un p-rum isotonico, portandoli alla dissoluzione proprio per questo motivo. Con questo cloruro di sodio nella soluzione dovrebbe essere contenuto in una quantità in grado di bilanciare l'effetto osmotico del fluido cellulare.
Ad
Se le droghe di un tipo somministrato sono state fatte sulla base di acqua o soluzioni altamente diluite, la decomposizione osmotica potrebbe rompere i globuli forzando l'acqua a penetrare in essi. La creazione di soluzioni utilizzando concentrazioni di sostanze troppo elevate costringerà l'acqua a lasciare le cellule e, di conseguenza, si restringerà. Per questo è sufficiente dal tre al dieci percento di cloruro di sodio nel p-re.
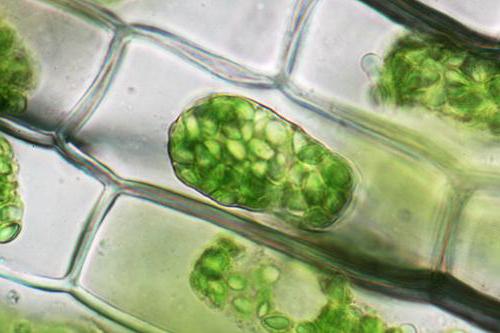
Le cellule vegetali, a differenza degli animali, saranno sottoposte alla separazione dalla parete cellulare, tutto il suo contenuto, ad eccezione della parete cellulare esterna, ma insieme alla membrana. Questo fenomeno è chiamato plasmolisi. Deplazmolizom, a sua volta, è il processo osservato quando si spostano le cellule ristrette nella pp di un tipo più diluito.
Il rapporto tra pressione e soluzione
La natura chimica dei soluti nel composto non influisce sulla grandezza dell'effetto osmotico. Il suo tasso dipende dalla quantità di queste sostanze nel p-re. Pertanto, vediamo che la pressione osmotica è una proprietà colligativa della soluzione. La pressione aumenterà con l'aumento della concentrazione di sostanze attive nel p-re. Questo è indicato dalla legge della pressione osmotica. La formula è abbastanza semplice:
π = i · C · R · T ,
dove coefficiente isotonico è indicato dalla lettera i , il livello molare della concentrazione di p-ra è espresso da C (mol / m 3 ), l'indice universale del gas della sua costante è indicato dalla lettera R, e T è il livello termodinamico della temperatura p-ra.
Ad
La formula è simile alla legge del gas ideale. Particelle nell'aria gas perfetto in un mezzo solvente di tipo viscoso, le somiglianze nelle loro proprietà indicano anche le loro caratteristiche comuni. Questa affermazione conferma un certo numero di esperimenti condotti da J. B. Perrin nel 1906. Osservò il processo di distribuzione delle particelle di emulsione di resina gummigovoy nella colonna d'acqua, che generalmente obbediva alla legge di Boltzmann.
Esiste un concetto di pressione osmotica oncotica, che dipende dalla quantità di proteine nella soluzione. Come risultato della fame o della malattia renale, la concentrazione di proteine diminuirà. Per questo motivo, la pressione oncotica cadrà e appariranno edemi di natura oncotica. Ci sarà un trasferimento di acqua dai tessuti alle navi, a quei luoghi dove π onc di più. I processi purulenti causano un aumento di π onc due o tre volte. Ciò è dovuto alla distruzione delle proteine, che porta ad un aumento del numero di particelle.
L'indice osmotico stabile dovrebbe essere di circa 7,7 atm. Per questo motivo, le soluzioni isotoniche contengono tipicamente circa π di plasma = 7.7 atm. Soluzioni con π supera π di plasma , usato per rimuovere il pus dalle ferite o eliminare l'edema di natura allergica. Sono anche medicine lassative.
Vista termodinamica della pressione osmotica
La formula di Vant-Hoff utilizzata per il trattamento osmotico può essere giustificata da un punto di vista termodinamico.

L'energia libera, essendo in soluzione, corrisponderà a G = G 0 + RTlnx A + π V C. La parte molare della soluzione sarà indicata con x A , V C - questo è un indicatore del volume molare. Il termine π V C equivale all'introduzione di energia libera di pressione esterna. Il solvente puro ha G = G 0 . Se l'indice di equilibrio G del solvente corrisponde all'indicatore 0, allora otteniamo:
Ad
0 = ∇ G = G 0 + RTlnx A + π V C - G 0 = RT lnx A + π V C.
Il record risultante può essere convertito nella formula van't Hoff.
A proposito di soluzioni colloidali
La pressione osmotica della soluzione può verificarsi se sono presenti due condizioni:
- È necessaria una partizione semipermeabile (membrana).
- La presenza di due soluzioni su entrambi i lati della membrana, mentre le soluzioni devono essere di diverse concentrazioni.
La membrana cellulare può passare particelle di dimensioni specifiche, ad esempio, ammettere e rilasciare una molecola d'acqua, ma avere l'effetto opposto su C 2 H 6 O. Pertanto, utilizzando materiali speciali, che hanno anche una tale possibilità di separazione, è possibile separare i vari componenti della miscela.
Le soluzioni osmotiche sono calcolate usando π = cRT. Questa formula fu derivata da Vant-Hoff nel 1885 e gli esperimenti di Pfeffer con porosità porosa servirono da base per la sua scoperta.
Turgore in gabbia
Sia l'osmosi che l'osmosi sono componenti molto importanti di molti sistemi biologici. Se la struttura contiene un setto semipermeabile (un tessuto specifico o una parete cellulare), allora una velocità costante di osmosi d'acqua creerà troppa pressione idrostatica e, di conseguenza, si formerà un turgore che fornirà la forza e la capacità di recupero del tessuto.
Ad
Forse il fenomeno dell'emolisi, che è una rottura della membrana cellulare, come l'eritrocita a causa del suo eccessivo gonfiore quando viene posto in acqua purificata.
plasmolysis
Processi opposti si verificano quando la cellula viene posta in soluzioni di un sale di un tipo concentrato: l'acqua contenuta nella cellula si diffonderà nelle soluzioni saline attraverso la membrana. Di conseguenza, la cella si restringerà, perdendo il suo turgore di uno stato stabile. Questo fenomeno è chiamato plasmolisi. Tuttavia, il turgore può essere ripristinato posizionando la cellula plasmolizzata in acqua protoplasmatica. Il volume cellulare verrà mantenuto solo in un p-re isotonico con la stessa concentrazione (costante osmotico).
Riassumendo
Questo materiale ha permesso al lettore di familiarizzare con il concetto di trattamento osmotico, di formulare un'idea generale su di esso e di apprendere un sacco di cose interessanti. Ad esempio, la somiglianza del calcolo della formula con la formula di Van't Hoff, la somiglianza con il gas ideale, il ruolo nei processi biologici e le conseguenze che possono causare, vale a dire il turgore, la plasmolisi, l'emolisi e molto altro.