L'ozono è ... Definizione, proprietà, formula
Hai mai notato quanto è bello respirare dopo la pioggia? Questa aria rinfrescante fornisce ozono nell'atmosfera che appare dopo la pioggia. Qual è questa sostanza, quali sono le sue funzioni, la sua formula ed è davvero utile per il corpo umano? Vediamo.
Cos'è l'ozono?
Tutti coloro che hanno frequentato la scuola superiore sanno che la molecola di ossigeno è costituita da due atomi dell'elemento chimico dell'ossigeno. Tuttavia, questo elemento è in grado di formare un altro composto chimico: l'ozono. Questo nome è una sostanza, di solito si trova sotto forma di gas (sebbene possa essere presente in tutti e tre gli stati aggregativi).
La molecola di questa sostanza è abbastanza simile all'ossigeno (O 2 ), ma non è composta da due, ma da tre atomi - O 3 .
Storia della scoperta dell'ozono
L'uomo che per primo ha sintetizzato l'ozono è il fisico olandese Martin Van Marum.

Fu lui che condusse l'esperimento nel 1785 facendo passare una scarica elettrica nell'aria. Il gas risultante non ha solo acquisito un odore specifico, ma anche una tinta bluastra. Inoltre, la nuova sostanza si è rivelata un agente ossidante più forte rispetto all'ossigeno normale. Così, dopo aver considerato il suo effetto sul mercurio, Van Marum scoprì che il metallo cambiava leggermente le sue proprietà fisiche, il che non era il caso con esso sotto l'influenza dell'ossigeno.
Nonostante la sua scoperta, il fisico olandese non ha ritenuto che l'ozono sia una sostanza speciale. Solo 50 anni dopo la scoperta di Van Marum, lo scienziato tedesco Christian Friedrich Schönbein si interessò seriamente all'ozono. È grazie a lui che questa sostanza ha preso il suo nome: l'ozono (in onore della parola greca che significa "odore"), ed è stata anche più studiata e descritta.
Ozono: proprietà fisiche
Questa sostanza ha un numero di proprietà. La prima di queste è la capacità dell'ozono, come l'acqua, di essere in tre stati di aggregazione.
Lo stato normale in cui si trova l'ozono è un gas bluastro (è lui che dipinge il cielo dentro) colore azzurro) con un percepibile profumo metallico. La densità di tale gas è 2,1445 g / dm³.
Quando la temperatura diminuisce, le molecole di ozono formano un liquido blu-violetto con una densità di 1,59 g / cm³ (a -188 ° C). Far bollire il liquido O 3 a -111,8 ° C.
Mentre si trova allo stato solido, l'ozono si scurisce, diventando quasi nero con un bagliore viola-blu distinto. La sua densità è di 1,73 g / cm 3 (con -195,7 ° C). La temperatura alla quale l'ozono solido inizia a fondere è -197,2 ° C.
Il peso molecolare di O 3 è di 48 dalton.
Ad una temperatura di 0 ° C, l'ozono è perfettamente solubile in acqua e dieci volte più veloce dell'ossigeno. La presenza di impurità nell'acqua può ulteriormente accelerare questa reazione.
Oltre all'acqua, l'ozono viene sciolto in freon, il che ne facilita il trasporto.
Tra le altre sostanze in cui è facile sciogliere O 3 (nello stato di aggregato liquido) - argon, azoto, fluoro, metano, anidride carbonica, tetracloruro di carbonio.
Si miscela anche bene con ossigeno liquido (a una temperatura di 93 K).
Proprietà chimiche dell'ozono
La molecola di O 3 è piuttosto instabile. Per questo motivo, nello stato normale, esiste 10-40 minuti, dopo di che si decompone, formando una piccola quantità di calore e ossigeno O 2 . Questa reazione può verificarsi molto più rapidamente se si usano come catalizzatori l'aumento della temperatura ambiente o una diminuzione della pressione atmosferica. Inoltre, la decomposizione dell'ozono e contribuisce al suo contatto con i metalli (eccetto oro, platino e iridio), ossidi o sostanze di origine organica.
Interazione con acido nitrico ferma la decomposizione di O 3 . Contribuisce anche a questa sostanza di conservazione ad una temperatura di -78 ° C.
La principale proprietà chimica dell'ozono è la sua ossidabilità. Uno dei prodotti di ossidazione è sempre ossigeno.
In varie condizioni, O 3 è in grado di interagire con quasi tutte le sostanze e gli elementi chimici, riducendo la loro tossicità trasformandoli in meno pericolosi. Ad esempio, i cianuri sono ossidati da lui a cianati, che sono molto più sicuri per gli organismi biologici.
Come viene estratto?
Al fine di ottenere e preservare una sostanza instabile come l'ozono, vengono utilizzate le sue proprietà fisiche e chimiche.
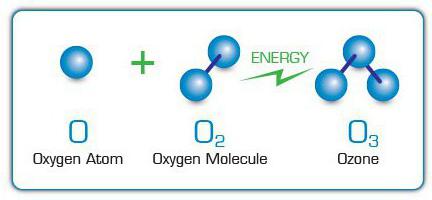
Il più delle volte, per l'estrazione di O 3 da parte dell'ossigeno è sottoposto a corrente elettrica. Per separare la miscela risultante di ossigeno e ozono, usano la proprietà di quest'ultimo per liquefare meglio di O 2 .
Nei laboratori chimici, a volte O 3 viene estratto dalla reazione di un concentrato di acido solforico raffreddato con perossido di bario.
Nelle istituzioni mediche che usano l'O 3 per il recupero dei pazienti, questa sostanza si ottiene irradiando O2 con l'ultravioletto (a proposito, questa sostanza si forma nell'atmosfera della Terra sotto l'azione della luce solare).
L'uso di O3 in medicina e nell'industria
La semplice struttura dell'ozono, la disponibilità del materiale sorgente per la sua estrazione, contribuisce all'utilizzo attivo di questa sostanza nell'industria.
Essendo un forte agente ossidante, può disinfettare molto meglio del cloro, della formaldeide o dell'ossido di etilene, pur non essendo così tossico. Pertanto, O 3 è spesso usato per sterilizzare strumenti medici, attrezzature, forme e molti altri farmaci.
Nell'industria, questa sostanza viene spesso utilizzata per pulire o estrarre molte sostanze chimiche.
Un'altra industria è l'uso di carta sbiancante, tessuti, oli minerali.
Nell'industria chimica, O 3 non solo aiuta a sterilizzare attrezzature, utensili e contenitori, ma è anche usato per disinfettare i prodotti stessi (uova, cereali, carne, latte) e aumentare la loro durata. Infatti, è considerato uno dei migliori conservanti per i prodotti, poiché non è tossico e non cancerogeno e uccide perfettamente anche le spore della muffa e altri funghi e batteri.

Nelle panetterie, l'ozono viene utilizzato per accelerare la fermentazione del lievito.
Inoltre, con l'aiuto di O 3, il brandy viene invecchiato artificialmente e gli oli grassi vengono raffinati.
In che modo l'ozono influisce sul corpo umano?
A causa di questa somiglianza con l'ossigeno, c'è un equivoco che l'ozono è una sostanza utile per il corpo umano. Tuttavia, questo non è il caso, dal momento che O 3 è uno dei più forti ossidanti che possono distruggere i polmoni e uccidere tutti coloro che inalano eccessivamente questo gas. Non c'è da stupirsi che le organizzazioni ambientaliste di ogni paese controllino rigorosamente la concentrazione di ozono nell'atmosfera.
Se l'ozono è così cattivo, perché fa sempre più facile respirare dopo la pioggia?

Il fatto è che una delle proprietà di O 3 è la sua capacità di uccidere i batteri e purificare le sostanze dalle impurità nocive. L'ozono inizia a formarsi durante la pioggia. Questo gas influisce sulle sostanze tossiche contenute nell'aria, le scinde e purifica l'ossigeno da queste impurità. È per questo motivo che l'aria dopo la pioggia è così fresca e piacevole, e il cielo acquista un bel colore azzurro.
Queste proprietà chimiche dell'ozono, che gli consentono di purificare l'aria, sono state recentemente utilizzate attivamente per curare le persone affette da varie malattie respiratorie, nonché per pulire aria, acqua e varie procedure cosmetiche.
Oggi attivamente pubblicizzato ozonizzatori domestici, purificando l'aria in casa con l'aiuto di questo gas. Anche se questa tecnica sembra essere molto efficace, finora gli scienziati non hanno studiato l'effetto di una grande quantità di aria purificata da ozono sul corpo. Per questo motivo, eccessivamente trascinato dall'ozonizzazione non ne vale la pena.