Proprietà dei sali: fisico e chimico
Ogni giorno ci confrontiamo con i sali e non pensiamo nemmeno al ruolo che svolgono nella nostra vita. Ma senza di loro, l'acqua non sarebbe così gustosa, e il cibo non porterebbe piacere, e le piante non crescerebbero, e la vita sulla terra non potrebbe esistere se non ci fosse sale nel nostro mondo. Quindi quali sono queste sostanze e quali proprietà dei sali le rendono indispensabili?
Cos'è il sale
In composizione, è la classe più numerosa, caratterizzata dalla diversità. это продукт реакции между кислотой и основанием, при которой водородный атом заменяется металлическим. Già nel 19 ° secolo, il chimico J. Vercelius definiva il sale - questo è il prodotto della reazione tra un acido e una base, in cui l'atomo di idrogeno viene sostituito da uno metallico. In acqua, i sali vengono solitamente dissociati in un metallo o ammonio (catione) e un residuo acido (anione).

Puoi ottenere il sale nei seguenti modi:
- dall'interazione di metallo e non metallo, in questo caso sarà privo di ossigeno;
- quando un metallo interagisce con un acido, si ottiene il sale e si libera l'idrogeno;
- il metallo può spostare un altro metallo dalla soluzione;
- кислотного и основного (еще их называют оксидом неметалла и оксидом металла соответственно); nell'interazione di due ossidi , acidi e basici (sono anche chiamati ossido non metallico e ossido metallico, rispettivamente);
- la reazione dell'ossido di metallo e l'acido producono sale e acqua;
- la reazione tra la base e l'ossido non metallico dà anche sale e acqua;
- usando una reazione di scambio ionico, varie sostanze idrosolubili (basi, acidi, sali) possono reagire, ma la reazione procederà se nell'acqua si formano gas, acqua o sali leggermente solubili (insolubili).
Le proprietà dei sali dipendono solo dalla composizione chimica. Ma prima, guardiamo le loro classi.
classificazione
A seconda della composizione, si distinguono le seguenti classi di sali:
- sul contenuto di ossigeno (contenente ossigeno e senza ossigeno);
- sull'interazione con l'acqua (solubile, scarsamente solubile e insolubile).
Una tale classificazione non riflette pienamente la diversità delle sostanze. La classificazione moderna e più completa, che riflette non solo la composizione, ma anche le proprietà dei sali, è presentata nella seguente tabella.
| Il sale | |||||
|---|---|---|---|---|---|
| normale | aspro | principale | doppio | ibrido | complesso |
| L'idrogeno è completamente sostituito | Gli atomi di idrogeno sono sostituiti dal metallo non completamente | I gruppi base sono sostituiti da un residuo acido non completamente | Composto da due metalli e un residuo acido | Composto da un metallo e due residui acidi | Sostanze complesse costituite da un complesso catione e anione o catione e anione complesso |
| NaCl | KHSO 4 | FeOHSO 3 | KNaSO 4 | CaClBr | [Cu (NH 3 ) 4 ] SO 4 |
Proprietà fisiche
Per quanto ampia possa essere la classe di queste sostanze, è possibile individuare le proprietà fisiche generali dei sali. Queste sono sostanze di struttura non molecolare, con un reticolo cristallino ionico.
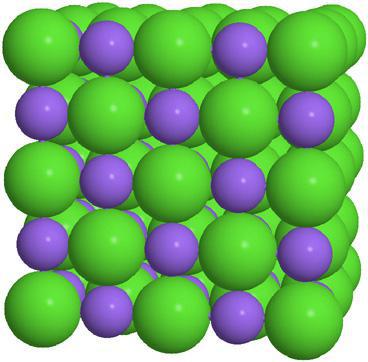
Punti di fusione e di ebollizione molto alti. In condizioni normali, tutti i sali non conducono elettricità, ma la maggior parte di essi sono perfettamente conduttivi in soluzione.
Il colore può essere molto diverso, dipende dallo ione metallico, che ne fa parte. Il solfato ferroso (FeSO 4 ) è verde, il cloruro ferrico (FeCl 3 ) è rosso scuro e il cromato di potassio (K 2 CrO 4 ) è un bel colore giallo brillante. Ma la maggior parte dei sali è ancora incolore o bianca.
Ad

La solubilità in acqua varia anche e dipende dalla composizione degli ioni. In linea di principio, tutte le proprietà fisiche dei sali hanno una caratteristica. Essi dipendono da quale ione metallico e quale residuo acido è incluso nella composizione. Continuiamo a considerare il sale.
Proprietà chimiche dei sali
Anche qui c'è una caratteristica importante. Così come le proprietà fisiche e chimiche dei sali dipendono dalla loro composizione. E anche su quale classe appartengono.

Ma le proprietà generali dei sali possono ancora essere distinte:
- molti di essi si decompongono quando riscaldati per formare due ossidi: acido e base e senza ossigeno - metallo e non metallo;
- i sali interagiscono con altri acidi, ma la reazione procede solo se il sale contiene un residuo acido di un acido debole o volatile, oppure il risultato è un sale insolubile;
- l'interazione con alcali è possibile se il catione forma una base insolubile;
- la reazione è possibile tra due diversi sali, ma solo se uno dei sali appena formati non si scioglie in acqua;
- una reazione può verificarsi con il metallo, ma è possibile solo se prendiamo il metallo situato a destra del campo di tensione dal metallo contenuto nel sale.
Le proprietà chimiche dei sali normali sono discusse sopra, mentre altre classi reagiscono con sostanze in un modo leggermente diverso. Ma la differenza è solo sui prodotti in uscita. Fondamentalmente, tutte le proprietà chimiche dei sali sono preservate, così come i requisiti per le reazioni.