Soda Ash: proprietà fisico-chimiche e produzione
Caratteristiche fisico-chimiche
Il carbonato di sodio esternamente è una polvere incolore di una struttura cristallina che è facilmente solubile in un mezzo acquoso ed è caratterizzata da un tipo di reazione chimica fortemente alcalina. Questa sostanza è caratterizzata da una maggiore igroscopicità, assorbe intensivamente umidità e anidride carbonica nell'aria, contribuendo alla formazione di sali acidi di NaHCO 3. Nel caso di stoccaggio all'aria aperta, la soda è soggetta a rapida agitazione. Questo composto chimico funge da principale reagente per il legame degli ioni calcio. Come tale, viene utilizzato quando è necessario convertire l'argilla calcica in argilla sodica.

Produzione di ceneri di soda
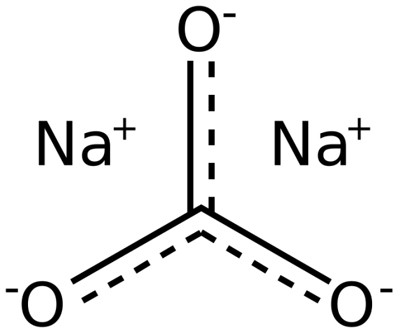
Carbonato di sodio, Denominato carbonato di sodio (Na 2 CO 3 ), è uno dei prodotti più importanti nell'industria chimica. Non una singola sfera dell'economia nazionale può fare a meno di questa sostanza oggi. Oggi, vetro, sapone, tessile, olio, pasta di legno e carta e molte altre aree dell'industria consumate in grandi quantità di carbonato di sodio. Anche il suo uso nella vita di tutti i giorni è noto. E sebbene questa sostanza si trovi in natura sotto forma di minerale trona, non è sufficiente per soddisfare esigenze industriali sempre crescenti. Già nel diciottesimo secolo c'era un'urgente necessità della sua produzione aggiuntiva. Il primo metodo industriale per ottenere il carbonato di sodio fu sviluppato e introdotto da Leblanc nel 1791. L'essenza di questo metodo è la calcinazione ad una temperatura di 1000 ° C di mirabilite disidratata con un componente di carbone e calcare. Quando si tratta la fusione con acqua calda, l'idrolisi del solfuro di calcio si verifica con la formazione di idrogeno solforato e idrossido di calcio scarsamente solubile, mentre la soda si deposita nella soluzione.
Ad
Metodo Solvay
Attualmente, il carbonato di sodio su scala industriale viene prodotto secondo il metodo proposto dal chimico e industriale di processo belga Ernest Solvay. Questo metodo si basa sulle proprietà della debole solubilità del bicarbonato di sodio in soluzioni saline ad alta concentrazione. Attraverso la soluzione di acqua-ammoniaca, che è satura cloruro di sodio, il biossido di carbonio è passato. Il NaHCO 3 risultante, in quanto meno solubile in questo terreno, precipita come un precipitato fine. Per ottenere direttamente carbonato di sodio, il bicarbonato recuperato è calcinato (calcinato). Questo metodo è perfettamente applicabile alla sintesi di Na 2 CO 3 su scala industriale, poiché è altamente economico e la relativa semplicità del processo. Oggi la produzione mondiale di carbonato di sodio è di circa 30 milioni di tonnellate. all'anno
Ad

Aspetti ecologici dell'ottenimento di Na 2 CO 3
Dal filtrato rimanente dopo la separazione del bicarbonato, sotto l'influenza di calce idrata l'ammoniaca viene rigenerata L'unico sottoprodotto della produzione di carbonato di sodio è cloruro di calcio, il riciclaggio di cui è un grave problema ambientale. I tentativi di utilizzare questa sostanza per combattere le condizioni del ghiaccio portano alla salinizzazione del suolo e alla forte inibizione della copertura vegetale. Ora per eliminare la glassa Paesi europei più spesso usato più acetato di ammonio ecocompatibile. Un altro fatto interessante è che, all'alba del XX secolo, il metodo di produzione di cloruro di potassio (una sostanza che è in gran parte simile nella sua struttura chimica alla soda) secondo lo schema Solvay, ma con la sostituzione dell'ammoniaca tossica con trimetilammina, è stato brevettato in Francia. Tuttavia, questa tecnica non ha avuto un'ampia applicazione a causa dell'elevato costo di quest'ultima. In conclusione, vorrei aggiungere che l'elevata solubilità di Na 2 CO 3 è dovuta alle peculiarità della struttura chimica di questa sostanza, in particolare alla presenza di legami idrogeno tra gli anioni, grazie ai quali gli ioni bicarbonato sono combinati in dimeri.