Acido nitrico: proprietà, preparazione e uso
introduzione
 Sei interessato alla floricoltura e sei venuto al negozio per comprare fertilizzante per i tuoi fiori. Revisionando i vari nomi e composizioni, hai notato una bottiglia con la scritta "Concime azotato". Leggiamo la sua composizione: "Fosforo, calcio, quello ... quell'acido nitrico? E che cos'è quella bestia?!". Di solito con acido nitrico familiarizzare in una situazione del genere. E molti poi vogliono sapere di più su di esso. Oggi proverò a soddisfare la tua curiosità.
Sei interessato alla floricoltura e sei venuto al negozio per comprare fertilizzante per i tuoi fiori. Revisionando i vari nomi e composizioni, hai notato una bottiglia con la scritta "Concime azotato". Leggiamo la sua composizione: "Fosforo, calcio, quello ... quell'acido nitrico? E che cos'è quella bestia?!". Di solito con acido nitrico familiarizzare in una situazione del genere. E molti poi vogliono sapere di più su di esso. Oggi proverò a soddisfare la tua curiosità.
definizione
L'acido nitrico (formula HNO 3 ) è un acido monobasico forte. Nello stato non ossidato, appare come nella foto 1. In condizioni normali, è liquido, ma può essere convertito in uno stato solido di aggregazione. E in esso assomiglia a cristalli con un reticolo monoclino o rombico.
Ad
Proprietà chimiche dell'acido nitrico
 Ha la capacità di mescolarsi bene con l'acqua, dove si verifica una dissociazione quasi completa di questo acido in ioni. L'acido nitrico concentrato ha un colore marrone (foto). È fornito dalla decomposizione in biossido di azoto, acqua e ossigeno, che è dovuto alla luce del sole che cade su di esso. Se è riscaldato, si verificherà la stessa decomposizione. Tutti i metalli reagiscono con esso, ad eccezione del tantalio, dell'oro e dei platinoidi (rutenio, rodio, palladio, iridio, osmio e platino). Tuttavia, la sua connessione con acido cloridrico può persino dissolversi alcuni di loro (questa è la cosiddetta "vodka reale"). L'acido nitrico, che ha una qualsiasi concentrazione, può manifestarsi come agente ossidante. molti materia organica quando interagisce con esso può accendersi spontaneamente. E alcuni metalli in questo acido saranno passivati. Quando esposti a loro (e anche quando reagiscono con ossidi, carbonati e idrossidi), l'acido nitrico forma i suoi sali, chiamati nitrati. Questi ultimi si dissolvono bene in acqua. Ma gli ioni nitrati in esso non vengono idrolizzati. Se i sali di un dato acido vengono riscaldati, saranno irreparabilmente decomposti.
Ha la capacità di mescolarsi bene con l'acqua, dove si verifica una dissociazione quasi completa di questo acido in ioni. L'acido nitrico concentrato ha un colore marrone (foto). È fornito dalla decomposizione in biossido di azoto, acqua e ossigeno, che è dovuto alla luce del sole che cade su di esso. Se è riscaldato, si verificherà la stessa decomposizione. Tutti i metalli reagiscono con esso, ad eccezione del tantalio, dell'oro e dei platinoidi (rutenio, rodio, palladio, iridio, osmio e platino). Tuttavia, la sua connessione con acido cloridrico può persino dissolversi alcuni di loro (questa è la cosiddetta "vodka reale"). L'acido nitrico, che ha una qualsiasi concentrazione, può manifestarsi come agente ossidante. molti materia organica quando interagisce con esso può accendersi spontaneamente. E alcuni metalli in questo acido saranno passivati. Quando esposti a loro (e anche quando reagiscono con ossidi, carbonati e idrossidi), l'acido nitrico forma i suoi sali, chiamati nitrati. Questi ultimi si dissolvono bene in acqua. Ma gli ioni nitrati in esso non vengono idrolizzati. Se i sali di un dato acido vengono riscaldati, saranno irreparabilmente decomposti.
reception
Per ottenere l'acido nitrico, l'ammoniaca sintetica viene ossidata usando catalizzatori al platino-rodio fino a quando non appare una miscela di gas nitrosi che viene successivamente assorbita dall'acqua. Si forma anche quando mescolato e riscaldato. nitrato di potassio e ferro vetriolo. 
applicazione
Con l'aiuto di acido nitrico produce fertilizzanti minerali, esplosivi e alcune sostanze tossiche. Ha inciso forme stampate (lastre di incisione, cliché di magnesio, ecc.) E soluzioni di tonificazione acidificate per foto. Coloranti e droghe sono prodotti dall'acido nitrico e vengono anche utilizzati per determinare la presenza di oro nelle leghe d'oro.
Ad
Impatto fisiologico
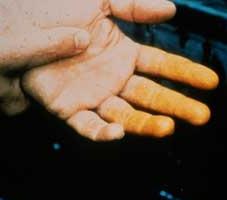
Dato il grado di influenza dell'acido nitrico sul corpo, si riferisce alla terza classe di pericolo (moderatamente pericolosa). L'inalazione dei suoi vapori porta all'irritazione delle vie respiratorie. Quando applicato sulla pelle, l'acido nitrico lascia molte ulcere a lunga durata. Le aree di pelle dove è diventato diventano un caratteristico colore giallo (foto). Scientificamente parlando, si verifica la reazione di xantoproteina. Il biossido di azoto, che viene prodotto riscaldando l'acido nitrico o scomponendolo alla luce, è molto tossico e può causare edema polmonare.
conclusione
L'acido nitrico avvantaggia una persona in uno stato sia diluito che puro. Ma il più delle volte si trova nella composizione di sostanze, molte delle quali probabilmente lo conoscete (per esempio la nitroglicerina).