Enzimi proteolitici. Proprietà degli enzimi. Azione di enzimi proteolitici
La digeribilità del cibo dipende in gran parte dalla qualità della sua elaborazione nel corpo umano. La digestione del cibo è considerata un processo complesso, in cui sono coinvolti composti altamente attivi di origine proteica, che possono accelerare il processo di scissione di proteine, carboidrati, molecole lipidiche in frammenti più piccoli.
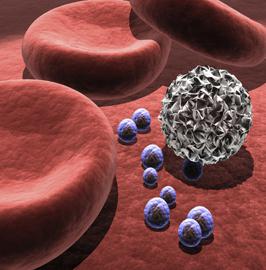
Enzimi digestivi
enzimi sistema digestivo sono prodotti dalle cellule delle ghiandole, il cui segreto è secreto nel tratto digestivo. Il processo di scissione di composti complessi è strettamente selettivo, quindi ci sono gruppi principali di enzimi che possono influenzare solo nucleotidi, proteine, carboidrati, molecole di grassi.
Azione degli enzimi digestivi
Gli enzimi del tubo digerente si dividono in lipasi, proteasi, amilasi, nucleasi, nucleotidasi.
Le lipasi sono enzimi prodotti da cellule secretorie nel pancreas e nello stomaco. Il loro scopo principale è quello di abbattere i lipidi e inserirli nel sangue.
L'amilasi viene utilizzata per digerire i componenti di carboidrati del cibo in modo che i singoli frammenti possano facilmente penetrare nel flusso sanguigno. Tali enzimi includono amilasi e maltasi nella saliva del cavo orale, lattasi nel pancreas e succo intestinale.
Ad

Le secrezioni pancreatiche possono fendere acidi nucleici ai nucleotidi, e quelli a loro volta, sotto l'azione dei nucleotidasi del succo intestinale, si scindono in nucleosidi.
Composizione enzimatica di saliva
Nella cavità orale inizia il processo di digestione del cibo, che è associato alla macerazione di particelle secche con saliva e alla scissione primaria di componenti di carboidrati. Gli enzimi della saliva, in particolare l'amilasi, influenzano le molecole di amido, trasformandole in maltosio. Grassi e proteine alimentari non subiscono trasformazioni chimiche nella cavità orale.
Esistono anche tali enzimi della saliva, che sono in grado di esporre alla distruzione della parete cellulare dei batteri dannosi. Ciò si verifica a causa dell'idrolisi delle strutture del guscio di mouraine. Ecco perché la saliva ha un effetto battericida.
Ad
Caratteristiche degli enzimi digestivi
Solo l'osservanza di una corretta alimentazione e l'assenza di cattive abitudini consentiranno agli organi digestivi di lavorare in piena forza.
Una temperatura adatta per il normale funzionamento degli enzimi nel corpo è 36,6-37 gradi. I piatti caldi causano ustioni della membrana mucosa nell'esofago e la distruzione dei composti enzimatici. Si verifica uno spasmo dei muscoli lisci della parete gastrica, a seguito del quale il cibo non preparato entra nel duodeno. Ciò porta a disturbi intestinali ea tutti i tipi di malattie. organi digestivi.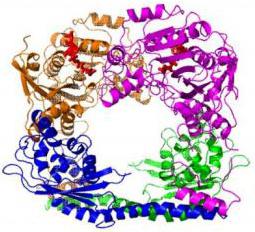
Il pH dell'ambiente influenza le proprietà degli enzimi, in particolare la loro attività. A diverse concentrazioni di ioni idrogeno, i siti attivi della proteina enzimatica e il substrato sono ionizzati a vari gradi.
Le proprietà specifiche degli enzimi sono correlate al riconoscimento della struttura chimica delle sostanze che subiscono la scissione. Anche per due isomeri di una sostanza, ci sono enzimi.
Cosa sono gli enzimi proteolitici?
Le proteasi sono enzimi idrolitici che possono scindere i legami di peptidi e proteine e ripristinare batteri benefici nell'intestino. La presenza di chimosina e pepsina nel succo gastrico, chimotripsina, tripsina, erepsina nella secrezione intestinale, carbossipeptidasi nel succo pancreatico indica una varietà di enzimi proteolitici.
Ad
A causa della specificità posizionale e di substrato di questi enzimi, viene selezionata una lacuna nella lunga catena peptidica della proteina idrolizzabile o della molecola peptidica.
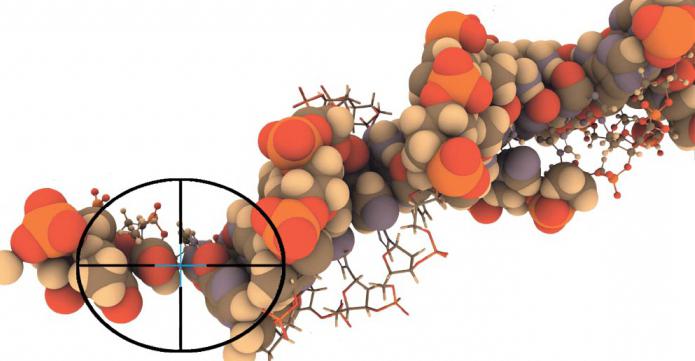
Gli enzimi proteolitici, a seconda del sito di azione, sono exopeptidasi, che sono in grado di rompere i legami terminali e le endopeptidasi, che svolgono l'idrolisi dei legami interni in una molecola proteica.
I legami peptidici a C e N-terminale della catena proteica vengono scissi da carbossipeptidasi e aminopeptidasi correlati a exopeptidasi. Esistono anche dipeptidasi che rompono il legame nei dipeptidi.
Le endopeptidasi, a seconda della struttura dell'elemento attivo, sono suddivise in:
- la serina, come parte del loro centro attivo contiene residui di serina e istidina;
- la cisteina, nella composizione del loro centro attivo contiene il gruppo SH dal residuo di cisteina;
- carbossile, come parte del loro centro attivo contiene gruppo COOH dal residuo asparaginata;
- la metalloproteinasi, come parte del centro attivo contiene uno ione metallico.
La struttura aminoacidica dei residui, i loro radicali e la configurazione spaziale del substrato influenzano la selettività delle proteasi. La maggior parte delle proteasi risponde a una struttura specifica di residui di amminoacidi localizzati vicino al legame che si rompe. Ad esempio, l'enzima tripsina catalizza la scissione di un composto tra amminoacidi basici (lisina e arginina) che hanno un gruppo carbossilico.
Gli enzimi proteolitici come la chimotripsina, la pepsina reagiscono ai residui idrofobi di fenilalanina, tirosina, triptofano e leucina e rompono i legami vicino a loro. Per l'azione dell'elastasi del succo pancreatico, è importante che il residuo amminoacidico abbia un piccolo ramo laterale, che si trova in alanina e serina.
Ad
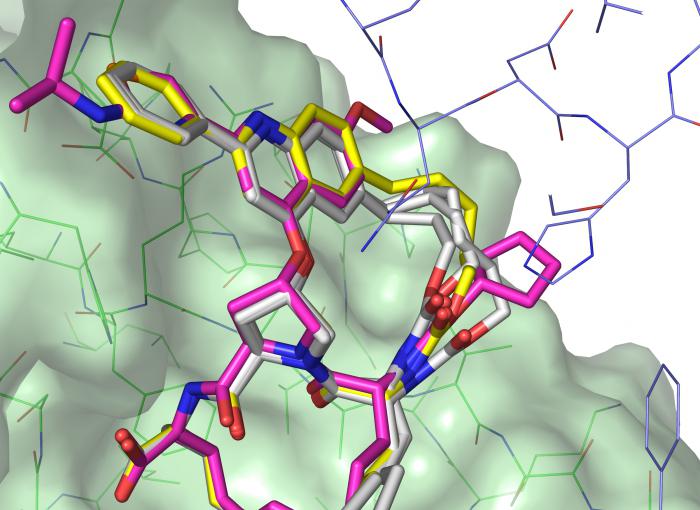
Struttura degli enzimi proteolitici
La molecola della proteasi è una catena lineare di amminoacidi che è piegata in un globulo e ha un effetto unico sulle proteine. La superficie degli enzimi proteolitici ha una cavità per legare il substrato. 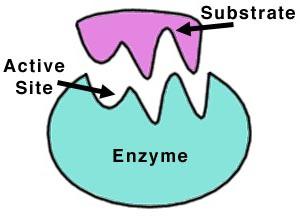
Diverse catene proteiche possono essere combinate in un complesso, e globuli raccolti in questo modo formano la struttura terziaria degli enzimi. Per l'attivazione di molte proteasi, i cofattori sono ioni Ca 2+ e Mg 2+ .
Ci sono enzimi proteolitici che sono collegati alla membrana cellulare e agiscono su una specifica struttura proteica. Un esempio è la proteasi del segnale responsabile del trasporto di molecole proteiche dalle cellule alla regione extracellulare.
Inibizione di enzimi proteolitici
Alcune malattie dell'apparato digerente sono causate dall'eccessiva attività delle proteasi, ad esempio lo stato di pancreatite acuta. Gli attivatori di enzimi prodotti dal pancreas sono citochinasi. Con il loro aiuto, la tripsina è formata da tripsinogeno, proelastasi, kallikreinogen, chimotripsinogeno che si trasformano in forme attive di enzimi. Come risultato della loro azione nel pancreas, si osserva la digestione dei tessuti con il loro segreto, seguito da gonfiore ed emorragia di questo organo.
Ad
Gli inibitori degli enzimi proteolitici mirano a sopprimere la loro attività enzimatica. Usa per iniezione endovenosa le droghe sulla base di trasilolo, panthripin e kontrikala possono ridurre l'attività delle proteasi e ridurre l'infiammazione nel pancreas.
La gravità della malattia dipende in gran parte dal sistema inibitorio della tripsina. Con un contenuto sufficiente della sostanza inibitrice, la neutralizzazione dell'enzima attivato avviene con il ripristino dell'equilibrio. La mancanza di inibitori porta a un ulteriore sviluppo della malattia.
Il ruolo delle proteasi
Molti processi nel corpo umano sono influenzati dall'azione degli enzimi proteolitici. Senza la loro partecipazione, la fecondazione, la coagulazione delle proteine del sangue, la fibrinolisi, la biosintesi delle molecole proteiche, le reazioni immunitarie, la regolazione ormonale non si verificherà.
Interruzione delle cause della proteasi distrofia muscolare, malattie di natura autoimmune, enfisema polmonare, infiammazione del pancreas.
Sulla base di enzimi proteolitici, sono stati sviluppati numerosi farmaci che consentono di correggere la digestione, guarire le ferite e le ustioni.
Proteasi utilizzato per la produzione di cibo per la somministrazione parenterale, per la produzione di farmaci a base di ormoni e antibiotici.
Gli enzimi sono ottenuti dagli organi interni e dalle ghiandole degli animali (bovini e suini) e da un substrato vegetale (lattice di frutta di un albero di melone).