Redox Reactions (ORR): esempi
Cos'è l'IAD? Esempi di tali reazioni possono essere trovati non solo inorganici, ma anche in chimica organica. Nell'articolo daremo le definizioni dei termini principali usati nell'analisi di tali interazioni. Inoltre, presenteremo alcune ERI, esempi e soluzioni di equazioni chimiche che aiuteranno a capire l'algoritmo delle azioni.

Definizioni di base
Ma prima, ricordiamo le definizioni di base che aiuteranno a capire il processo:
- Un ossidante è un atomo o uno ione capace di accettare gli elettroni nel processo di interazione. Sotto forma di agenti ossidanti gravi sono gli acidi minerali, il permanganato di potassio.
- Un agente riducente è uno ione o un atomo che dona elettroni di valenza ad altri elementi.
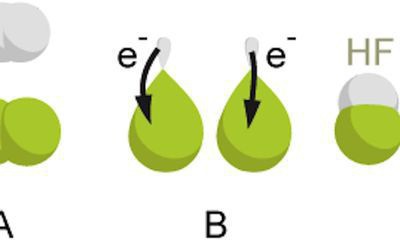
- Il processo di collegamento degli elettroni liberi è chiamato ossidazione, mentre il rinculo è chiamato riduzione.
Algoritmo di azione
Come smontare l'equazione ia Gli esempi offerti ai laureati delle scuole suggeriscono la distribuzione dei coefficienti mediante bilancia elettronica. Ecco la procedura:
- Innanzitutto, è necessario impostare i valori degli stati di ossidazione per tutti gli elementi in sostanze semplici e complesse coinvolte nella trasformazione chimica proposta.
- Quindi, selezionare quegli elementi che hanno cambiato il valore digitale.
- I segni "+" e "-" indicano gli elettroni ricevuti e dati, il loro numero.
- Inoltre, tra loro determinare il più piccolo multiplo comune, determinare i coefficienti.
- I numeri risultanti inseriscono l'equazione di reazione.
Primo esempio
Come completare l'attività relativa a IAD? Gli esempi offerti agli esami finali di grado 9 non implicano l'aggiunta di formule di sostanze. I ragazzi, di regola, devono determinare i coefficienti e le sostanze che hanno modificato i valori di valenza.
Ad
Considera quelle IAD (reazioni), esempi dei quali sono offerti ai diplomati dell'11 ° grado. Gli scolari dovrebbero integrare autonomamente l'equazione con le sostanze e solo dopo che il saldo elettronico disponga i coefficienti:
H 2 O 2 + H 2 SO 4 + KMnO 4 = Mn SO 4 + O 2 + ... + ...
Per cominciare, organizzeremo gli stati di ossidazione in ogni composto. Quindi, nel perossido di idrogeno nel primo elemento corrisponde a +1 , in ossigeno -1 . Nell'acido solforico, i seguenti indicatori: +1, +6, -2 (in totale, otteniamo zero). L'ossigeno è una sostanza semplice, quindi ha un tasso di ossidazione pari a zero.
il permanganato di potassio, e anche in manganese solfato (2) otteniamo i seguenti valori:
K + Mn +7 O 4 -2 , Mn +2 S +6 O 4 -2
Mettendo i valori degli elementi proposti nell'attività, è necessario completare la IAD. Esempi di tali interazioni sono simili, quindi la soluzione richiede l'identificazione di atomi (ioni) che mostrano proprietà ossidanti e riducenti.
Ad
Quindi, poiché uno dei prodotti mancanti della reazione sarà il sale di potassio, cioè il solfato. La seconda sostanza è l'acqua, poiché il processo coinvolge l'acido solforico con proprietà igroscopiche.
Il prossimo passo sarà la preparazione del bilancio elettronico di questo processo:
- 2O - dà 2 elettroni = O 2 0 5 (agente riducente);
- Mn +7 accetta 5 elettroni = Mn + 2 2 (ossidante).
Nel processo di disposizione dei coefficienti, sommiamo necessariamente gli atomi di zolfo, otteniamo l'equazione pronta del processo:
5H 2 O 2 + 3H 2 SO 4 + 2KMnO 4 = 2Mn SO 4 + 5O 2 + 8H 2 O + K 2 SO 4

Momenti difficili
Quali difficoltà hanno gli scolari quando analizzano l'IAD? Gli esempi offerti nelle prove finali in chimica, i ragazzi devono finire da soli, cosa che causa loro difficoltà.
Supponiamo che lo schema proposto sia FeCl 2 + HCl + K 2 Cr 2 O 7 = FeCl 3 + CrCl 3 + ... + ...
È necessario aggiungere le sostanze mancanti e disporre i coefficienti stereochimici necessari nell'equazione. Nell'assegnazione proposta stato di ossidazione cambia ferro: da +2 a +3 , quindi, mostra le proprietà riducenti. Il bicromato di potassio agisce come un agente ossidante, abbassando il valore del grado di ossidazione da +6 a +3 .
Ad
L'acqua sarà il prodotto di reazione mancante. cloruro di potassio. Non partecipano al bilancio elettronico, poiché gli elementi nella loro composizione non mostrano un cambiamento nel loro valore numerico. Il saldo elettronico per questo processo sarà il seguente:
- Fe +2 dà 1 elettrone = Fe +3 6 (agente riducente);
- 2Cr +6 richiede 6 e = 2Cr +3 1 (ossidante).
Quando si posizionano i coefficienti in questo schema, riassumiamo gli atomi di cloro:
6 FeCl 2 + 14HCl + K 2 Cr 2 O 7 = 6 FeCl 3 + 2CrCl 3 + 2KCl + 7H 2 O
Un altro esempio di interazione
Continuiamo la conversazione su come smontare correttamente la IAD. La chimica (esempi di tali reazioni in esso sono comuni) non solo spiega l'algoritmo delle azioni, ma caratterizza anche l'essenza dei processi in atto. Considera un altro esempio dell'interazione, accompagnato dalla formazione di nuove sostanze chimiche:
Ad
KMnO 4 + H 2 SO 4 + KI = MnSO 4 + I 2 + ... + ...
In questo esempio, ci sono due elementi che cambiano il grado di ossidazione: iodio e manganese. Scopri quali sostanze saranno formate come prodotti di questa reazione chimica.
Poiché il processo prende parte acido solforico una delle sostanze formate sarà l'acqua. Nella parte destra non c'è composto in potassio, quindi il secondo prodotto sarà il solfato di questo metallo alcalino.
Il saldo elettronico per questa interazione è il seguente:
- Mn +7 richiede 5 e = Mn +2 2 , è un agente ossidante;
- 2I - dà 2e = I 2 0 5 , agisce come agente riducente.
Nella fase finale di questo compito, inseriamo i coefficienti nello schema finito e otteniamo:
2KMnO 4 + 8H 2 SO 4 + 10KI = 2MnSO 4 + 5I 2 + 6K 2 SO 4 + 8H 2 O.
conclusione
Questi processi hanno trovato una seria applicazione nell'analisi chimica. Con il loro aiuto, puoi aprire e separare vari ioni, eseguire il metodo di ossimetria.
Una varietà di metodi fisici e chimici di analisi si basa su IAD. La teoria delle interazioni acida e principale spiega la cinetica dei processi che si verificano e consente calcoli quantitativi mediante equazioni.
Affinché gli studenti che hanno scelto la chimica per passare all'esame finale superino con successo questi test, è necessario elaborare un algoritmo di equalizzazione IHB basato sul bilanciamento elettronico. Gli insegnanti lavorano con i loro studenti sul metodo di organizzazione dei coefficienti, utilizzando vari esempi di chimica organica e inorganica.
Le assegnazioni relative alla determinazione degli stati di ossidazione degli elementi chimici in sostanze semplici e complesse, così come la stesura di un equilibrio tra elettroni adottati e dati, sono un elemento indispensabile delle prove di esame al livello base e generale di allenamento. Solo in caso di completamento con successo di tali compiti possiamo parlare dell'effettiva padronanza del corso scolastico di chimica inorganica, nonché aspettarci di ricevere un punteggio elevato sull'OGE, USO.