Diossido di zolfo - proprietà fisiche, preparazione e uso
Il biossido di zolfo ha una struttura molecolare simile all'ozono. L'atomo di zolfo situato nel centro della molecola è legato a due atomi di ossigeno. Questo prodotto gassoso di ossidazione dello zolfo non ha colore, produce un forte odore e quando le condizioni cambiano si condensa facilmente in un liquido limpido. La sostanza è ben solubile in acqua, ha proprietà antisettiche. L'SO 2 è prodotto in grandi quantità nell'industria chimica, in particolare nel ciclo di produzione dell'acido solforico. Il gas è ampiamente utilizzato per la lavorazione di prodotti agricoli e alimentari, tessuti per sbiancatura nell'industria tessile.
Nomi di sostanze sistematiche e banali
È necessario comprendere la varietà di termini relativi allo stesso composto. Il nome ufficiale del composto, la cui composizione chimica riflette la formula SO 2 , è il biossido di zolfo. IUPAC raccomanda di utilizzare questo termine e il suo equivalente inglese - Diossido di zolfo. I libri di testo per scuole e università citano più spesso un nome simile: l'ossido di zolfo (IV). Il numero romano tra parentesi indica la valenza dell'atomo S. L'ossigeno in questo ossido è bivalente e il numero ossidativo dello zolfo è +4. La letteratura tecnica usa termini antiquati come il biossido di zolfo, l'anidride dell'acido solforoso (il prodotto della sua disidratazione).
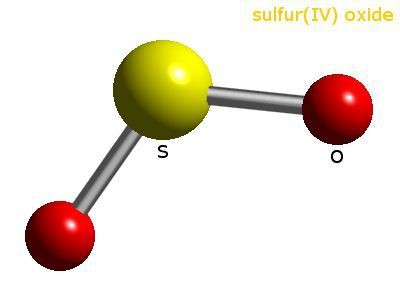
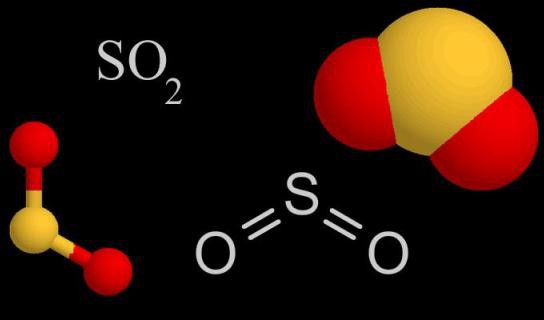
La composizione e la struttura molecolare di SO 2
La molecola SO 2 è formata da un atomo di zolfo e due atomi di ossigeno. Tra i legami covalenti c'è un angolo di 120 °. L'ibridazione sp2 si verifica nell'atomo di zolfo - sono allineati nella forma e nell'energia di una nuvola di uno e due p-elettroni. Sono coinvolti nell'educazione. legame covalente tra zolfo e ossigeno. In una coppia O - S, la distanza tra gli atomi è di 0,143 nm. L'ossigeno è un elemento più elettronegativo dello zolfo, il che significa che le coppie di legame degli elettroni vengono spostate dal centro agli angoli esterni. Anche l'intera molecola è polarizzata, il polo negativo è O atomi, quello positivo è un atomo di S.
Alcuni parametri fisici di anidride solforosa
L'ossido di zolfo tetravalente in condizioni ambientali normali preserva lo stato gassoso di aggregazione. La formula del biossido di zolfo consente di determinare la sua massa molecolare e molare relativa: Mr (SO 2 ) = 64.066, M = 64.066 g / mol (può essere arrotondato a 64 g / mol). Questo gas è quasi 2,3 volte più pesante dell'aria (M (aria) = 29 g / mol). Il diossido ha un forte odore specifico di zolfo che brucia, difficile da confondere con gli altri. È sgradevole, irrita le mucose degli occhi, provoca tosse. Ma l'ossido di zolfo (IV) non è tossico come l'idrogeno solforato.
Sotto pressione a temperatura ambiente, il diossido di zolfo gassoso si liquefa. A basse temperature, la sostanza è allo stato solido, si scioglie a -72 ... -75.5 ° C. Con un ulteriore aumento della temperatura, appare un liquido, e a -10,1 ° C, il gas si riformula. Le molecole di SO 2 sono termicamente stabili, la decomposizione in zolfo atomico e l'ossigeno molecolare si verifica a temperature molto elevate (circa 2800 ºС).

Solubilità e interazione con l'acqua
L'anidride solforosa, quando sciolta in acqua, reagisce parzialmente con essa per formare acido solforoso molto debole. Al momento del suo ricevimento, si decompone immediatamente in anidride e acqua: SO 2 + H 2 O ↔ H 2 SO 3 . In effetti, la soluzione non è presente acido solforico e idrato SO 2 molecole. Il diossido di gas gassoso interagisce meglio con l'acqua fredda, la sua solubilità diminuisce all'aumentare della temperatura. In condizioni normali, può dissolversi in 1 volume di acqua a 40 volumi di gas.
Diossido di zolfo in natura
Quantità significative di anidride solforosa vengono rilasciate con gas vulcanici e lava durante le eruzioni. Molti tipi di attività antropogeniche portano anche ad un aumento della concentrazione di SO 2 nell'atmosfera.

L'anidride solforosa viene fornita all'aria dagli impianti metallurgici, dove i gas di scarico non vengono intrappolati durante la cottura del minerale. Molti tipi di combustibili fossili contengono zolfo e, di conseguenza, quantità significative di anidride solforosa vengono rilasciate nell'aria atmosferica quando il carbone, il petrolio e il gas da essi derivati vengono bruciati. L'anidride solforosa diventa tossica per l'uomo a concentrazioni nell'aria superiori allo 0,03%. In una persona, la mancanza di respiro inizia, si possono verificare sintomi come bronchite e polmonite. Concentrazioni molto elevate di anidride solforosa nell'atmosfera possono portare a gravi avvelenamenti o morte.
Anidride solforosa - produzione in laboratorio e nell'industria
Metodi di laboratorio:
- Quando lo zolfo viene bruciato in un pallone con ossigeno o aria, il diossido viene ottenuto con la formula: S + O 2 = SO 2 .
- È possibile agire sui sali di acido solforoso con acidi inorganici più forti, è meglio prendere cloridrico, ma è possibile diluire solforico:
- Na 2 SO 3 + 2HCl = 2NaCl + H 2 SO 3 ;
- Na 2 SO 3 + H 2 SO 4 (d). = Na 2 SO 4 + H 2 SO 3 ;
- H 2 SO 3 = H 2 O + SO 2 .
3. Quando il rame interagisce con l'acido solforico concentrato, non viene rilasciato idrogeno, ma anidride solforosa:
2H 2 SO 4 (conc.) + Cu = CuSO 4 + 2H 2 O + SO 2 .
Metodi moderni di produzione industriale di anidride solforosa:
- Ossidazione dello zolfo naturale quando viene bruciato in forni speciali: S + O 2 = SO 2 .
- Pirite pirolitica (pirite).
Proprietà chimiche di base del biossido di zolfo
Il biossido di zolfo è un composto attivo chimicamente. Nei processi redox, questa sostanza agisce spesso come agente riducente. Ad esempio, nell'interazione del bromo molecolare con biossido di zolfo, i prodotti di reazione sono acido solforico e acido bromidrico. Le proprietà ossidative di SO 2 appaiono quando questo gas viene fatto passare attraverso l'acqua di idrogeno solforato. Di conseguenza, lo zolfo viene rilasciato, avviene l'auto-ossidazione: auto-riduzione: SO 2 + 2H 2 S = 3S + 2H 2 O.
Il diossido di zolfo presenta proprietà acide. Corrisponde a uno degli acidi più deboli e instabili - sulfureo. Questo composto non esiste nella sua forma pura, è possibile rilevare le proprietà acide di una soluzione di biossido di zolfo usando degli indicatori (tornasole è il rosing). L'acido solforico fornisce i sali medi - solfiti e acidi - idrosolfiti. Tra loro ci sono composti stabili.
Il processo di ossidazione dello zolfo in biossido allo stato esavalente in anidride dell'acido solforico è catalitico. La sostanza risultante è energicamente sciolta in acqua, reagisce con le molecole di H 2 O. La reazione è esotermica, si forma acido solforico, o meglio, la sua forma idratata.
Uso pratico dell'anidride solforosa
Il principale metodo di produzione industriale dell'acido solforico, che richiede l'elemento diossido, ha quattro fasi:
- Ottenere biossido di zolfo bruciando zolfo in forni speciali.
- Purificazione del biossido di zolfo risultante da tutti i tipi di impurità.
- Ulteriore ossidazione allo zolfo esavalente in presenza di un catalizzatore.
- Assorbimento di triossido di zolfo dall'acqua.
Precedentemente, quasi tutta l'anidride solforosa richiesta per la produzione di acido solforico su scala industriale era ottenuta mediante arrostimento della pirite come sottoprodotto della fabbricazione dell'acciaio. I nuovi tipi di lavorazione delle materie prime metallurgiche utilizzano meno la combustione del minerale. Pertanto, negli ultimi anni, lo zolfo naturale è diventato il principale materiale di base per la produzione di acido solforico. Riserve globali significative di questa materia prima, la sua disponibilità ci consente di organizzare elaborazioni su larga scala.

Il diossido di zolfo è ampiamente usato non solo nell'industria chimica, ma anche in altri settori dell'economia. Le fabbriche tessili usano questa sostanza e i prodotti della sua interazione chimica per sbiancare la seta e tessuti di lana. Questo è uno dei tipi di sbiancamento senza cloro, in cui le fibre non vengono distrutte.
L'anidride solforosa ha eccellenti proprietà disinfettanti, utilizzate nella lotta contro funghi e batteri. L'anidride solforosa viene sottoposta a fumigazione con stoccaggio di prodotti agricoli, botti di vino e cantine. Usato SO 2 nell'industria alimentare come conservante e sostanza antibatterica. Aggiungilo agli sciroppi, immergilo nella frutta fresca. Sulfitizatsiya
il succo di barbabietola da zucchero scolorisce e disinfetta le materie prime. Puree e succhi vegetali in scatola contengono anche anidride solforosa come agente antiossidante e conservante.
