L'acido più forte. Formula dell'acido più forte
A proposito di che tipo di acido è il più forte, ha discusso più di una generazione di chimici. In momenti diversi, questo titolo ha ricevuto azoto, solforico, acido cloridrico. Alcuni credevano che non ci potesse essere un composto più forte dell'acido fluoridrico. Recentemente, sono stati ottenuti nuovi composti con forti proprietà acide. Forse, tra loro c'è l'acido più forte del mondo? Questo articolo discute le caratteristiche degli acidi persistenti più forti del nostro tempo e fornisce le loro brevi caratteristiche chimiche.
Concetto acido 
La chimica è una scienza quantitativa esatta. E il titolo "L'acido più forte" deve essere ragionevolmente attribuito all'una o all'altra sostanza. Quale può essere l'indicatore principale che caratterizza la forza di qualsiasi connessione?
Innanzitutto, ricordiamo la definizione classica di acido. Fondamentalmente, questa parola è usata per composti chimici complessi, composti da idrogeno e residui acidi. Il numero di atomi di idrogeno nel composto dipende dalla valenza del residuo acido. Ad esempio, nella molecola di acido cloridrico esiste un solo atomo di idrogeno; e l'acido solforico ha già due atomi di H + .
Proprietà acide
Tutti gli acidi hanno certe proprietà chimiche che possono essere chiamate comuni a questa classe di composti chimici.
- La capacità di interagire con i metalli rilasciando idrogeno.
- La capacità di interagire con le basi, evidenziando i sali.
- La possibilità di cambiare il colore degli indicatori - ad esempio, per causare arrossamento della cartina di tornasole.

In tutte le proprietà sopra menzionate, si manifesta un'altra "abilità" di qualsiasi acido noto: la capacità di donare un atomo di idrogeno, sostituendolo con un atomo di un'altra sostanza chimica o una molecola di un composto. È questa capacità che caratterizza la "forza" di un acido e il grado della sua interazione con altri elementi chimici.
Acqua e acido
La presenza di acqua riduce significativamente la capacità dell'acido di rilasciare atomi di idrogeno. Questo perché l'idrogeno è in grado di formarsi legami chimici tra molecole di acido e acqua, quindi la sua capacità di separarsi dalla base è inferiore a quella degli acidi non diluiti.
superacido
La parola "superacido" fu introdotta nel dizionario chimico nel 1927, con la mano leggera del famoso chimico James Conant.
Lo standard di resistenza di questo composto chimico è acido solforico concentrato. Una sostanza chimica o una miscela che supera l'acidità dell'acido solforico concentrato è chiamata superacido. Il valore di superacido è determinato dalla sua capacità di dare un positivo carica elettrica qualsiasi motivo Per il parametro di base per la determinazione dell'acidità è stato adottato l'indicatore corrispondente di H 2 SO 4 . Tra gli acidi forti ci sono sostanze con nomi e proprietà piuttosto insoliti.
Noti acidi forti
Gli acidi più famosi del corso di chimica inorganica sono gli acidi idroiodici (HI), idrobromici (HBr), cloridrico (HCl), solforico (H 2 SO 4 ) e nitrico (HNO 3 ). Hanno tutti un alto indice di acidità e sono in grado di reagire con la maggior parte dei metalli e delle basi. In questa serie, l'acido più forte è una miscela di acido nitrico e cloridrico, chiamata "acqua regia". La formula dell'acido più forte di questa serie è HNO 3 + 3 HCl. Questo composto è in grado di sciogliere anche metalli preziosi come oro e platino.

Stranamente, l'acido fluoridrico, che è un composto di idrogeno con l'alogeno più forte - il fluoro, non è riuscito a conquistare il titolo di "L'acido più forte in chimica". L'unica caratteristica di questa sostanza è la capacità di dissolvere il vetro. Pertanto, tale acido viene immagazzinato in un contenitore di polietilene.
Acidi organici forti
Candidati per il titolo "L'acido più forte nella chimica organica" - formico e acetico L'acido. Acido formico è il più forte nella gamma omologa di acidi limitanti. Ha ricevuto il suo nome a causa del fatto che alcuni di essi sono contenuti nelle secrezioni di formiche.

L'acido acetico è leggermente più debole dell'acido formico, ma il suo spettro di distribuzione è molto più ampio. Si trova spesso nei succhi di piante e si forma durante l'ossidazione di vari prodotti organici.
I recenti sviluppi nel campo della chimica hanno permesso di sintetizzare una nuova sostanza in grado di competere con le sostanze organiche tradizionali. L'acido trifluorometansolfonico ha un indice di acidità superiore a quello dell'acido solforico. Allo stesso tempo, CF3SO3H è un liquido igroscopico stabile con proprietà fisico-chimiche consolidate in condizioni normali. Oggi, il titolo "The Strongest Organic Acid" può essere assegnato a questo composto.
Molti possono pensare che il grado di acidità non possa essere significativamente più alto del tasso di acido solforico. Ma recentemente, gli scienziati hanno sintetizzato un numero di sostanze i cui parametri di acidità sono diverse migliaia di volte superiori ai valori dell'acido solforico. I composti ottenuti dall'interazione degli acidi protonici con gli acidi di Lewis hanno valori anormalmente elevati di acidità. Nel mondo scientifico sono chiamati: acidi protonici complessi.
Acido magico
Sì. Va bene Acido magico Si chiama così. L'acido magico è una miscela di acido fluoridrico o acido solfonico di fluoro con pentafluoruro di antimonio. La formula chimica di questo composto è mostrata nella figura: 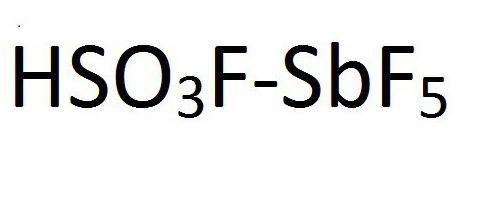
Questo strano nome di acido magico ha ricevuto alla festa di Natale dei chimici, avvenuta nei primi anni '60. Un membro del gruppo di ricerca, J. Olaha, ha mostrato un trucco divertente, dissolvendo una candela di cera in questo liquido straordinario. Questo è uno degli acidi più forti della nuova generazione, ma una sostanza che lo supera in forza e acidità è già stato sintetizzato.
L'acido più forte del mondo
L'acido carborano è acido carboranico, che è di gran lunga il composto più forte al mondo. La formula dell'acido più forte è la seguente: H (CHB11Cl11).
Questo mostro è stato creato nel 2005 presso l'Università della California, in stretta collaborazione con l'Istituto di Catalisi Novosibirsk della SB RAS.
L'idea stessa di sintesi sorse nella mente degli scienziati, insieme al sogno di nuove molecole e atomi senza precedenti. Un nuovo acido è un milione di volte più forte del solforico, mentre è completamente non aggressivo e l'acido più forte può essere facilmente conservato in una bottiglia di vetro. Tuttavia, nel tempo, il vetro si dissolve ancora e con l'aumento della temperatura il tasso di questa reazione aumenta in modo significativo. 
Questa straordinaria morbidezza è dovuta all'elevata stabilità del nuovo composto. Come tutti gli acidi prodotti chimici correlati, l'acido carborico reagisce prontamente, rinunciando al suo unico protone. La base dell'acido è così stabile che la reazione chimica non va oltre.
Proprietà chimiche dell'acido carboranico
Un nuovo acido è un eccellente donatore di protoni H + . Questo è ciò che determina la forza di questa sostanza. Una soluzione di acido carborico contiene più ioni idrogeno di qualsiasi altro acido nel mondo. Nella reazione chimica SbF 5 - pentafluoruro di antimonio, lega lo ione fluoro. Allo stesso tempo, vengono rilasciati nuovi e nuovi atomi di idrogeno. Pertanto, l'acido carborico è il più forte del mondo - la sospensione dei protoni nella sua soluzione è 2 × 10 19 volte superiore a quella dell'acido solforico.
Tuttavia, la base acida di questo composto è notevolmente stabile. La molecola di questa sostanza consiste di undici atomi di bromo e lo stesso numero di atomi di cloro. Nello spazio, queste particelle formano una figura complessa, geometricamente regolare, che è chiamata icosaedro. Questa disposizione degli atomi è la più stabile, e questo spiega la stabilità dell'acido carboranico. 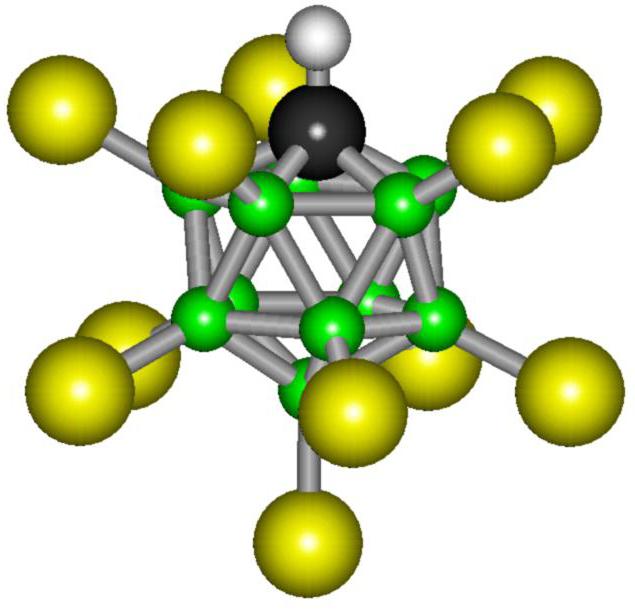
Il valore dell'acido carborico
L'acido più forte del mondo ha portato i suoi creatori a meritare premi e riconoscimenti nel mondo scientifico. Sebbene tutte le proprietà di una nuova sostanza non siano completamente comprese, sta già diventando chiaro che il significato di questa scoperta va oltre i laboratori e gli istituti di ricerca. L'acido carborico può essere utilizzato come potente catalizzatore in varie reazioni industriali. Inoltre, il nuovo acido può interagire con le sostanze chimiche più resistenti: i gas inerti. Attualmente, il lavoro è in corso, consentendo la possibilità di entrare nella reazione dello xeno.
Indubbiamente, le proprietà sorprendenti dei nuovi acidi troveranno la loro applicazione in vari campi della scienza e della tecnologia.