Acido benzoico: storia di scoperta, proprietà, preparazione, uso del reagente
La classe più ampia di composti chimici è considerata materia organica. La loro diversità è associata alla capacità unica del carbonio di creare catene atomiche con elevata stabilità. Uno dei rappresentanti di composti organici che hanno un anello benzenico è l'acido benzoico. Una storia interessante di scoperta, una vasta gamma di applicazioni, metodi di produzione, i benefici e i danni delle sostanze per gli esseri umani saranno descritti in questo articolo.
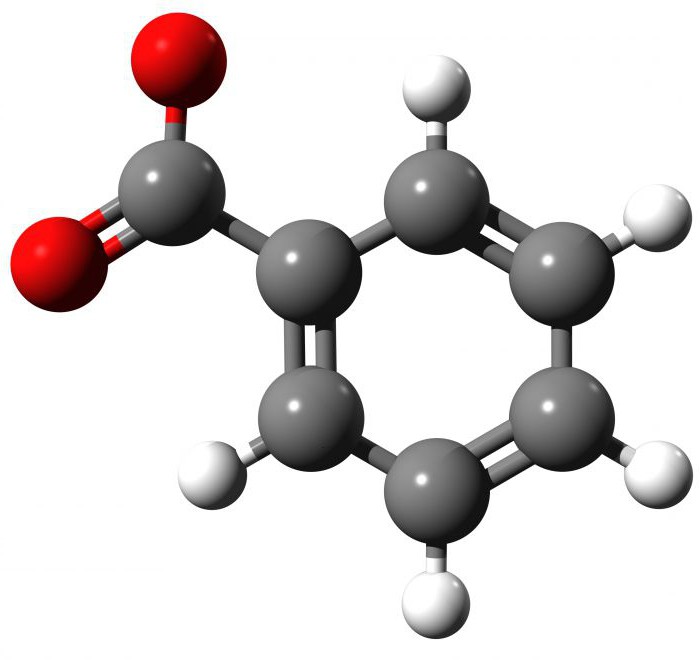
Descrizione, proprietà fisiche del composto
A temperatura ambiente, l'acido benzoico sembra una polvere bianca. Se lo esaminate al microscopio, vedrete che i cristalli sono sotto forma di aghi o scaglie (compresse). Il composto ha un forte odore. La formula chimica di questo acido (organico) carbossilico è C 6 H 5 COOH o C 7 H 6 O 2 . Quando viene scaldato a 122,4 ° C, inizia a sciogliersi ea 249 ° C - per bollire, un ulteriore aumento della temperatura a 370 ° C porterà alla decomposizione termica. È facile calcolare la massa molare del composto, è 122,12 g / mol. Il reagente è molto poco solubile in acqua, e in etanolo ed eteri - bene. Il reattivo C 6 H 5 COOH è un acido debole, la sua costante di dissociazione è 4.202.

sublimazione
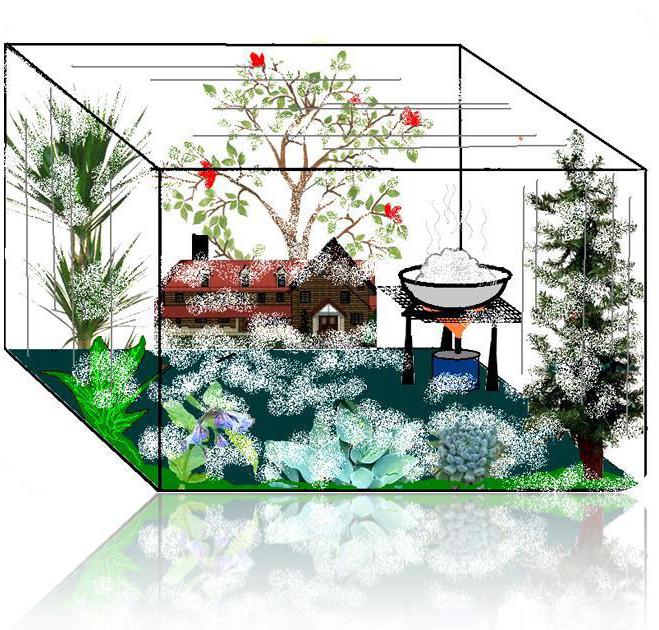
Il reagente è facile da sublimare. In questo caso, i cristalli sublimano dal vapore, bypassando la fase liquida. Una tale transizione è facile da seguire attraverso l'esperienza di "inverno in un bicchiere" o "neve artificiale". Per fare ciò, una piccola quantità di reagente e un ramoscello di abete vengono posti in piatti chimici resistenti al calore. Una fiaschetta a fondo tondo con acqua è posta sopra, servirà da frigorifero e coperchio. Il design è impostato su un treppiede e sottoposto a riscaldamento. In questo caso, il reagente inizia a sublimare. Le coppie, raggiungendo i matracci con acqua fredda, cristallizzano e diventano "neve". Si sistemano sul ramo di abete e sulle pareti del vetro sotto forma di sottili aghi. Spettacolo fantastico! Ha un'applicazione pratica - la sublimazione viene utilizzata per ottenere l'acido benzoico.
Storia della scoperta
L'acido benzoico prende il nome dal composto naturale da cui fu isolato, incenso rugiadoso. Questo processo fu descritto da Nostradamus nel 1556 e poco dopo dall'alchimista francese Blaise de Vigener. La resina di benzoino è stata a lungo considerata l'unica fonte di sintesi di acido carbossilico, per la quale è stata chiamata la neve carica. Un importante contributo allo studio della struttura e della composizione del composto è stato fatto da J. Liebig e A. Kolbe. Nel 1875 furono studiate le proprietà antisettiche e antimicotiche dell'acido benzoico. La scoperta appartiene al fisiologo tedesco E. L. Zalkowski. Questo ha permesso l'uso del reagente in medicina.
Reazioni chimiche tipiche
L'acido benzoico, le cui proprietà chimiche sono direttamente dipendenti dalla presenza di un anello aromatico, entra in una reazione di sostituzione elettrofila. Inoltre, sono più sensibili al terzo atomo di carbonio, situato ad uguale distanza dal gruppo carbossilico. La sostituzione in -COOH procede molto più lentamente. Per C 6 H 5 COOH, le stesse interazioni sono caratteristiche degli acidi carbossilici. Durante la reazione di esterificazione (con alcoli), gli esteri hanno un aroma gradevole. Come tutti composti organici l'acido benzoico brucia con il rilascio di CO 2 e acqua. Le interazioni con basi e metalli procedono attraverso il gruppo carbossilico con la formazione di sali - benzoati. La disidratazione si traduce in cicloalcani. Caratteristica chimica reazione (qualità) su C 6 H 5 COOH è il rilascio di benzoato di ferro (III). Appare come un precipitato di colore giallastro-rosato a causa dell'interazione dell'acido benzoico con FeCl 3 .
Ricezione e pulizia
Come già descritto sopra, per la prima volta l'acido benzoico è stato isolato dall'incenso rugiadoso. Questo composto naturale è una resina styrax. Per questo, la materia prima frantumata è stata riscaldata in un bagno di sabbia e cristalli sublimati sono stati raccolti in una piccola scatola ricoperta di carta. Il prodotto risultante ha un aroma gradevole dovuto alla presenza di olii essenziali nell'incenso rugiadoso - cannella e vaniglia.

È stato anche utilizzato il metodo di interazione dell'acido ippurico con acido cloridrico con forte riscaldamento. Il primo è stato ottenuto per evaporazione delle urine degli erbivori, quindi purificato per cristallizzazione fino alla scomparsa dell'odore caratteristico. Ma che dire della sintesi moderna di una sostanza come l'acido benzoico? Ottenere molto economico, semplice ed ecologico. Viene effettuato utilizzando l'ossidazione industriale del metilbenzene KMnO 4 o mediante l'interazione parziale del reagente iniziale con O 2 . La purificazione delle materie prime si basa sulle proprietà fisiche del reagente - bassa solubilità dell'acido benzoico in acqua fredda e alta in acqua calda, ed è chiamata ricristallizzazione.
Conservante indispensabile
Quando si esaminano le etichette degli alimenti, si incontrano spesso componenti codificati in codice elettronico. Sotto questa etichetta ci sono vari coloranti, aromi, emulsionanti, conservanti e esaltatori di sapidità. L'acido benzoico può essere trovato con il codice E210. Questo integratore alimentare è un conservante naturale, che viene prodotto in prodotti lattiero-caseari in modo naturale. In natura, il composto può essere trovato in varie parti di piante, resine, ruscelli di castori. E210 è utilizzato nella produzione di prodotti alimentari - salse, zuppe, gelatine, cibi in scatola, bevande. Poiché il componente è leggermente solubile in acqua, più spesso assumere sali di acido benzoico, ad esempio, benzoato di sodio con il codice E211.

L'effetto del composto sul corpo umano
Conservante E210, entrando nel corpo umano, reagisce con le proteine, formando acido ippurico, che viene escreto dai reni. Questo componente è approvato dall'associazione OMS, ma solo in una concentrazione non superiore a 5 mg / kg di assunzione giornaliera. A grandi dosi, l'acido benzoico può causare danni al fegato e ai reni. Inoltre, dovresti fare attenzione ai prodotti in cui il conservante è presente insieme alla vitamina C. L'interazione di questi componenti porta alla formazione di benzene libero, che è il più potente cancerogeno.
applicazione
L'acido benzoico ha trovato applicazione non solo nell'industria alimentare. È usato in medicina come agente disinfettante e antifungino, aggiunto a farmaci espettoranti e unguenti per le malattie della pelle. Il reagente è una materia prima per la sintesi chimica di fenoli, plastificanti e coloranti. Di grande importanza per la profumeria sono gli esteri dell'acido benzoico. Sono usati come fissatori per gli aromi. Per non farti avvelenare, dovresti usare la protezione della pelle e del polmone, perché l'ingresso del reagente nel corpo porta a ustioni, irritazione delle mucose, nausea.