Gli ioni sono carichi di atomi e gruppi atomici. Il concetto di reazioni ioniche e carica ionica
Per la prima volta il termine "ione" fu introdotto nel 1834, in cui il merito di Michael Faraday. Dopo aver studiato l'effetto della corrente elettrica su soluzioni di sali, alcali e acidi, è giunto alla conclusione che contengono particelle che hanno una certa carica. Cationi di Faraday chiamati ioni, che in un campo elettrico si spostarono verso il catodo, che ha una carica negativa. Gli anioni sono particelle ioniche non elementari caricate negativamente, che in un campo elettrico si muovono verso l'anodo positivo.
Questa terminologia viene ora utilizzata e le particelle vengono ulteriormente studiate, il che ci consente di considerare una reazione chimica come risultato dell'interazione elettrostatica. Molte reazioni procedono secondo questo principio, che ha reso possibile comprendere il loro corso e selezionare catalizzatori e inibitori per accelerare il loro decorso e inibire la sintesi. È anche noto che molte sostanze, specialmente nelle soluzioni, sono sempre sotto forma di ioni.
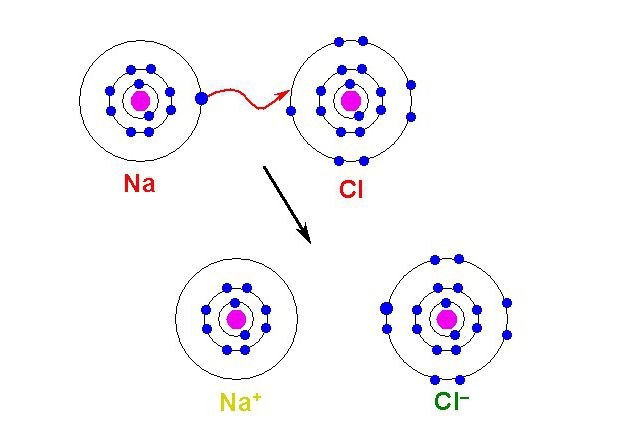
Nomenclatura e classificazione degli ioni
Gli ioni sono carichi di atomi o di un gruppo di atomi che hanno perso o acquisito elettroni durante una reazione chimica. Costituiscono gli strati esterni dell'atomo e possono essere persi a causa della bassa forza di gravità del nucleo. Quindi il risultato del distacco dell'elettrone è uno ione positivo. Inoltre, se un atomo ha una forte carica nucleare e uno stretto guscio di elettroni, il nucleo è un accettore di elettroni aggiuntivi. Di conseguenza, si forma una particella ionica negativa.
Gli ioni stessi non sono solo atomi con un guscio di elettroni in eccesso o insufficiente. Potrebbe essere un gruppo di atomi. In natura, molto spesso ci sono ioni di gruppo che sono presenti in soluzioni, fluidi biologici di corpi di organismi e nell'acqua di mare. Ci sono un numero enorme di tipi di ioni, i cui nomi sono abbastanza tradizionali. I cationi sono particelle ioniche caricate positivamente e gli ioni caricati negativamente sono anioni. A seconda della composizione sono chiamati diversamente. Ad esempio, cationi di sodio, cationi di cesio e altri. Gli anioni sono chiamati in modo diverso, poiché spesso sono costituiti da molti atomi: anione solfato, anione ortofosfato e altri.
Meccanismo di formazione degli ioni
Gli elementi chimici nei composti sono raramente elettricamente neutri. Cioè, non sono quasi mai in uno stato di atomi. Nell'educazione legame covalente, che è considerato il più comune, anche gli atomi hanno una certa carica e la densità degli elettroni si sposta lungo i legami all'interno della molecola. Tuttavia, la carica ionica non si forma qui, perché l'energia del legame covalente è inferiore all'energia di ionizzazione. Pertanto, nonostante la diversa elettronegatività, alcuni atomi non possono attrarre completamente gli elettroni dello strato esterno di altri.
Nelle reazioni ioniche, dove la differenza di elettronegatività tra gli atomi è abbastanza grande, un atomo può prendere gli elettroni dello strato esterno da un altro atomo. Quindi il collegamento creato è fortemente polarizzato e rotto. L'energia spesa su questo, che crea una carica ionica, è chiamata energia di ionizzazione. Per ogni atomo, è diverso ed è indicato nelle tabelle standard.
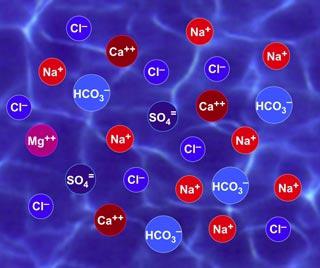
La ionizzazione è possibile solo nel caso in cui un atomo o un gruppo di atomi sia in grado di donare elettroni o accettarli. Il più spesso questo è osservato in soluzione e cristalli di sale. Il reticolo cristallino contiene anche particelle cariche quasi immobili, prive di energia cinetica. E poiché non vi è alcuna possibilità di movimento nel cristallo, la reazione degli ioni si verifica più spesso nelle soluzioni.
Ioni in fisica e chimica
Fisici e chimici stanno studiando attivamente ioni per diversi motivi. Innanzitutto, queste particelle sono presenti in tutto ciò che è noto stati aggregativi della materia. In secondo luogo, l'energia di separazione degli elettroni da un atomo può essere misurata per utilizzarla nelle attività pratiche. Terzo, in cristalli e soluzioni, gli ioni si comportano in modo diverso. E, in quarto luogo, gli ioni consentono una corrente elettrica, e le proprietà fisico-chimiche delle soluzioni variano con le concentrazioni di ioni.
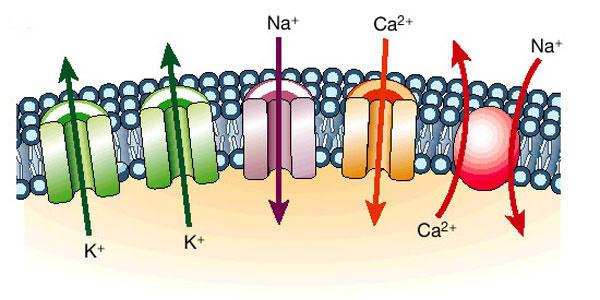
Reazioni ioniche in soluzione
Le soluzioni e i cristalli stessi dovrebbero essere considerati in modo più dettagliato. Nei cristalli di sali ci sono ioni positivi localizzati separatamente, ad esempio cationi di sodio e anioni di cloro negativi. La struttura cristallina è sorprendente: a causa delle forze di attrazione e repulsione elettrostatica, gli ioni sono orientati in modo speciale. Nel caso di cloruro di sodio formano il cosiddetto reticolo di cristallo di diamante. Qui, ogni catione di sodio è circondato da 6 anioni di cloruro. A sua volta, ogni anione di cloruro circonda 6 anioni di cloro. Per questo è semplice sale e in acqua fredda e calda si dissolve quasi alla stessa velocità.

In soluzione, non esiste anche una molecola solida di cloruro di sodio. Ciascuno degli ioni qui è circondato da dipoli d'acqua e si muove caoticamente nel suo spessore. La presenza di cariche e interazioni elettrostatiche porta al fatto che le soluzioni di acqua salata congelano a una temperatura leggermente inferiore a zero e fanno bollire a una temperatura superiore a 100 gradi. Inoltre, se ci sono altre sostanze nella soluzione che possono entrare in un legame chimico, allora la reazione non si verifica con la partecipazione di molecole, ma di ioni. Questo ha creato la dottrina della messa in scena di una reazione chimica.
I prodotti che si ottengono alla fine non si formano immediatamente durante l'interazione, ma vengono gradualmente sintetizzati dai prodotti intermedi. Lo studio degli ioni ha permesso di capire che la reazione procede esattamente secondo i principi delle interazioni elettrostatiche. Il loro risultato è la sintesi di ioni, che interagiscono elettrostaticamente con altri ioni, creando il prodotto finale di reazione all'equilibrio.
sommario
Una particella come un ione è un atomo o un gruppo di atomi caricati elettricamente, che si ottiene durante la perdita o l'acquisizione di elettroni. Lo ione più semplice è l'idrogeno: se perde un elettrone, è solo un nucleo con una carica di +1. Provoca l'ambiente acido delle soluzioni e dei media, che è importante per il funzionamento dei sistemi biologici e degli organismi.
Gli ioni possono avere sia cariche positive che negative. A causa di ciò, nelle soluzioni ciascuna particella entra in interazione elettrostatica con i dipoli di acqua, che crea anche condizioni per la vita e la trasmissione del segnale da parte delle cellule. Inoltre, nella tecnologia degli ioni si evolve ulteriormente. Ad esempio, sono stati creati motori a ioni che equipaggiavano già 7 missioni spaziali della NASA.